- Лимфатические узлы: допустимые размеры
- Предельно допустимый размер лимфатического узла — короткая ось
- Источник:
- Метастатическое поражение шейных лимфатических узлов
- Из чего состоит лимфатическая система шеи
- Классификация лимфатических узлов шеи
- Диагностика
- Осмотр
- Лучевые методы
- Биопсия
- План лечения
- Хирургическое лечение
- Лучевая терапия
- Химиотерапия
- Прогноз
- Наблюдение после лечения
- Стандартный график наблюдения
- Ретрокруральные лимфоузлы что это значит
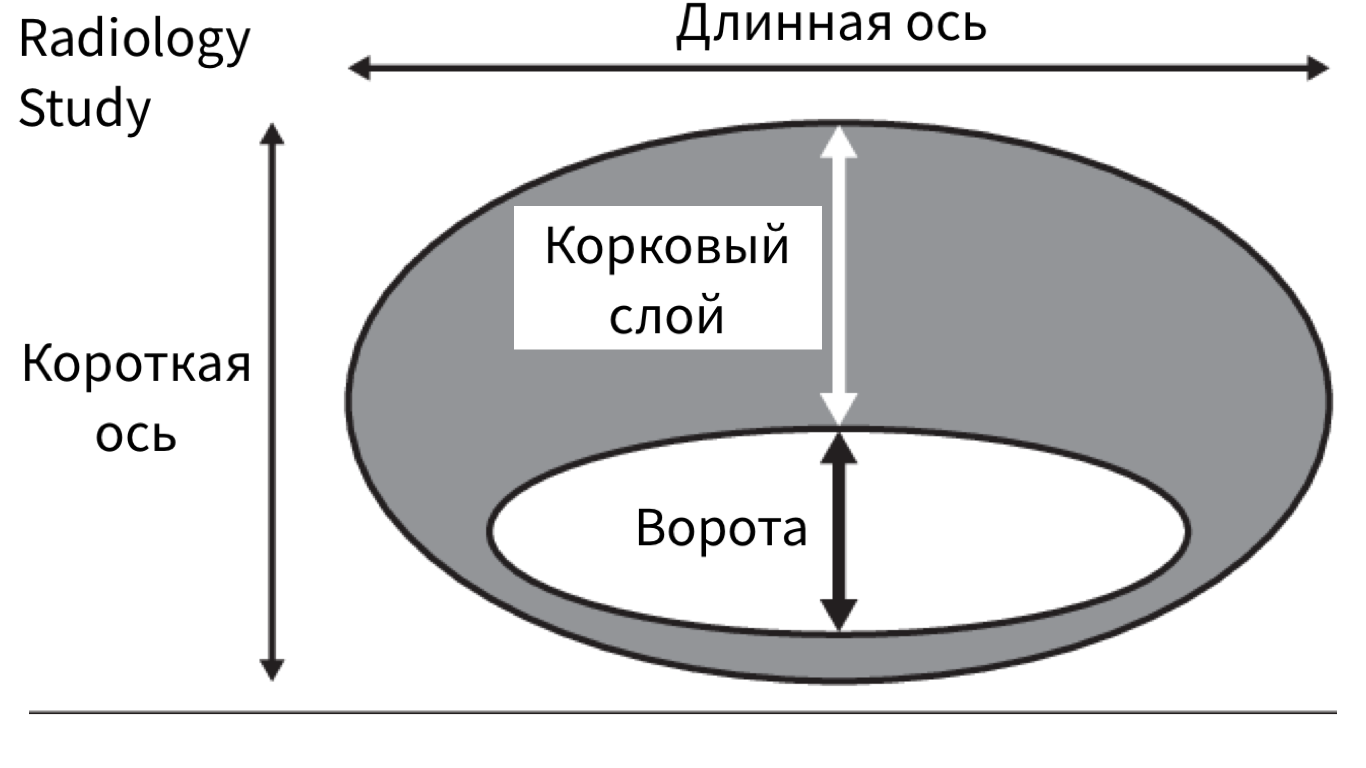
Лимфатические узлы: допустимые размеры
Предельно допустимый размер лимфатического узла — короткая ось
- Большая часть шейных лимфатических узлов — 10 mm
- Подподбородочные и подчелюстные лимфатические узлы — 15 mm
- Ретрофаренгиальные лимфатические узлы -8 mm
- Аксиллярные лимфатические узлы — 10 mm
- Лимфатические узлы следующих областей: паратрахеальной, хиларной, субкаринальной, параэзофагеальной, парааортальной, субаортальной — 10 mm
- Лимфатические узлы перидиафрагмальной области — 5 mm
- Мезентериальные лимфатические узлы — 5 mm
- Лимфатические узлы ретрокрурального пространства — 6 mm
- Паракардиальные лимфатические узлы — 8 mm
- Лимфатические узлы желудочно-печеночной связки — 8 mm
- Лимфатические узлы верхней парааортальной области — 9 mm
- Лимфатические узлы портокавального пространства — 10 mm
- Лимфатические узлы ворот печени — 7 mm
- Лимфатические узлы нижней парааортальной области — 11 mm
- Паховые лимфатические узлы — 15 mm
Источник:
Dorfman RE, Alpern MB, Gross BH, Sandler MA. Upper abdominal lymph nodes: Criteria for normal size determined by CT. Radiology 1991; 180:319-322
Torabi M, Aquino SL, Harisinghani MG. Current Concepts in Lymph Node Imaging. J Nucl Med 2004; 45:1509–1518
Источник
Метастатическое поражение шейных лимфатических узлов
Шейные лимфатические узлы являются частым местом метастазирования злокачественных опухолей, первичный очаг которых располагается в области головы и шеи. К ним, например, относятся плоскоклеточный рак верхних отделов дыхательных путей, а также метастазы рака слюнных желез и щитовидной железы.
Наиболее распространенным клиническим признаком является увеличивающееся образование шеи, которое обычно обнаруживается пациентом или его врачом. При подозрении на метастатическое поражения лимфатических узлов шеи для диагностики и определения наилучшей тактики лечения потребуется осмотр врачом-онкологом, инструментальные методы и биопсия.
Иногда новообразования вне области головы и шеи могут неожиданно метастазировать в шейные лимфатические узлы, что требует особенно тщательной диагностики для выявления первичного очага.
Лечение будет зависеть от типа и локализации первичной опухоли, которая распространилась в лимфатические узлы шеи, и, скорее всего, будет включать в себя комбинацию хирургического вмешательства, лучевой терапии и/или химиотерапии.
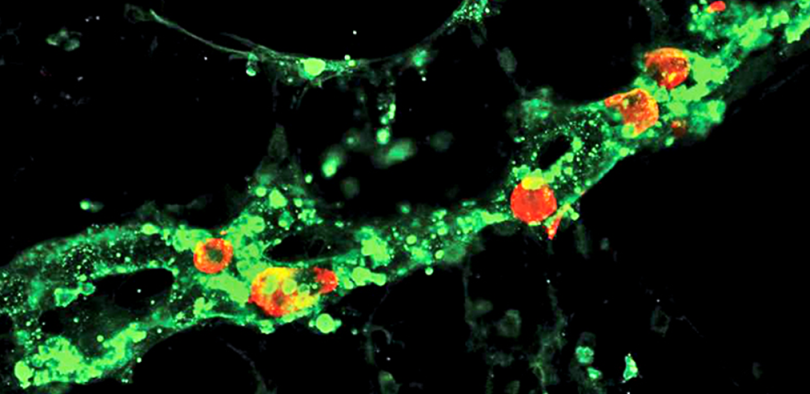
Иммунофлюоресцентная визуализация метастатических клеток меланомы (красные) внутри лимфатических сосудов (зеленые). Масштабная линейка: 100 мкм
(Science Advances/Michael Detmar Group ©)
Из чего состоит лимфатическая система шеи
Лимфатическая система шеи включает в себя сосуды и узлы.
Лимфатические капилляры — это тонкостенные структуры, состоящие из одного слоя эндотелиальных клеток. Они находятся во всех тканях организма и, объединяясь друг с другом, способствуют оттоку лимфатической жидкости в более крупные лимфатические сосуды.
Стенка лимфатических сосудов состоит из трех слоев: внутреннего слоя эндотелиальных клеток, среднего мышечного слоя и внешнего слоя соединительной ткани. В лимфатических сосудах гораздо больше клапанов, чем в венозных, при этом циркуляция лимфы полностью зависит от сжатия сосудов окружающими мышцами. Лимфатические сосуды дренируют лимфу в лимфатические узлы.
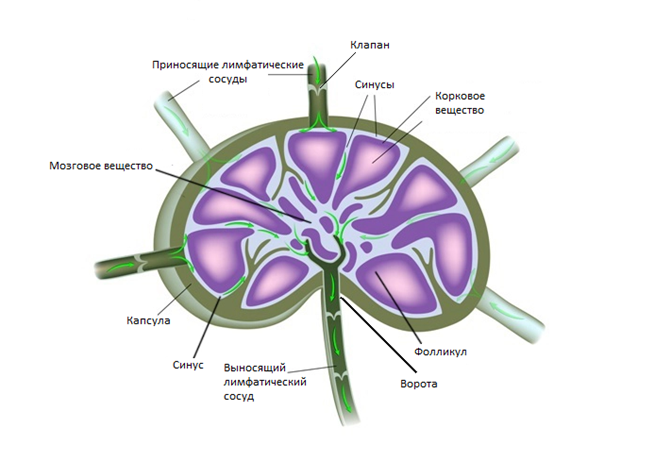
В среднем на каждой стороне шеи расположено до 75 лимфатических узлов. Снаружи узел покрывает капсула, под которой располагается субкапсулярные синусы – место куда попадает лимфатическая жидкость из приносящих лимфатических сосудов. Жидкость проходит сквозь ткань лимфатического узла, которая состоит из коркового и мозгового вещества, а затем выходит через ворота лимфатического узла и попадает в отводящие лимфатические сосуды. В итоге лимфа попадает в венозную систему в месте соустья внутренней яремной и подключичной вены.
Анатомическая структура лимфатического узла (Alila Medical Media/ Shutterstock ©)
Классификация лимфатических узлов шеи
На данный момент во всем мире рекомендована к использованию классификация Американского объединенного комитета по раку (American Joint Committee on Cancer (AJCC)) 8 издания от 2018 года:
- Уровень I (IA и IB): подбородочные и поднижнечелюстные лимфатические узлы;
- Уровень II (IIA и IIB): верхняя яремная группа (делится на 2 подуровня, границей между которыми является добавочный нерв);
- Уровень III: средняя яремная группа;
- Уровень IV: нижняя яремная группа;
- Уровень V (VА и VB): лимфатические узлы заднего треугольника шеи;
- Уровень VI: передние шейные лимфатические узлы;
- Уровень VII: верхние медиастинальные лимфатические узлы.
Уровни лимфатических узлов шеи (Tenese Winslow LLC ©)
Диагностика
Осмотр
При пальпации шеи врач обращает внимание на расположение, размер, плотность и подвижность каждого узла. Особое внимание уделяется узлам, которые кажутся фиксированными к подлежащим сосудисто-нервным структурам и внутренним органам. Описание каждого узла становится важной частью медицинской документации, которая в дальнейшем может использоваться для оценки эффекта лечения.
Лучевые методы
Преимуществами УЗИ перед другими методами визуализации являются цена, скорость исследования и низкая лучевая нагрузка на пациента.
Ультразвуковыми признаками метастатического поражения лимфатических узлов может быть образование сферической формы, нарушение структуры, нечеткие границы, наличие центрального некроза и др.
Поскольку не всегда по УЗИ можно с уверенностью сказать является лимфатический узел пораженным или нет, иногда одновременно выполняют тонкоигольную аспирационную биопсию под ультразвуковым контролем с последующим цитологическим исследованием материала из этого узла. Результат цитологического исследования зависит от навыков врача УЗИ и качества образца (т.е. наличия достаточного количества репрезентативных клеток).
С появлением систем высокого разрешения и специальных контрастных веществ КТ позволяет обнаруживать лимфатические узлы, которые могли быть пропущены при иных методах диагностики.
Ценность МРТ – превосходная детализация мягких тканей. МРТ превосходит КТ в качестве предпочтительного исследования при оценке ряда новообразований головы и шеи, таких как основание языка и слюнные железы. Размер, наличие нескольких увеличенных узлов и центральный некроз – критерии, общие для протоколов исследования КТ и МРТ.
Этот новый метод визуализации все чаще используется для определения стадии опухолей головы и шеи. Метод основан на поглощении 2-фтор-2-дезокси-D-глюкозы (ФДГ) метаболически активными тканями. Исследование также может быть объединено с КТ, чтобы улучшить разрешение получаемого изображения и более точно определить расположение образования.
Биопсия
Биопсия — это удаление небольшого кусочка ткани для исследования под микроскопом или для тестирования в лаборатории на предмет наличия признаков злокачественности. В подавляющем большинстве случаев проводится тонкоигольная аспирационная биопсия. Врач, выполняющий биопсию, может использовать УЗИ или КТ для выполнения процедуры. Иногда тонкоигольная аспирационная биопсия не позволяет поставить окончательный диагноз, и требуются другие виды биопсии, такие как трепан-биопсия или эксцизионная биопсия.
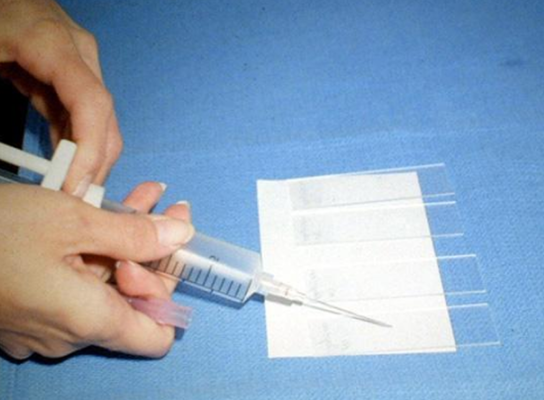 | 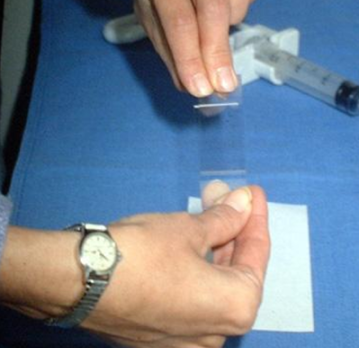 |
| Процесс приготовления предметных стекол для цитологического исследования. Материалом служит содержимое шприца после выполнения тонкоигольной аспирационной биопсии | |
План лечения
После определения диагноза и проведения всех диагностических исследований врач порекомендует оптимальный для пациента курс лечения. В конечном итоге лечение метастатического поражения лимфатических узлов зависит от типа и локализации первичной опухоли.
Существует три различных варианта лечения, которые могут быть использованы отдельно или в комбинации:
- хирургическое вмешательство,
- лучевая терапия,
- химиотерапия.
Хирургическое лечение
Хирургическое лечение обычно включает удаление лимфатических узлов шеи (лимфодиссекция) и последующее гистологическое исследование для точного определения стадии, так как это может существенно повлиять на дальнейшую тактику лечения. Хоть и не всегда, но чаще всего лимфодиссекция выполняется одновременно с удалением первичной опухоли.
Существуют различные виды лимфодиссекций:
- радикальная лимфодиссекция: удаление всех лимфоузлов, удаление внутренней яремной вены, удаление мышц и нервов;
- модифицированная радикальная лимфодиссекция: удаление всех лимфоузлов с сохранением мышц. Нервы и/или внутренняя яремная вена могут быть удалены;
- селективная лимфодиссекция: удаление только определенных групп лимфоузлов.
Лучевая терапия
Лучевая терапия может быть назначена в качестве самостоятельного метода лечения в послеоперационном периоде, чтобы снизить вероятность рецидива либо в комбинации с химиотерапией в качестве самостоятельного или адъювантного лечения. Обычно адъювантная лучевая терапия необходима, если по результатам гистологического исследования обнаруживается несколько пораженных лимфатических узлов.
Химиотерапия
Химиотерапия обычно добавляется к лучевой терапии в качестве самостоятельного или адъювантного (послеоперационного) лечения. В некоторых случаях может использоваться индукционная химиотерапия с целью уменьшения объема образования и последующего хирургического вмешательства.
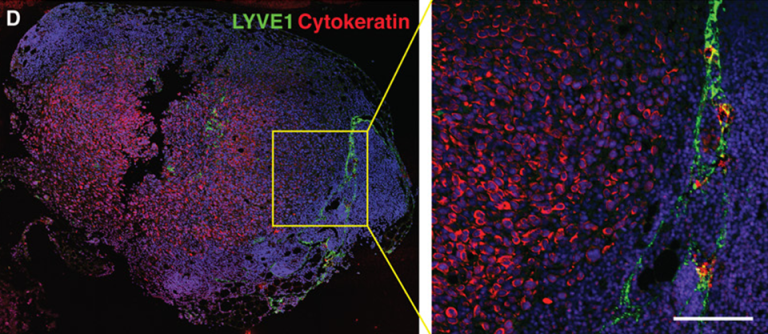
Иммунофлюоресцентная визуализация метастатически пораженного лимфатического узла с окраской на Цитокератин (красный) – маркер характерный для опухолевых клеток эпителиального происхождения. Масштабная линейка: 50 мкм
(Science Advances/Michael Detmar Group ©)
Прогноз
Метастазы в лимфатические узлы шеи могут возникать при онкологических заболеваниях различных локализаций, поэтому давать прогностические оценки для этой группы пациентов следует только после выявления первичной опухоли.
Факторы, влияющие на прогноз:
- стадия заболевания,
- локализация первичной опухоли,
- гистологический подтип и степень дифференцировки,
- количество и размер пораженных лимфатических узлов,
- характеристика края резекции опухоли.
Наблюдение после лечения
Пациенты должны регулярно посещать своего специалиста по опухолям головы и шеи для оценки состояния на предмет любых признаков рецидива заболевания.
Стандартный график наблюдения
В первые 1–2 года осмотр и сбор жалоб рекомендуется проводить каждые 3–6 месяца, на сроке 3–5 лет – один раз в 6–12 месяцев. После 5 лет с момента операции посещать врача необходимо один раз в год или при появлении жалоб. У пациентов с высоким риском рецидива перерыв между обследованиями может быть сокращен.
Список литературы:
- RUSSCO Практические рекомендации по лечению злокачественных опухолей головы и шеи. 2020г
- NCCN Clinical Practice Guidelines in Oncology Head and Neck Cancers Version 1.2021 — November 9, 2020
- DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (Cancer Principles and Practice of Oncology) 11th Edition 2019
- AJCC (American Joint Committee on Cancer). Cancer Staging Manual – 8th Edition. New York, NY: Springer; 2018
- Pisani, Paolo et al. “Metastatic disease in head & neck oncology.” Acta otorhinolaryngologica Italica 2020
- Van den Brekel MW. Lymph node metastases: CT and MRI. Eur J Radiol. 2000
- Chen ZW, Zhu LJ, Hou QY, Wang QP, Jiang S, Feng H. Clinical application of positron-emission tomography for the identification of cervical nodal metastases of head and neck cancer compared with CT or MRI and clinical palpation. Chinese journal of stomatology. 2008
- Qiaoli Ma et al. Unexpected contribution of lymphatic vessels to promotion of distant metastatic tumor spread. ScienceAdvances 08 Aug 2018
- Sun, J et al. Computed tomography versus magnetic resonance imaging for diagnosing cervical lymph node metastasis of head and neck cancer: a systematic review and meta-analysis. OncoTargets and therapy. 2015
- Robbins KT, Shaha AR, Medina JE, et al. Consensus statement on the classification and terminology of neck dissection. Arch Otolaryngol Head Neck Surg. 2008
- López, Fernando et al. Cervical lymph node metastases from remote primary tumor sites. Head&neck 2016
Авторская публикация:
Амиров Николай Сергеевич
Клинический ординатор НМИЦ онкологии им. Н.Н. Петрова
Под научной редакцией:
Раджабова З.А.
Заведующий отделением опухолей головы и шеи
НМИЦ онкологии им. Н.Н. Петрова,
врач-онколог, научный сотрудник, кандидат медицинских наук, доцент
Источник
Ретрокруральные лимфоузлы что это значит
а) Терминология:
1. Синонимы:
• Неходжкинская лимфома (НХЛ), лимфома Ходжкина (ЛХ)
2. Определение:
• Гемобластоз, субстратом которого являются лимфоциты
1. Общие характеристики:
• Локализация:
о Брыжейка: часто прилегает к сосудам брыжейки или окружает их
о Забрюшинное пространство: парааортальные (несколько подгрупп) узлы, а также узлы, расположенные вдоль подвздошных сосудов
• Размер:
о Как правило, узлы более 1 см в наименьшем размере для мезентериальных и парааортальных лимфатических узлов:
— Увеличенные ретрокруральные лимфатические узлы: более 6 мм
• Морфология:
о Круглый или неправильный контур
о Смещение или отсутствие жировой клетчатки ворот лимфатического узла
о Отдельные узелки мягких тканей, находящиеся в пределах брыжейки или заполняющие парааортальное пространство
2. КТ при ретроперитонеальной и мезентериальной лимфоме:
• КТ с контрастированием:
о Увеличенные узлы (обычно более 1 см в наименьшем размере) для мезентериальных и парааортальных лимфатических узлов:
— Ретрокруральные лимфатические узлы считают увеличенными при размере более 6 мм
о Сплошная мягкая ткань может окружать сосуды брыжейки и аорту/НПВ
о Смещение аорты от позвоночника (нехарактерно для доброкачественного процесса)
о Контрастирование лимфатических узлов, плотность которых приближена в мышечной
о У пациентов при отсутствии лечения редко происходит кальцификация лимфатических узлов (менее 1%) или кистозное перерождение
о Узлы при НХЛ, как правило, больше, чем ЛХ:
— Для лимфатических узлов при НХЛ также более характерно фрагментированное распределение
— Мезентериальную лимфаденопатию чаще встречают при НХЛ (более 50%), чем при ЛХ (менее 5%)
о При НХЛ перипанкреатическиелимфатическиеузлы могут имитировать опухоль поджелудочной железы
о У 25% больных с впервые выявленной ЛХ вовлечены парааортальные лимфатические узлы по сравнению с 50% при НХЛ
о ЛХ: как правило, в начальной стадии вовлечены верхние парааортальные лимфатические узлы с отсутствием непораженных участков
о При ЛХ лимфатические узлы могут быть нормальных размеров, но при этом содержат микроскопическую опухоль, что приводит к ложноотрицательному результату при КТ
3. МРТ при ретроперитонеальной и мезентериальной лимфоме:
• Т1-ВИ:
о Характерна лимфаденопатия с низкой ИС
• Т2-ВИ:
о Характерна лимфаденопатия с высокой ИС
о При низкой ИС можно предположить фиброз после лечения заболевания
• ДВИ:
о Характерна ограниченная диффузия
• Т1-ВИ С+:
о Лимфатические узлы без участков некроза, контрастирование аналогично мышечной ткани
о Гетерогенное контрастирование при некротизированных или частично излеченных лимфатических узлах
4. УЗИ:
• Режим серой шкалы:
о Лимфатические узлы от гипоэхогенных до гетерогенных:
— Округлой или неправильной формы
— Деформация/отсутствие нормальной жировой клетчатки ворот лимфатического узла
5. Радионуклидная диагностика:
• ПЭТ:
о Гиперметаболические узлы демонстрируют повышенное поглощение ФДГ
о Чувствительность для ПЭТ составляет 90-95% по сравнению с 80-85% для КТ с контрастированием
о Большая чувствительность к лимфомам грудной полости (более 90%), чем брюшной или тазовой полости (более 75%)
о Позволяет увеличить выявление опухолей скрытых локализаций (например, кости, мышцы, отдаленные/не увеличенные узлы):
— Может изменить стадию заболевания в 10-40% случаев
— Изменяет лечение в 25% случаев
о Исследование эффективно для определения раннего ответа на химиотерапию:
— Снижение поглощения ФДГ предшествует уменьшению размеров
о Помогает дифференцировать остаточную лимфому от постлучевого фиброза
о Низкая чувствительность к выявлению В-клеточной лимфомы и мукоза-ассоциированной лимфоидной ткани (MALT)
6. Советы по визуализации:
• Лучший метод визуализации:
о ПЭТ/КТ, КТ с контрастированием, МРТ
• Рекомендации по протоколу исследования: о ПЭТ/КТ: высокочувствительный метод
о КТ с контрастированием: реконструкция коронарных срезов эффективна при оценке лимфатических узлов
о МРТ Т2 ДВИ + постконтрастное Т1-ВИ в режиме подавления сигнала от живой ткани
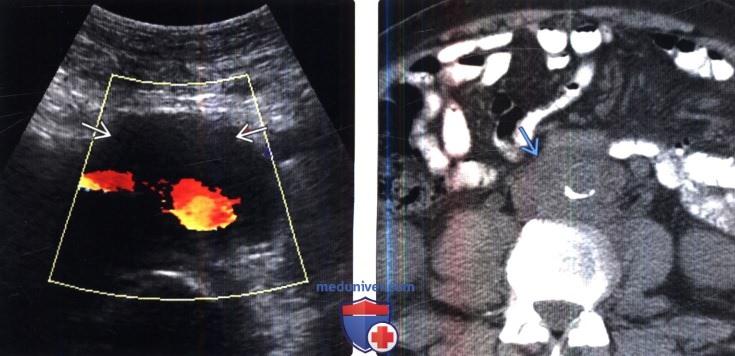
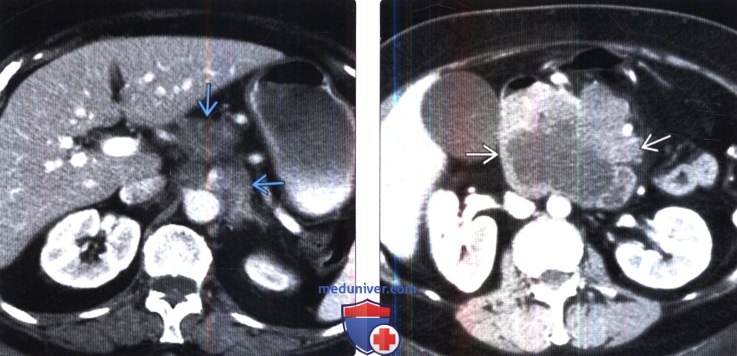
(Справа) Бесконтрастная КТ, аксиальная проекция (этот же пациент): пораженные лимфатические узлы при НХЛ заполняют парааортальное пространство и смещают аорту от позвоночника.
в) Дифференциальная диагностика ретроперитонеальной и мезентериальной лимфомы:
1. Метастазы забрюшинного пространства:
• Увеличенные отдельные узлы, как правило, не «слившиеся»
• Кальцификация при некоторых опухолях (т.е. муцинозная аденокарцинома)
2. Метастазы рака яичек:
• Узлы увеличены вдоль семенной вены, так как она впадает в НПВ (справа) и в почечную вену (слева)
• Увеличенные лимфатические узлы расположены ипсилатерально по отношению к тестикулярной опухоли
3. Забрюшинная саркома:
• Односторонняя крупная гетерогенная опухоль забрюшинного пространства
• Смещение сосудов или органов
• Гетерогенная жировая плотность при липосаркоме
4. Нейрогенная опухоль забрюшинного пространства:
• Параганглиома, ганглионеврома, шваннома
• Параспинальное расположение и расширение межпозвонкового отверстия
5. Внутрибрюшной туберкулез:
• Лимфатические узлы низкой плотности; отграниченный асцит
6. Ретроперитонеальный фиброз:
• Как правило, ограничен тканями, окружающими аорту и НПВ
7. Другие:
• Саркома Капоши: гиперваскуляризированные забрюшинные лимфатические узлы у больных СПИДом
• Болезнь Каслмана (ангиофолликулярная лимфоидная гиперплазия): гиперваскуляризированные забрюшинные лимфатические узлы
• Синдром растущей тератомы: узловая опухоль водной или жировой плотности, возникшая вследствие развития материнской тератомы после химиотерапии несеминомной опухоли яичек
• Саркоидоз: лимфаденит, проявления со стороны респираторного тракта, поражение печение и селезенки
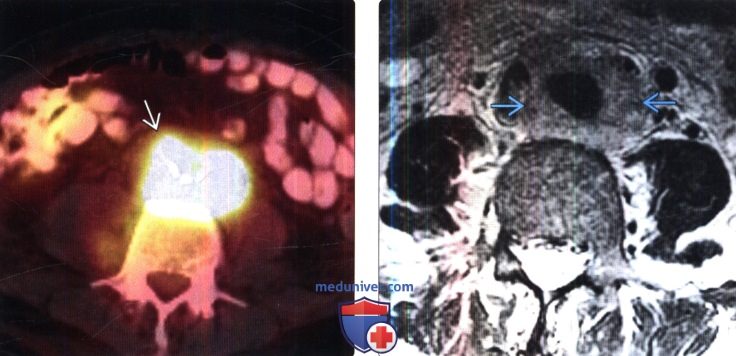
(Справа) МРТ, Т2-ВИ, SS FSE, аксиальная проекция: у этого же пациента выявлено парааортальное образование , имеющее ИС от высокой до умеренной.
1. Общие характеристики:
• Этиология:
о Неизвестна; описаны многочисленные факторы риска
• Генетика:
о Существует несколько типов НХЛ, связанных с онкогенами Bel 1, 2, 3 и 6
2. Стадирование, степень дифференцировки, классификация ретроперитонеальной и мезентериальной лимфомы:
• ВОЗ выделяет более 80 форм лимфомы
• Классификация Анн Арбор:
о I стадия: лимфатические узлы одной области/экстралимфатическая локализация
о II стадия: лимфатические узлы двух или более областей по одну сторону диафрагмы (в том числе единичная экстралимфатическая локализация)
о III стадия: вовлечение групп лимфатических узлов по обе стороны диафрагмы
о IV стадия: диффузное поражение одной или более экстралимфатической локализации (печень, легкие, костный мозг)
3. Макроскопические и хирургические признаки:
• Для определения подтипов предпочтительна эксцизионная или трепан-биопсия (кор-биопсия)
4. Микроскопия:
• ЛХ:
о Несколько злокачественных клеток на фоне нормальных Т-лимфоцитов и воспалительных клеток
о Злокачественные клетки: клетки Рид-Штернберга и варианты:
— Лакунарные клетки, одноядерные и плеоморфные варианты
о Деформация структуры лимфатического узла
о Гистологические подтипы: нодулярный склероз, лимфоидное преобладание, смешанноклеточный, лимфоидное истощение
• НХЛ:
о Классификация, как правило, основана на критериях ВОЗ
о Тип клетки-предшественницы определяет подтип (В-клетка, Т-клетка и др.)
(Справа) КТ с контрастированием, аксиальная проекция: визуализирована панкреатическая НХЛ в виде массивного образования в области головки поджелудочной железы. Лимфома расположена в перипанкреатической группе лимфатических узлов, однако внешне может имитировать первичную опухоль поджелудочной железы.
д) Клинические особенности:
1. Клиническая картина ретроперитонеальной и мезентериальной лимфомы:
• Наиболее распространенные признаки/симптомы:
о Лихорадка, ночная потливость, потеря веса
о Другие признаки/симптомы: образование в подмышечной, паховой областях или в области шеи
• Клинический профиль:
о Пациент молодого возраста с пальпируемым узловым образованием
2. Демография:
• Возраст:
о ЛХ-бимодальный; два пика заболеваемости:
— 20-24 лет
— 80-84 лет
о НХЛ: увеличение заболеваемости с повышением возраста
• Пол:
о ХЛ: несколько чаще у мужчин
о НХЛ: в возрасте до 45 лет, чаще у мужчин:
— В возрасте после 45 лет гендерные различия отсутствуют
• Этнос:
о ХЛ: выше у кавказцев
• Эпидемиология:
о 5% впервые выявленных онкологических заболеваний в США:
— ЛХ: — 8000 случаев в год в США
— НХЛ: — 50000 случаев в год в США
о Повышение заболеваемости вследствие СПИД-ассоциирован-ной НХЛ и трансплантации органов
о Третья по распространенности причина смерти от онкологических заболеваний
3. Течение и прогноз:
• ЛХ: в 80% случаев применяют химиолучевую терапию или трансплантацию стволовых клеток
• НХЛ: в зависимости от степени дифференцировки и стадии:
о При НХЛ прогноз, как правило, хуже, чем ЛХ
о Самый неблагоприятный прогноз: при СПИД-ассоциированной НХЛ
о Неблагоприятный прогноз в случае отсутствия ответа на первый курс терапии
4. Лечение ретроперитонеальной и мезентериальной лимфомы:
• Варианты, риски, осложнения:
о ХЛ: первичная химио- или лучевая терапия; трансплантация стволовых клеток при неэффективности лечения или рецидиве
о НХЛ: первичное лечение-химиотерапия; трансплантация стволовых клеток при неэффективности лечения или рецидиве
е) Диагностическая памятка:
1. Следует учесть:
• Метастазы карцином в лимфатические узлы
2. Эталон интерпретации изображений:
• Отдельные узлы мягких тканей или сливающаяся мягкая ткань в брыжейке и/или парааортальных пространствах
ж) Список использованной литературы:
1. Barrington SF et al: Role of imaging in the staging and response assessment of lymphoma: consensus of the International Conference on Malignant Lymphomas Imaging Working Group. J Clin Oncol. 32(27):3048-58, 2014
2. Cheson BD et al: Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol. 32(27):3059-68, 2014
3. Kostakoglu L et al: Current role of FDG PET/CT in lymphoma. EurJ Nud Med Mol Imaging. 41 (5):1004-27, 2014
4. Allen-Auerbach Metal: PET/computed tomography and lymphoma. Radiol Clin North Am. 51 (5):833-44, 2013
5. Heller MT et al: Managing incidental findings on abdominal and pelvic CT and MRI, part 3: white paper of the ACR Incidental Findings Committee lion splenic and nodal findings. J Am Coll Radiol. 10(11):833-9, 2013
6. Manzella A et al: Abdominal manifestations of lymphoma: spectrum of imaging features. ISRN Radiol. 2013:483069, 2013
7. Tateishi U et al: Nodal status of malignant lymphoma in pelvic and retroperitoneal lymphatic pathways: PET/СТ. Abdom Imaging. Epub ahead of print, 2009
8. Anis M et al: Imaging of abdominal lymphoma. Radiol Clin North Am. 46(2):265 85, viii-ix, 2008
9. Lee WK et al: Abdominal manifestations of extranodal lymphoma: spectrum of imaging findings. AJR Am J Roentgenol. 191 (1): 198-206, 2008
Редактор: Искандер Милевски. Дата публикации: 23.9.2019
Источник