Клинико-инструментальная характеристика некомпактного миокарда левого желудочка
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
Некомпактный миокард левого желудочка (НМЛЖ) — генетически обусловленное поражение миокарда, манифестирующее сердечной недостаточностью (СН), нарушениями ритма, тромбоэмболиями и внезапной сердечной смертью. НМЛЖ ввиду своей редкости и отсутствия специфических жалоб, физикальных данных впервые как нозологическая единица был описан в 1984 г. R. Eng berding и F. Bender [1]. По данным эхокардиографического исследования у взрослых НМЛЖ выявляется редко — в среднем с частотой 0,014%, но у пациентов со снижением фракции выброса 2 у взрослых и до 1,4 у детей).
C. Lilje и соавт. [3] в 2006 г. предложили количественные критерии для определения степени некомпактности миокарда по отношению слоя «плотного» истинного миокарда (Х) к толщине всей стенки сердца на уровне верхушки ЛЖ (Y): 0,33-0,26 — «мягкая» некомпактность; 0,25-0,2 — умеренная; меньше 0,2 — тяжелая.
Данная величина тесно коррелирует со степенью и скоростью развития СН и имеет прогностическое значение для дальнейшего развития заболевания и возникновения осложнений.
Дифференциальная диагностика
В исследованиях сообщается, что у многих пациентов диагноз был выставлен ошибочно: по убыванию частоты — ДКМП, ГКМП, фиброэластоз, миокардит, рестриктивная кардиомиопатия, перикардит и тромбоз полости ЛЖ.
Прогноз и предикторы неблагоприятного течения заболевания. Летальность в течение 6 лет составляет около 50%. У детей летальность около 17,1%. Предикторы неблагоприятного прогноза:
- Увеличенный конечный диастолический размер ЛЖ при первичной эхокардиографии у пациента.
- Хроническая СН III-IV ФК по NYHA.
- Постоянная форма ФП.
- Блокада ножек пучка Гиса.
Прогноз также ухудшает наличие желудочковых тахиаритмий, что нередко является причиной внезапной сердечной смерти у больных с некомпактным миокардом, которая может быть первым и единственным проявлением НМЛЖ.
Лечение
Специфической терапии НМЛЖ не существует. Проводят симптоматическое лечение застойной СН, нарушений ритма и профилактику тромбоэмболических осложнений. В терминальных стадиях возможна трансплантация сердца.
Клиническое наблюдение
Больной Г., 1962 года рождения, поступил в экстренном порядке в приемно-диагностическое отделение с жалобами на выраженную одышку, в том числе в покое, ортопноэ, увеличение живота, уменьшение количества мочи, отеки нижних конечностей, резкую слабость при незначительной физической нагрузке. Больным себя считает в течение последнего месяца, когда появилась субфебрильная температура, стала нарастать одышка при физической нагрузке и в горизонтальном положении, появились отеки на ногах, увеличился живот. Принимал антибиотики в течение 5 дней. Температура тела нормализовалась, но самочувствие не улучшалось.
При осмотре общее состояние тяжелое. Сознание ясное. Телосложения правильного. Питания удовлетворительного. Кожные покровы бледные. Склеры субиктеричны. Видимые слизистые оболочки цианотичные. Массивные отеки нижних конечностей. Пульс 102 уд/мин, ритмичный, низкого наполнения. АД 140/80 мм рт.ст. Набухание шейных вен. Цианоз лица в горизонтальном положении. Тоны глухие, систолический шум с максимумом в точке Боткина. Частота дыхания 19 в 1 мин. Живот увеличен за счет асцита. При поверхностной пальпации напряжен.
В анализе крови обращает на себя внимание: увеличение D-димера в 24 раза. Ультразвуковое исследование органов грудной и брюшной полостей: увеличение и диффузные изменения печени. Уве ли чение и диффузные изменения поджелудочной железы. Каликоэктазия и кисты паренхимы левой почки. Свободная жидкость в брюшной полости. Двусторонний гидроторакс. Компьютерная томография: косвенные признаки тромбоэмболии мелких ветвей легочной артерии. Признаки инфарктпневмонии SX правого и левого легкого.
По данным ЭКГ имели место: синусовая тахикардия с частотой 104 уд/мин. Увеличение левого и правого предсердия. Выраженные вольтажные критерии гипертрофии ЛЖ. Вторичные изменения в миокарде ЛЖ, связанные с гипертрофией ЛЖ. Неполная блокада левой ножки пучка Гиса (QRS 110 мс).
Эхокардиографическое исследование, выполненное на ультразвуковой системе EKO7 (компании Samsung Medison), установило значительное расширение аорты на уровне синусов Вальсальвы и восходящего отдела — 47/48 мм. Левое предсердие: переднезадний размер 50 мм. По длинной оси — 73 мм. Конечный диастолический размер ЛЖ — 75 мм, конечный систолический размер ЛЖ — 63 мм, фракция выброса ЛЖ — 33%. Правый желудочек (на уровне трикуспидального клапана) — 47 мм. Правое предсердие — 47 х 70 мм. Значительное расширение ствола легочной артерии (ЛА) — 41 мм. Расщепление листков перикарда за задней стенкой ЛЖ — 5 мм, за правым предсердием — до 6 мм. Митральная регургитация II степени. Трикуспидальная регургитация III степени. Аортальная регургитация II степени. Регургитация на клапане ЛА — II степени. Среднее гемодинамическое давление в ЛА (по трикуспидальной регургитации) — 46 мм рт.ст. Максимальное давление в ЛА — 72 мм рт.ст.
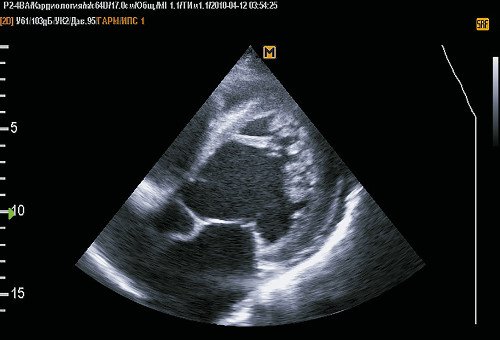
Стенка ЛЖ в средней и верхушечной области представляет собой 2 слоя: наружный, толщиной 5,5 мм, однородной структуры (компактный миокард) и внутренний, представленный широкими трабекулами, лакунами, доходящими до компактного слоя (по типу губчатой структуры). На всем протяжении лакун регистрируется кровоток. Толщина некомпактного слоя в средней части ЛЖ до 16 мм, в области верхушки до 29 мм. На сканограммах (рис. 1-4) при хорошем уровне ультразвуковой визуализации видны четкие признаки некомпактности миокарда ЛЖ. Таким образом, имеется типичная эхокардиографическая картина НМЛЖ. Данное клинико-эхокардиографическое описание представляет собой первое клиническое выявление и описание НМЛЖ в Приволжском федеральном округе.
Рис. 1. Пятикамерная позиция при локации с верхушки.
Источник
Повышенная трабекулярность верхушки левого желудочка что это значит
Шомахов Р.А., Макаренко В.Н., Голухова Е.З., Машина Т.В.
Вышеперечисленные жалобы стали беспокоить около 5 лет назад. Тогда же при плановой диспансеризации на ЭКГ выявлена частая желудочковая экстрасистолия (ЖЭС). Выполнено холтеровское мониторирование, выявлено 23 тысячи ЖЭС, эпизоды бигеминии, тригеминии, пароксизмы неустойчивой желудочковой тахикардии (ЖТ). Назначен соталол, который из-за отсутствия должного антиаритмического эффекта заменен на амиодарон. На фоне лечения число ЖЭС уменьшилось до 6–7 тыс., однако сохранялись короткие пароксизмы ЖТ. В июне 2012 г. у пациентки развился длительный приступ учащенного сердцебиения с последующей потерей сознания. Бригадой скорой медицинской помощи на ЭКГ зарегистрирован пароксизм устойчивой ЖТ с частотой 204 уд/мин, который купирован внутривенным введением амиодарона. Была консультирована хирургом-аритмологом по месту жительства, рекомендовано ЭФИ с последующей аблацией очагов желудочковых аритмий.
Наследственность со стороны сердечно-сосудистой системы не отягощена, случаев внезапной смерти у ближайших родственников не отмечает.
Состояние при поступлении в НЦССХ им. А.Н. Бакулева РАМН удовлетворительное. Гиперстеническое телосложение, рост – 170 см, масса тела – 110 кг. Индекс массы тела – 38 кг/м2 (экзогенно-конституциональное ожирение 2-й степени). Кожные покровы обычной окраски, нормальной влажности. Периферические отеки отсутствуют. Дыхание в легких везикулярное, проводится во все отделы. Частота дыхания – 17 в мин. Тоны сердца приглушены, аритмичные, ЧСС – 75 уд/мин, АД – 125/80 мм рт. ст. Печень не увеличена, при пальпации безболезненна, по средне-ключичной линии ее край на уровне реберной дуги.
ЭКГ: ритм синусовый, правильный; ЧСС – 61 уд/мин, ЭОС отклонена влево. P – 100 мс, PQ – 140 мс, QRS – 100 мс, QTc – 450 мс. Морфология rS в отведениях II, III, AVF, V1–V4. Единичная желудочковая экстрасистолия. Заключение: блокада передней ветви левой ножки пучка Гиса, единичная желудочковая экстрасистолия.

На рисунках фрагменты холтеровского мониторирования пациентки П.: групповые желудочковые экстрасистолы (слева), пароксизм неустойчивой ЖТ (справа).
Трансторакальная эхокардиограмма. Апикальная четырехкамерная позиция: повышенная трабекулярность миокарда левого желудочка с межтрабекулярными лакунами (указано стрелками).
Заключение: кардиомиопатия, некомпактный миокард левого желудочка, сократительная способность ЛЖ удовлетворительная., ФВ ЛЖ – 61%, недостаточность МК II ст., недостаточность ТК до II ст., умеренное расширение полостей сердца.
Чреспищеводная эхокардиограмма. Среднепищеводная 4-камерная позиция: зоны некомпактного миокарда в области верхушки левого желудочка с переходом на боковую стенку (указано стрелками).
Чреспищеводная эхокардиограмма. Среднепищеводная 2-камерная позиция, режим цветного допплеровского картирования: межтрабекулярные пространства, сообщающиеся с полостью левого желудочка (указано стрелками)
Коронарография: правый тип кровоснабжения миокарда, гемодинамически значимых сужений коронарных артерий не выявлено.
По лабораторным данным изменений не выявлено.
Диагноз: кардиомиопатия; изолированная некомпактность миокарда левого желудочка; умеренная дилатация камер сердца; недостаточность митрального клапана II ст.; недостаточность трикуспидального клапана II ст.; нарушения ритма сердца: желудочковая экстрасистолия 5-й градации по Ryan, пароксизмальная желудочковая тахикардия; синкопальное состояние от июня 2012 г.; артериальная гипертензия II ст.; риск 3; НК II ст. по NYHA; экзогенно-конституциональное ожирение I ст.
Для подтверждения диагноза и определения тактики лечения пациентке выполнено инвазивное ЭФИ и МРТ сердца.
Электрофизиологическое исследование: ретроградного проведения нет; РЭРП ПЖ – 220 мс. При программируемой стимуляции ПЖ тремя стимулами (450–250–300 мс) индуцирован неустойчивый пароксизм полиморфной ЖТ, самостоятельно купировавшийся.
Магнитно-резонансные томограммы сердца. Повышенная трабекулярность миокарда левого желудочка (указано стрелками).
Магнитно-резонансные томограммы сердца. Измерение толщины компактного и некомпактного слоя миокарда левого желудочка. Сокращения: Н – некомпактный слой, К – компактный слой миокарда.
Заключение: умеренное увеличение полостей сердца, повышенная трабекулярность миокарда ЛЖ и ПЖ, неинтенсивные фиброзные изменения миокарда ЛЖ и ПЖ (преимущественно в области верхушки).
Таким образом, в результате обследования у пациентки выявлены диагностические критерии кардиомиопатии некомпактного миокарда левого желудочка:
– двухслойная структура миокарда с истонченным компактным и утолщенным некомпактным слоем в соотношении более 1/2;
– повышенная трабекулярность миокарда левого желудочка;
– глубокие межтрабекулярных щели, сообщающиеся, по данным ЦДК, с полостью левого желудочка при отсутствии иной кардиальной патологии.
Примечательно, что желудочковые нарушения ритма явились единственным клиническим проявлением заболевания.
При выборе тактики лечения от операции РЧА было решено воздержаться ввиду отсутствия убедительных данных об эффективности и безопасности процедуры у пациентов с НМЛЖ. С целью профилактики внезапной сердечной смерти пациентке был имплантирован автоматический кардиовертер-дефибриллятор Biotronik Lumax 340 VR-T с первичной эндокардиальной системой.
Послеоперационный период протекал без осложнений. Помимо амиодарона, к антиаритмической терапии был добавлен бисопролол в дозе 2,5 мг/сут. Пациентка отмечала улучшение самочувствия, отсутствие приступов сердцебиения. Положительная динамика была также по данным ЭКГ и холтеровского мониторирования (желудочковая эктопическая активность представлена 4303 ЖЭС, двух морфологий, из них 2623 одиночных, по типу бигеминии – 6, по типу тригеминии – 315, ранних – 20, вставочных – 1036, парных – 31, триплетов – 2.
За время пребывания в стационаре разрядов дефибриллятора не зафиксировано. Пациентка выписана на 8-е сутки под наблюдение кардиолога по месту жительства.
Представленный клинический случай редкой формы кардиомиопатии – некомпактного миокарда левого желудочка – демонстрирует, что пациенты с некоронарогенными желудочковыми нарушениями ритма требуют тщательного обследования с применением современных методов, которые могут менять наше представление о диагнозе и тактике лечения.
Подробнее о генетических аспектах, патогенезе, клиники и возможных методах лечения некомпактного миокарда левого желудочка в журнале «Креативная кардиология».
Источник
Видео
Некомпактный миокард или гипертрабекулярность левого желудочка/NONCOMPACTION CARDIOMYOPATHY OR LEFT VENTRICULAR HYPERTRABECULARITY
Еще фото
Автор (ы): Л.В. Крашенинников, ветеринарный врач-кардиолог, Инновационный ветеринарный центр Московской ветеринарной академии им. К.И.Скрябина l.krasheninnikov@yandex.ru
Журнал: №6-2017
Ключевые слова: некомпактный миокард левого желудочка (НМЛЖ), гипертрабекулярность, сердечная недостаточность
Kew words: noncompaction cardiomyopathy (NCCMP), hypertrabecularity, heartfailure
Аннотация
Некомпактный миокард левого желудочка – очень редкая форма врожденной кардиомиопатии, характеризующаяся гипертрабекулярностью миокарда левого желудочка. В процессе эмбриогенеза при некомпактном (гипертрабекулярный) миокарде левого желудочка (НМЛЖ) формируются два слоя сердечной мышцы – нормальный компактный и патологический некомпактный. Клинически данный вид кардиомиопатии проявляется желудочковыми аритмиями, сердечной недостаточностью, тромбоэмболией, внезапной смертью, а также может протекать бессимптомно. Основные методы диагностики – эхокардиография, компьютерная томография и магнитно-резонансная томография.
Summary
Left ventricular noncompaction is a very rare form of genetic cardiomyopathy, that is characterized by hypertrabecularity of left ventricle myocardium. During embryogenesis in case of Noncompaction cardiomyopathy (NCCMP) two layers of cardiac myocardium are formed – normal compact and pathological non compact. Clinicaly this type of cardiomyopathy presents with ventricular arrhythmias, heart failure, thromboembolic events, sudden death and also can be asymptomatic. Echocardiography, CT and MRI can be helpful in providing diagnosis of NCCMP.
Некомпактный (гипертрабекулярный) миокард левого желудочка (НМЛЖ), также ранее известный как губчатый миокард, – одна из редких первичных кардиомиопатий, характеризующаяся выраженными трабекулами левого желудочка и глубокими межтрабекулярными углублениями. При этом формируются два слоя – некомпактный со сниженной сократительной функцией и компактный. У людей НМЛЖ встречается в любом возрасте и может быть изолированным или сочетаться с другими врожденными заболеваниями сердца.
Впервые болезнь была описана у ребенка в 1926 г. и долгое время считалась разновидностью апикальной гипертрофической кардиомиопатии (ГКМП). В настоящее время НМЛЖ отнесена к категории неклассифицируемых кардиомиопатий (Европейская классификация).
Этиология, генетика и эмбриогенез
Сердечная мышца развивается из миоэпикардиальной пластинки мезодермы в I триместре беременности, при этом изначально миокард представлен группой раздельных волокон, разделенных между собой широкими синусоидами. Во время эмбриогенеза постепенно происходит уплотнение волокон между собой и сужение межтрабекулярных пространств. Процесс протекает от основания сердца к его верхушке и от эпикарда к эндокарду. Нарушение течения этого процесса приводит к тому, что остаются зоны неуплотненных, «некомпактных» трабекул, разделенных глубокими межтрабекулярными рецессусами (рис. 1).
На сегодняшний день этиология заболевания остается малоизученной. Есть данные о ненаследуемом и наследуемом характере заболевания, преимущественно аутосомно-доминантном и сцепленном с Х-хромосомой. В развитии НМЛЖ у людей могут участвовать различные мутации генов, в том числе кодирующих синтез саркомеров, – MYH7, ACTC, TNNT2, ответственных за развитие ГКМП – MYBPC3, белков, участвующих в организации цитоскелета, – LDB3, Lamin A/C, кардиоспецифических – CSX, альфа-дистробревина – Cypher/ZASP, дистропина и некоторых других.
В частности, выявлена интересная общая R820W мутация MYBPC3 гена, вызывающая ГКМП у кошек породы рэг-долл, у гомозиготных людей – НМЛЖ и ГКМП, а у гетерозиготных людей экспрессия минимальна.
Распространенность и классификация
В настоящее время в человеческой популяции распространенность заболевания сильно недооценена в связи со сложностями диагностики. Часто данную патологию описывают, как другие формы кардиомиопатий, тромбы, опухоли и т.д.
Заболевание чаще регистрируется у мужчин – до 80% случаев по данным разных авторов. В педиатрической практике НМЛЖ занимает третье место после ГКМП и ДКМП, составляя, по некоторым данным, около 9,2% всех диагностируемых кардиомиопатий. Общая доля заболевания составляет около 0,014% (E. Oechslin). На сегодняшний день описан и гистологически подтвержден один случай бивентрикулярного НМЛЖ без гипертрофии у мейн-куна с A31P мутацией протеина С, ответственного за ГКМП у данной породы кошек, при этом животное наблюдалось каждые 6 мес в течение 6 лет до смерти.
НМЛЖ может быть как изолированным, так и комбинированным с другими кардиомиопатиями, нейропатиями и врожденными пороками сердца. У людей наиболее часто встречается вместе с дефектами межжелудочковой или межпредсердной перегородок, но может сочетаться и с другими врожденными пороками сердца (ВПС).
Патогенез и клиническая картина
Нарушение нормальной архитектуры сердечной мышцы, проявляющееся в виде двух слоев, компактного с нормальной сократительной способностью и некомпактного со сниженной, приводит к снижению общей сократительной способности миокарда желудочка, а нарушение микроциркуляции – к хронической ишемии. Эти два фактора, а также величина некомпактной части сердечной мышцы по отношению к компактной, определяют тяжесть и скорость развития хронической сердечной недостаточности у пациента, при этом страдает как систола, так и диастола, которая в некоторых случаях может быть рестриктивного типа.
Клинически НМЛЖ проявляется хронической сердечной недостаточностью, реже – желудочковыми и наджелудочковыми аритмиями, повышенной вероятностью тромбообразования или протекает бессимптомно.
Развитие хронической сердечной недостаточности связано с систолической и диастолической дисфункциями и возникающей на их фоне кардиомегалией и ретроградным застоем в соответствующих кругах кровообращения.
Ввиду выраженных структурных изменений миокарда, аритмии являются патогномоничным синдромом для НМЛЖ и могут быть единственным проявлением патологии. Наиболее часто встречаются желудочковые нарушения ритма, такие как желудочковая тахикардия и экстрасистолия, при этом механизмы, отвечающие за их развитие, предположительно, схожи с таковыми при аритмогенной кардиомиопатии правого желудочка. Другими часто встречаемыми нарушениями являются фибрилляция предсердий, АВ-блокады и блокады на уровне ножек Гиса, причиной чему служит прогрессирующий эндомиокардиальный фиброз. Синдром WPW встречается реже, при этом дополнительный путь чаще локализуется в переднеперегородочном сегменте в области фиброзного кольца трикуспидального клапана. Дополнительные пути проведения – основная причина внезапной смерти при НМЛЖ.
Повышенная вероятность тромбообразования зависит от нескольких причин. С одной стороны, это увеличенные размеры камер сердца, что особенно важно для кошек, с другой – глубокие межтрабекулярные рецессусы в полости желудочка в совокупности со сниженной насосной функцией сердца.
Первичным методом диагностики НМЛЖ является эхокардиография. В дальнейшем для уточнения диагноза может быть использована магнитно-резонансная и компьютерная томография, в гуманной медицине также используется контрастная вентрикулография.
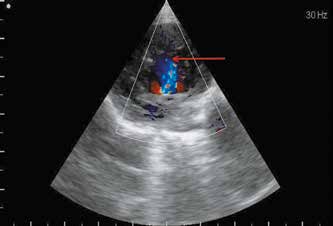
Эхокардиографически НМЛЖ представлен двухслойной структурой миокарда желудочка – тонкий эпикардиальный компактный слой и трабекулярный, с глубокими рецессусами, некомпактный слой, чаще всего локализованный в апикальной области и на свободной стенке левого желудочка. Существует несколько вариантов комбинаций критериев оценки изображения для постановки диагноза НМЛЖ. Одной из наиболее распространенных является соотношение некомпактного слоя к компактному более 2 у взрослых и 1,4 у детей, измеренных в конце систолы, наличие нескольких трабекул в одном срезе и глубоких рецессусов, сообщающихся с полостью левого желудочка, что визуализируется при цветном допплеровском картировании (рис. 2).
Магнитно-резонансная томография является высокочувствительным и специфичным методом диагностики при подозрении на НМЛЖ, особенно при недостаточно четкой визуализации верхушки сердца во время эхокардиографии. Согласно рекомендациям AHA, должны использоваться томографы с мощностью более 1,5 Тесла для получения максимально четкого изображения. Критерием НМЛЖ будет являться наличие двух слоев миокарда, а также выбирается один из нескольких диастолических срезов по длинной или короткой осям с наиболее выраженной трабекулярностью, при этом, в отличие от эхокардиографии, соотношение некомпактного слоя к компактному должно быть более 2,3. Для определения локализации используется 17-сегментарная модель сердца.
НМЛЖ может быть ошибочно принят за различные формы ГКМП, так как при обеих патологиях может иметь место гипертрофия свободной стенки левого желудочка и, что особенно важно, апикальной области. Ошибка описания НМЛЖ как ДКМП связана с тем, что систолическая функция может быть умеренно или значительно снижена, а полость желудочка расширена. Ошибки определения как фиброэластоз и эндомиокардиальный фиброз связаны с тем, что изменения при данных патологиях затрагивают прежде всего апикальную область, которая наиболее трудна для визуальной оценки, и межтрабекулярные рецессусы могут плохо визуализироваться при эхокардиографическом исследовании. При миокардите стенки желудочка могут быть утолщены (у кошек), а систолическая функция может быть снижена (у собак), аналогичные изменения можно встретить при НМЛЖ.
Согласно данным Stöllberger и J. Finsterer, наиболее частым ошибочным диагнозом в порядке убывания будут ГКМП, ДКМП, фиброэластоз, миокардит, РКМП и другие причины.
Лечение и прогноз
Бессимптомные пациенты при отсутствии нарушений ритма и проводимости не требуют специфической терапии. В остальных случаях она ничем не отличается от обычной патогенетической и симптоматической терапии хронической сердечной недостаточности.
Предикторами неблагоприятного прогноза будут являться дилатация камер сердца и тяжелые нарушения ритма и проводимости.
Динамическое наблюдение во всех случаях рекомендуется минимум 2 раза в год.
На прием по направлению терапевта поступил бенгальский котенок в возрасте 3 мес с выявленной рентгенологически кардиомегалией. Единственной жалобой было затрудненное, «хрюкающее» дыхание. Аппетит и переносимость физических нагрузок сохранены полностью. При аускультации выявлен систолический шум слева 2–3-й степени из 6.
ЭКГ – ритм синусовый, ЧСС 208 в 1 мин, нарушений проводимости не выявлено.
Эхокардиография – выявлена повышенная трабекулярность верхушки левого желудочка с характерным «мозаичным» кровотоком (соотношение некомпактного и компактного слоев в диапазоне 1,5–2,2) и апикальной мезовентрикулярной обструкцией с градиентом 55 мм рт. ст. (рис. 3 и 4), умеренная дилатация левого предсердия (13,7 мм, аорта 7 мм, измерения в короткой оси), 3–4-й класс диастолической дисфункции левого желудочка, фракция выброса 66% по Симпсону, выраженный застой по малому кругу кровообращения (ЛВ/ПВЛА 1,5), умеренная регургитация на митральном клапане, признаки легочной гипертензии отсутствуют. Предварительный диагноз на основании данных исследования – неклассифицируемая кардиомиопатия, мезовентрикулярная обструкция на фоне некомпактного развития левого желудочка. Дифференциальный диагноз – апикальная форма гипертрофии левого желудочка. Безусловно, в данном случае диагноз НМЛЖ является строго предварительным и, учитывая крайне редкую частоту встречаемости заболевания, должен быть подтвержден гистологически.
К сожалению, хозяйка животного на повторный прием не явилась и о дальнейшей судьбе пациента ничего не известно. Интересным является тот факт, что этот котёнок – единственный выживший из второго помета. Первый помет, всего пять котят, был полностью мертворожденным. Во втором помете тоже было пять котят: два из них были мертворожденными, двух кошка задавила сразу же после рождения, а единственный выживший котенок спустя 3 мес попал на кардиологический прием с редким заболеванием миокарда.
1. Angelini P. Can Left Ventricular Noncompaction Be Acquired, and Can It Disappear? Texas Heart Institute Journal. 2017; 44 (4) : 264–265. PMC. Web. 27 Oct. 2017.
2. Shemisa K. et al. Left Ventricular Noncompaction Cardiomyopathy. Cardiovascular Diagnosis and Therapy. 2013; 3 (3): 170–175. PMC. Web. 27 Oct. 2017.
3. Ali Sulafa K.M. Ventricular Noncompaction: Over or under Diagnosis? Journal of the Saudi Heart Association. 2009; 21 (3): 191–194. PMC. Web. 27 Oct. 2017.
4. Lin Ying-Nan et al. Left Ventricular Noncompaction Cardiomyopathy: A Case Report and Literature Review. International Journal of Clinical and Experimental Medicine. 2014; 7 (12): 5130–5133. Print.
5. Fazlinezhad A. et al. Echocardiographic Characteristics of Isolated Left Ventricular Noncompaction. ARYA Atherosclerosis. 2016; 12 (5): 243–247. Print.
6. Kittleson M.D. et al. Naturally Occurring Biventricular Noncompaction in an Adult Domestic Cat. Journal of Veterinary Internal Medicine. 2017; 31 (2): 527–531. PMC. Web. 27 Oct. 2017.
7. Zhang W. et al. Molecular Mechanism of Ventricular Trabeculation/compaction and the Pathogenesis of the Left Ventricular Noncompaction Cardiomyopathy (LVNC). American journal of medical genetics. Part C, Seminars in medical genetics. 2013; 163 (3): 144–156. PMC. Web. 27 Oct. 2017.
8. Weir-McCall, Jonathan R. et al. Left Ventricular Noncompaction: Anatomical Phenotype or Distinct Cardiomyopathy? Journal of the American College of Cardiology. 2016; 68 (20): 2157–2165. PMC. Web. 27 Oct. 2017.
9. Jenni R., Oechslin E., Schneider J. et al. Echocardiographic and pathoanatomical characteristics of isolated left ventricular non-compaction: a step towards classification as a distinct cardiomyopathy. 2001; 86: 666–671.
10. Голухова Е.З., Шомахов Р.А. Некомпактный миокард левого желудочка. Креативная кардиология. 2013.
Источник