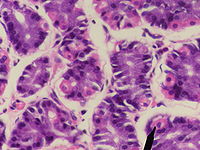
Париетальная (обкладочная) клетка

На рисунке справа изображена обкладочная клетка (взято из статьи О.Д. Лопиной):
- 1 – канальцы
- 2 – микроворсины
- 3 – митохондрии
- 4 – ядро
Число обкладочных клеток (миллионов штук): у мужчин — от 960 до 1 260, в среднем — 1 090; у женщин — от 690 до 910, в среднем — 820.
Строение обкладочной клетки поляризовано: ее противоположные мембраны резко отличаются. Секреция HCl обкладочными клетками происходит на их апикальной мембране, она основана на трансмембранном переносе ионов водорода (протонов) и выполняется протонной помпой — Н + /К + -АТФазой. После активизации молекулы протонных помп встраиваются в мембрану секреторных канальцев обкладочной клетки и переносят ионы водорода из клетки в просвет железы, обменивая их на ионы калия из внеклеточного пространства. Ионный перенос происходит за счет энергии АТФ (34% объема обкладочной клетки занято синтезирующими АТФ митохондриями). Этот процесс предваряет выход из цитозоля обкладочной клетки ионов хлора Cl – . Таким образом в просвете секреторного канальца обкладочной клетки образуется соляная кислота. Благодаря функционированию протонной помпы создается существенный концентрационный градиент ионов водорода и устанавливается значительная разница рН между цитозолем обкладочной клетки (рН 7,4) и просветом секреторного канальца (рН около 1). На базолатеральной мембране располагается ряд рецепторов и для стимулирующих, и для ингибирующих лигандов, регулирующих секреторную активность. Обкладочная клетка тесно связана с энтерохромаффиноподобными клетками, G-клетками, продуцирующими гастрин и D-клетками, продуцирующими соматостатин. Протонную помпы активизирует стимуляция её рейепторов: гастрином G–рецепторов, ацетилхолином М3–рецепторов, гистамином Н2–рецепторов. Рецепторы для соматостатина, простагландинов, эпидермального фактора роста участвуют в обратном процессе — торможении секреции HCl, в том числе стимулированной гистамином (Т.Л. Лапина).
Функциональная схема обкладочной (париетальной) клетки (Дубинская Т.К. и др.)
А) фаза покоя: 1 — секреторные канальцы; 2 — тубуловезикулы
Б) фаза секреции соляной кислоты, образование ионообменных транспортных систем: 1 — секреторные канальцы; 2 — ионные каналы; 3 — протонная помпа
Секреторная активность обкладочной клетки обеспечивается тремя основными эффекторными системами, способными к синергизму:
- гистамин активирует Н2–рецепторы, связанные с аденилатциклазой
- гастрин действует через G–рецепторы, связанные с фосфолипазой С, расщепляющей фосфатидилинозитол
- ацетилхолин, медиатор парасимпатического отдела вегетативной нервной системы, также действует через активацию инозитольного цикла
Каждый из основных трех стимуляторов (гистамин, гастрин и ацетилхолин) способен к самостоятельному эффекту. Ацетилихолин и гастрин усиливают действие гистамина. Этот эффект, скорее всего, связан с влиянием обоих медиаторов на поступление кальция. Антихолинергические агенты снижают эффекты гастрина и гистамина. Блокаторы Н2–рецепторов тормозят действие гастрина и ацетилхолина. Таким образом, максимальная секреторная активность обкладочной клетки возможна лишь при нормальном функционировании всех стимулирующих рецепторов (Бельмер С.В. и др.).
На рисунке справа (А.В. Яковенко) схематически показаны механизмы регуляции секреции соляной кислоты в желудке. Голубым изображена обкладочная (париетальная) клетка, G — гастриновый рецептор, Н2 — гистаминовый рецептор, М3 — ацетилхолиновый рецептор.
Механизмы снижения кислотности желудка
Так как кислота является важнейшим фактором образования язв, эрозий, развития гастритов, то при лечении таких (кислотозависимых) заболеваний важно добиться уменьшения кислотности в органах желудочно-кишечного тракта. Этого можно добиться с помощью операции ваготомии, заключающейся в рассечении вагусного нерва или его ветвей, стимулирующих секрецию кислоты в желудке, однако чаще всего для этого используют различные фармакологические средства. За исключением антацидов, химически нейтрализующих уже секретированную кислоту, остальные препараты действуют на уровне обкладочных (париетальных ) клеток, тормозя тем или иным способом процесс секреции. На рисунке ниже схемотически изображена париетальная клетка, механизм её регуляции и места приложения действия различных блокаторов секреции и антацидов:
Регуляция секреции соляной кислоты и место приложения действия блокаторов секреции и антацидов (Калинин А.В.). Обозначения: M1R и M2R — рецепторы ацетилхолина, GR — рецепторы гастрина, Н2R — рецепторы гистамина, PP — протонная помпа, ВСС — антагонист кальция (блокатор Ca 2+ -рецепторов)
Источник
Париетальные клетки
Париета́льная кле́тка (лат. cellula parietalis ) (синонимы обкла́дочная кле́тка, гландулоци́т париета́льный (лат. glandulocytus parietalis )) — клетка желудка, секретирующая соляную кислоту и внутренний фактор Кастля.
Содержание
Общие сведения
Париетальные клетки располагаются в наружной части фундальных желёз желудка. Фундальные (синоним главные) железы составляют основную часть желёз области дна, тела и интермедиальной зоны желудка. У мужчин число париетальных клеток — от 0,96 до 1,26 миллиарда, в среднем — 1,09 миллиарда; у женщин — от 0,69 до 0,91 миллиарда, в среднем — 0,82 миллиарда. Один миллиард париетальных клеток за один час секретирует в среднем 23 ммоль соляной кислоты. Максимальные объём секреции в час соляной кислоты у мужчин 22—29 ммоль, у женщин — 16—21 ммоль. [1]
Секреция соляной кислоты
Секреции соляной кислоты париетальными клетками основан на трансмембранном переносе ионов водорода (протонов) и осуществляется специфическим протонным насосом — Н + /К + -АТФазой. При активизации молекулы Н + /К + -АТФазы встраиваются в мембрану секреторных канальцев париетальной клетки и за счет энергии Н + /К + -АТФазы переносят ионы водорода из клетки в просвет железы, обменивая их на ионы калия из внеклеточного пространства. Этому процессу предшествует выход из цитоплазмы париетальной клетки ионов хлора, таким образом, в просвете секреторного канальца париетальной клетки и образуется соляная кислота. Н + /К + -АТФаза создаёт значительный градиент ионов водорода, вследствие чего устанавливается значительная разница рН между цитоплазмой париетальной клетки (рН = 7,4) и просветом секреторного канальца (рН около 1). Ни одна из других клеток человеческого организма никогда не граничит со средой с такими низкими рН.
Важнейшими стимуляторами секреции соляной кислоты в желудке являются гистамин, гастрин и ацетилхолин, которые достигают париетальные клетки через кровь и действуют через специфические клеточные рецепторы, располагающиеся на базальной мембране (направленной вглубь стенки желудка) париетальных клеток: гистаминовые (Н2), гастриновые (G) и ацетилхолиновые (М3). В результате их воздействия в париетальных клетках увеличивается концентрация кальция и циклического аденозинмонофосфата (цАМФ), что приводит к активации тубуловезикул, содержащих Н + /К + -АТФазы.
Важнейшие ингибиторы секреции соляной кислоты — простагландины и соматостатин.
Секреция внутреннего фактора
Париетальная клетка также секретирует так называемый «внутренний фактор», гликопротеин, отвечающий за абсорбцию витамина B12 в желудке и всасывание его в подвздошной кишке.
Источник
Париетальные клетки желудка что это значит
Аутоантитела к клеткам желудка, секретирующим соляную кислоту и внутренний фактор Кастла, появление которых при аутоиммунном процессе имеет патогенетическое значение в атрофии слизистой желудка, нарушении всасывания витамина В12 и развитии пернициозной анемии.
Синонимы английские
Gastric Parietal Cell Antibodies; GPA; Antiparietal cell antibody; APCA.
Непрямая реакция иммунофлюоресценции.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Аутоиммунный гастрит – вариант атрофического гастрита (хронического гастрита типа А). Его причиной является выработка собственной иммунной системой антител к париетальным клеткам слизистой желудка. Заболевание бывает длительно не диагностированным вследствие субклинического течения, отсутствия жалоб и явных объективных изменений пищеварения. Аутоиммунный гастрит может протекать самостоятельно или в сочетании с аутоиммунными процессами в щитовидной железе, алопецией и витилиго.
Появление антител к париетальным клеткам при аутоиммунном гастрите приводит к разрушению данной популяции клеток, хроническому воспалению, прогрессирующей атрофии слизистой с кишечной метаплазией. Париетальные (обкладочные) клетки желудка расположены преимущественно в железах слизистой оболочки дна желудка. Их главная функция – секреция соляной кислоты, которая является важным компонентом пищеварения человека, и внутреннего фактора Кастла, необходимого для всасывания витамина В12 из пищи.
Антигенами для АПКЖ являются поверхность париетальной клетки, митохондрии и бета-субъединица Н+/К+-АТФазы, обеспечивающей функцию протонного насоса, необходимого для секреции соляной кислоты в полость желудка. Повреждение париетальных клеток вызывает снижение секреции соляной кислоты (гипохлоргидрию) или ее полное отсутствие (ахлоргидрию, ахилию), что ведет к нарушению всасывания многих питательных веществ (мальабсорбции). При дефиците внутреннего фактора Кастла в кишечнике нарушается абсорбция витамина В12, без которого не происходит полноценного формирования красных кровяных телец в костном мозге, развивается В12-дефицитная (пернициозная, мегалобластная) анемия.
Антитела к париетальным клеткам желудка присутствуют у 90 % людей с пернициозной анемией и в 30 % случаев – у их близких родственников. Для данной патологии АПКЖ являются выскоспецифичными, но большая чувствительность характерна для антител к внутреннему фактору Кастла, который обнаруживается у 50 % пациентов с пернициозной анемией.
Титр антител не коррелирует с тяжестью атрофического процесса в желудке, поэтому для мониторинга течения заболевания не применяется.
Для чего используется исследование?
- Для диагностики мегалобластной (пернициозной) анемии аутоиммунного генеза;
- длядиагностики причин дефицита витамина В12;
- длядиагностики аутоиммунного гастрита.
Когда назначается исследование?
- При выявлении гиперхромной гипорегенераторной анемии по результатам клинического анализа крови;
- при клинических признаках пернициозной (мегалобластной) анемии (бледность, общая слабость, онемение или ощущение покалывания в конечностях, нейропатия, ярко-красный, «лакированный» язык).
Что означают результаты?
Референсные значения: Причины повышения:
- аутоиммунный гастрит и пернициозная анемия (у 90 % больных);
- аутоиммунный гастрит без пернициозной анемии
- патология щитовидной железы (при тиреоидите Хашимото выявляется у 30 % больных);
- сахарный диабет;
- рак желудка;
- язвенная болезнь желудка;
- миастения;
- болезнь Аддисона;
- железодефицитная анемия;
- витилиго;
- очаговая алопеция.
Что может влиять на результат?
Ложноположительные результаты могут быть получены при повышенном уровне иммунных комплексов и гетерофильных антител в крови.
Антитела могут выявляться у 2 % здоровых людей и часто обнаруживаются у лиц старше 60 лет без пернициозной анемии.
Источник
Париетальные клетки желудка что это значит
Желудок выполняет ряд пищеварительных и не пищеварительных функций, нарушение которых в условиях патологии может привести к расстройствам не только желудочного и кишечного пищеварения, но и к развитию анемий, к гормональному дисбалансу, нарушению кислотно-основного состояния, электролитного баланса и другим сдвигам. Основными функциями желудка являются секреторная, моторная, эвакуаторная, резервуарная, экскреторная, всасывательная и инкреторная [1, 2, 4, 5, 7, 8, 9].
Основными анатомическими отделами желудка, отличающимися своими структурными и функциональными особенностями, являются: кардиальный отдел, дно и тело желудка, пилорический отдел. Касаясь секреторной функции желудка, следует отметить способность слизистой секретировать соляную кислоту, бикарбонаты, пепсиногены, гастрин, слизь, однако в различных отделах желудка имеются особенности секреции [7, 8, 9].
Внутренняя поверхность желудка покрыта однослойным высокопризматическим эпителием, непрерывно выделяющим мукоидный секрет, или так называемую видимую слизь, а также бикарбонаты. Барьер видимой слизи составляет 0,5-1,5 мм и обеспечивает защиту подлежащих слоев слизистой от агрессивного действия кислотно-пептического фактора [1, 2, 4, 5, 7, 8, 9].
Кардиальный отдел представляет собой узкое (шириной в 1-4 см) кольцо ниже отверстия пищевода и содержит железы, вырабатывающие мукоидный секрет, здесь же обнаружены париетальные клетки, продуцирующие HCl и внутренний фактор Кастла. Основное количество париетальных или обкладочных клеток, секретирующих НCl и внутренний фактор Кастла, представлено в дне и теле желудка, составляющих 75 % всего желудка. Кроме того, в теле и дне желудка имеются главные зимогенные клетки, вырабатывающие пепсиногены, мукозные клетки, а также аргентофинные клетки. Железы пилорического отдела, составляющего 15-20 % желудка, содержат клетки, вырабатывающие слизь. Особенностью этого отдела является наличие в нем G-клеток, продуцирующих гастрин [7, 8, 9].
В различных отделах желудка выделяют так называемые промежуточные клетки, выделяющие мукоидный секрет и бикарбонаты. Эти клетки обладают высокой митотической активностью и являются камбием для всего эпителия желудка. Главные и часть париетальных клеток не обладают митотической активностью, их восполнение обеспечивается за счет пролиферации и созревания камбиальных клеток. По всей территории желудка в глубоких слоях слизистой располагаются аргентофинные клетки, продуцирующие 5-окситриптамин (предшественник серотонина) и другие биологически активные вещества. Тучные клетки соединительной ткани продуцируют гистамин, серотонин, гепарин, фактор активации тромбоцитов (ФАТ), фактор хемотаксиса эозинофилов (ФХЭ), фактор хемотаксиса моноцитов (ФХМ) и другие цитокины [4, 5, 6].
Иннервация желудка обеспечивается экстрамуральными нервами (блуждающим, чревным, диафрагмальным) и интрамуральной нервной системой [7, 8, 9].
Парасимпатическая иннервация осуществляется блуждающими нервами, содержащими преганглионарные волокна и оканчивающимися в миэнтеральном сплетении на клетках Догеля I типа – втором нейроне парасимпатической иннервации.
Симпатическая иннервация осуществляется волокнами, идущими в составе ваго-симпатических стволов блуждающих нервов и волокон чревных нервов, достигающих желудка совместно с брыжеечными нервами [7, 8, 9].
Метасимпатическая система регуляции основных функций желудка представлена подслизистым сплетением (мейснерово), слизистым, межмышечным (ауэрбахово) и субсерозным.
В свою очередь, активность метасимпатической системы желудка находится под преимущественным регулирующим влиянием n.vagus.
Характеристика фаз желудочной секреции
Различают базальную (голодную) и стимулированную (пищеварительную) секрецию. Секреция желудочного сока натощак составляет у взрослого человека 10 % того количества, которое образуется при максимальной стимуляции. Перерезка блуждающего нерва или удаление антрального отдела, содержащего G-клетки, приводит к прекращению базальной секреции, из чего следует, что она стимулируется гастрином и зависит от тонуса блуждающего нерва [1, 2, 4, 5, 7, 8, 9].
В процессе желудочной секреции выделяют три фазы:
1) сложнорефлекторную (цефалическую);
Клетки желудочных желез ежесуточно секретируют 2-3 литра желудочного сока. По своему составу желудочный сок на 99-99,5 % состоит из воды и 1-0,5 % составляет плотный остаток, представленный неорганическими (хлориды, сульфаты, фосфаты, бикарбонат натрия, ионы калия, кальция, магния) и органическими (ферменты, мукоиды) веществами. В небольшом количестве в желудочном соке находятся азотсодержащие вещества небелковой природы (мочевина, мочевая кислота, молочная кислота) [5, 7, 8, 9].
Афферентная стимуляция цефалической фазы желудочной секреции осуществляется при участии различных анализаторов – вкусового, обонятельного, зрительного, слухового.
Эфферентное звено регуляции первой фазы желудочной секреции обеспечивается холинэргическими нервными волокнами, ацетилхолином, освобождаемым интрамуральными нервными сплетениями. Латентный период первой фазы составляет 5-10 минут. В цефалическую фазу выделяется около 45 % желудочного сока, богатого ферментами.
Основными эфферентными регуляторами сложнорефлекторной фазы являются: холинергические нервные влияния, ацетилхолин, а также гастрин, высвобождающийся при активации n. vagus [5, 7, 8, 9].
Стимуляторами желудочной фазы секреции являются механические факторы (растяжение желудка поступающей в него пищей) и химические раздражения слизистой желудка, приводящие к активации холинергических влияний и усилению продукции ацетилхолина и гастрина.
Различают гастрин 17 и гастрин 34. Гастрин 17 обладает наибольшей активностью, гастрин 34 имеет более продолжительный период существования, но в шесть раз меньшую активность. Гастрин 17 в большей мере оказывает местный стимулирующий эффект на секреторную активность желудка при участии антрофундального кровотока. Гастрин 34, всасываясь в системный кровоток, регулирует оксигенацию и трофику слизистой желудочно-кишечного тракта. Гастрин 34 синтезируется клетками 12-перстной кишки и поджелудочной железы и при триптическом гидролизе расщепляется с образованием гастрина 17, 14, 13. Гастрин 14 и гастрин 13 обнаруживаются в небольших количествах, и биологическая значимость их неясна. Стимулируют инкрецию гастрина ацетилхолин, механическое растяжение антрального отдела, продукты протеолиза, катехоламины через a-адренорецепторы, ионы кальция, магния, алкоголь, кофеин [1, 2, 4, 5, 7, 8, 9].
Третья фаза желудочной секреции – кишечная – продолжается 1-3 часа развивается при переходе пищи из желудка в кишечник. Кишечная фаза поддерживается механическим растяжением тонкого кишечника и химическим раздражением хеморецепторов слизистой 12-перстной кишки продуктами гидролиза пищи и сопровождается освобождением различных биологически активных соединений – гастрина, энтерогастрона, соматостатина, секретина, холецистокинина, гастроингибирующего пептида, мотилина, нейротензина и другие [1, 2, 4, 5, 7, 8, 9].
К числу медиаторов, играющих роль первых посредников в индукции секреции желудочного сока, относятся ацетилхолин, гистамин и гастрин.
Как известно, важнейшими компонентами желудочного сока являются НСl, пепсиногены и слизь.
НСl вырабатывается париетальными клетками, расположенными в перешейке, шейке и верхнем отделе тела железы. Эти клетки характеризуются исключительным богатством митохондрий вдоль секреторных внутриклеточных канальцев. В состоянии покоя париетальных клеток секреторные канальцы выражены слабо, вместо них имеются особые пузырчатые образования – тубуловезикулы. В периоды секреторной активности в процессе пищеварения количество секреторных канальцев увеличивается, их мембрана сливается с плазматической мембраной, увеличивая тем самым ее площадь. Кислотопродуцирующие клетки желудка активно используют собственный гликоген для нужд секреторного процесса. Секреция НСl – ярко выраженный цАМФ-зависимый процесс, активация которого протекает на фоне усиления гликогенолитической и гликолитической активности. Кислотообразующая функция обкладочных клеток характеризуется наличием в них процессов фосфорилирования-дефосфорилирования, существованием митохондриальной окислительной цепи, транспортирующей ионы водорода из матриксного пространства, а также (Н-К)-АТФазы секреторной мембраны, перекачивающей протоны из клетки в просвет железы за счет энергии АТФ. Вода поступает в канальцы клетки путем осмоса [5, 7, 8, 9].
В полости желудка НСl стимулирует секреторную активность желез желудка, способствует превращению пепсиногена в пепсин, создает оптимальное рН для действия протеолитических ферментов желудочного сока, вызывает денатурацию и набухание белков. Кроме того, HCl стимулирует продукцию секретина в двенадцатиперстной кишке, обеспечивает антибактериальное действие вместе с лизоцимом и сиаломуцинами, а также стимулирует моторную функцию желудка и регулирует работу пилорического сфинктера [7, 8, 9].
При ахлоргидрии содержание микроорганизмов в 1 мл желудочного сока возрастает до 100000 (в норме в 1 мл содержится 100 микробных клеток).
Основным ферментативным процессом в полости желудка является начальный гидролиз белков до альбумоз и пептонов с образованием небольшого количества аминокислот. В желудочном соке выделено 7 видов пепсинов, продуцируемых главными клетками.
Основными пепсинами желудочного сока являются:
Пепсин А – группа ферментов, гидролизирующих белки при рН = 1,5- 2,0. Около 1 % пепсина переходит в кровяное русло, фильтруется в почках и выделяется с мочой (уропепсин).
Гастриксин, пепсин С, желудочный катепсин. Соотношение между пепсином А и гастриксином в желудочном соке от 1:1 до 1:5. Оптимум действия фермента при рН = 3,2-3,5.
Пепсин В, парапепсин, желатиназа – разжижает желатину, расщепляет белки соединительной ткани. Оптимум действия фермента при рН до 5,6.
Ренин, пепсин Д, химозин – расщепляет казеин молока в присутствии ионов Са, с образованием параказеина и сывороточного белка.
Пепсины не продуцируются железами антрального отдела желудка, гастриксин же присутствует во всех отделах желудка.
Желудочный сок содержит ряд непротеолитических ферментов – желудочную липазу, лизоцим, муколизин, карбоангидразу, уреазу. Лизоцим вырабатывается клетками поверхностного эпителия и придает бактерицидные свойства желудочному соку.
Желудочный сок обладает небольшой амилолитической и липолитической активностью. Не исключено, что амилаза и липаза рекретируются фундальными и пилорическими железами из крови. В желудочном соке обнаружены и другие непротеолитические ферменты: трансаминазы, аминопептидазы, щелочная фосфатаза, рибонуклеазы и другие [5, 7, 8, 9].
Важнейшим протективным фактором желудка от воздействия НСl и пепсинов является слизеобразование.
Желудочная слизь, или муцин, вырабатывается клетками поверхностного цилиндрического эпителия, добавочными клетками шеек желез дна и тела, мукоидными клетками кардиальных и пилорических желез.
Желудочная слизь состоит из нерастворимой видимой и растворимой слизи. Видимая слизь – высокогидратированный гель, содержит нейтральные мукополисахариды, сиаломуцины, гликопротеиды, протеогликаны, протеины. Растворенный муцин образуется из секрета желудочных желез и продуктов переваривания видимой слизи [5, 7, 8, 9].
Адсорбционная и антипептическая способность слизи, обусловленная наличием сиаловых кислот, обеспечивает защиту слизистой от самопереваривания. Гликопротеиды, входящие в состав видимого муцина, совершенно резистентны к протеолизу. Слизь обладает значительной буферной емкостью и способностью нейтрализовать кислоту за счет наличия бикарбонатов и фосфатов, которые секретируются вместе со слизью и адсорбируются на ней. Образующийся при взаимодействии муцина и бикарбоната мукозо-бикарбонатный барьер предохраняет слизистую от аутолиза, создает такую среду, в которой большинство макромолекул нерастворимы. Такой барьер непроницаем для бактериальных олигопептидов.
Кислые мукополисахариды – протеогликаны обеспечивают липотропную активность слизи, предотвращая ожирение печени. Биологическое действие фукомуцинов (нейтральных муцинов), составляющих основную массу видимой и растворимой слизи, связано с наличием в их составе групповых антигенов крови, фактора роста и антианемического фактора Кастла.
Сиаломуцины участвуют в синтезе НCl, они способны нейтрализовать вирусы и препятствовать вирусной гемаглютинации.
Выделение слизи стимулируют умеренные концентрации катехоламинов, гистамин, гастрин, серотонин, механическое раздражение слизистой. Усиливают образование слизи простациклин, а также простагландины (РgE1, PgE2), улучшающие кровоснабжение слизистой оболочки. Простагландины F2b стабилизируют мембраны лизосом эпителия, препятствуя его десквамации, и являются мембранопротекторами. АКТГ, глюкокортикоиды подавляют слизеобразование [3, 5, 6, 9].
Характер и механизмы нервных и гормональных влияний на желудочную секрецию
Ацетилхолин стимулирует деятельность главных, обкладочных и мукозных клеток через М-холинорецепторы, а также за счет стимуляции освобождения гастрина G-клетками. Кроме того, ацетилхолин подавляет активность D-клеток и продукцию соматостатина-ингибитора желудочной секреции. В ткани желудка под действием ацетилхолина и гастрина из ECL-клеток и тучных клеток выделяется гистамин, который через Н2 – рецепторы активирует аденилатциклазу с последующей стимуляцией (Н-К)-АТФ-азы. Этот фермент обеспечивает электронейтральный обмен ионов калия на ионы водорода. В равной степени гистамин стимулирует секрецию бикарбонатов и слизи. Стимулирующим влиянием на процесс желудочной секреции обладают простагландины F 2α, высвобождающиеся под влиянием ацетилхолина [1, 2, 4, 5, 7, 8, 9].
Эффекты катехоламинов на секреторную способность желудка, по данным ряда авторов, весьма противоречивы: через β1-адренорецепторы подавляется продукция НСI; через β2-адренорецепторы подавляется продукция пепсиногена. Действуя через α-адренорецепторы, катехоламины вызывают ограничение кровотока в слизистой желудка, активацию G-клеток и усиление продукции гастрина. Последнее приводит к повышению секреторной способности желудка.
В настоящее время очевидно значение ряда гормональных и гуморальных факторов, оказывающих модулирующее влияние на секреторную функцию желудка. Гормональными факторами, стимулирующими желудочную секрецию, являются АКТГ, глюкокортикоиды, СТГ, пролактин, инсулин, глюкагон, паратгормон. К гормональным и гуморальным ингибиторам желудочной секреции относятся вазопрессин, окситоцин, тиреокальцитонин, эндогенные опиоидные пептиды, ВИП, ГИП и другие факторы [1, 2, 4, 5, 7, 8, 9].
Важную роль в регуляции желудочной секреции играют биологически активные вещества и тканевые гормоны, причем гистамин, простагландины групп В, F оказывают стимулирующее воздействие на желудочную секрецию, в то время как простагландины типа Е, А и простациклин подавляют секрецию кислоты и пепсина [5, 7, 8, 9].
Что касается серотонина – важного медиатора воспалительных реакций – он оказывает неоднозначное действие на желудочную секрецию: стимулирует действие главных клеток и подавляет активность обкладочных [1, 2, 4, 5].
Ниже представлены особенности влияния ряда гормонов и гуморальных модуляторов секреторной, моторной и эвакуаторной функции желудка.
Холецистокинин – продуцируется в G-клетках тонкой кишки под влиянием пептидов, аминокислот, жирных кислот. Холецистокинин стимулирует секрецию секрецию желудочного сока, панкреатических ферментов, инсулина, моторику желчного пузыря, кишечника и тормозит эвакуаторную активность желудка.
Мотилин – является дигестивным пептидом, продуцируется энтерохромафинными клетками тонкого кишечника (ЕС2-клетками), стимулирует секрецию пепсиногена главными клетками желудка, вызывает тоническое сокращение желудка и кишечника. Мотилин потенцирует действие ацетилхолина на пилорический отдел желудка и ускоряет эвакуацию химуса.
Секретин – продуцируется S-клетками проксимального отдела тонкого кишечника. Секретин стимулирует секрецию пепсиногена главными клетками желудка, тормозит продукцию соляной кислоты париетальными клетками. Секретин стимулирует освобождение бикарбонатов и воды поджелудочной железой, печенью, дуоденальными железами, усиливает секрецию желчи и кишечного сока, потенцирует действие холецистокинина на моторику желчного пузыря.
Важнейшим регулятором желудочной секреции является соматостатин, продуцируемый D-клетками желудочно-кишечного тракта, а также нервными клетками центральной и периферической нервной системы. Стимуляция инкреции соматостатина происходит под влиянием пептонов, кислого содержимого. Реципрокные отношения отмечены между продукцией соматостатина, гастрина, ацетилхолина.
Соматостатин ингибирует секрецию СТГ, ТТГ, пролактина, инсулина, глюкагона, а также ряда дигестивных пептидов – гастрина, холецистокинина. Снижение содержания соматостатина в слизистой оболочке антрального отдела выявлено у больных с рецидивирующей язвой двенадцатиперстной кишки [1, 2, 4, 5].
У пациентов со соматостатинпродуцирующими опухолями выявлено снижение секреторной активности желудка.
Ингибирующим влиянием на секреторную активность желудка обладают:
Гастроингибирующий пептид (ГИП) – тормозный полипептид, синтезируется в эндокриноцитах (К-клетках) тонкой кишки под влиянием липидов, снижает секрецию НСI, угнетает реабсорбцию натрия и воды в ЖКТ, стимулирует секрецию инсулина, ингибирует моторику желудка. ГИП активирует секреторную деятельность толстого кишечника. Усиление секреции ГИП выявлено при диабете 2-типа, демпинг-синдроме.
Нейротензин образуется в N-клетках слизистой оболочки подвздошной кишки, в гипоталамусе и базальных ганглиях, высвобождение нейротензина в кишечнике происходит под влиянием липидов. Нейротензин ингибирует двигательную и секреторную функцию желудка, стимулирует секрецию бикарбонатов поджелудочной железой и освобождение глюкагона.
Пептид YY синтезируется эндокриноцитами толстой и тонкой кишки, угнетает секреторную функцию желудка и поджелудочной железы, тормозный медиатор для верхних отделов пищеварительной трубки.
Энтероглюкагон – синтезируется в ЕСI-клетках слизистой оболочки кишечника, особенно подвздошной и толстой кишки; его секреция возрастает под влиянием триглицеридов и углеводов. Энтероглюкагон угнетает моторику желудка, снижает образование соляной кислоты париетальными клетками. Энтероглюкагон обладает трофическим влиянием на слизистую кишечника.
Нейропептиды могут оказывать как активирующее, так и тормозное влияние на секреторную и моторную функции желудка.
Вазоактивный интестинальный пептид (ВИП) – содержится в больших нейросекреторных гранулах типа Р. Он подавляет секрецию соляной кислоты и пепсиногена клетками желудка, активирует кровоток в стенке кишечника, секрецию кишечного сока и бикарбоната поджелудочной железой. ВИП стимулирует инкрецию инсулина, усиливает гликогенолиз в печени. ВИП обладает выраженным вазодилятаторным и гипотензивным эффектом.
Бомбезин – гастринстимулирующий полипептид – GRP, продуцируется в нервных волокнах желудочно-кишечного тракта и клетках ЦНС. Стимулирует продукцию соляной кислоты, пепсиногена, гастрина, панкреатического сока. Бомбезин способствует выделению энтероглюкагона, холецистокинина, субстанции Р, панкреатического полипептида, соматостатина.
Субстанция Р – относится к нейропептидам, выделяется нервными окончаниями интрамускулярного нервного сплетения ЖКТ, а также клетками головного и спинного мозга. Субстанция Р усиливает слюноотделение, оказывает стимулирующее действие на моторику пищеварительного тракта, участвует в передаче информации о боли с периферии в центральную нервную систему.
Энкефалины и эндорфины – эндогенные опиоидные пептиды, образуются в гипоталамических структурах, слизистой двенадцатиперстной кишки, поджелудочной железе, надпочечниках. Они оказывают тормозное влияние на секреторную и моторную функции желудка и кишечника путем блокады освобождения ацетилхолина и субстанции Р клетками этих отделов.
Нейропептид Y образуется клетками центральной и периферической нервной системы, угнетает секрецию ацетилхолина в нервных окончаниях желудочно-кишечного тракта, а следовательно, секреторную и моторную функцию ЖКТ.
Тиролиберин – образуется в гипоталамусе, аденогипофизе, клетках ЖКТ, почках, печени, плаценте, сетчатке глаза. Тиролиберин угнетает образование НСI в желудке и моторику желудка.
Источник