- От чего зависит действие химиотерапии
- Эффективность химиотерапии
- Химиопрепараты делят на две группы
- Дозы препаратов
- Когда бывает устойчивость к лечебным препаратам
- Почему химиотерапия не помогает на 3-4 стадии
- Рецидив рака
- Токсичность красной химиотерапии
- Иммуномодуляторы
- Для чего назначаются иммуномодуляторы?
- Суть паллиативной химиотерапии
- Отрицательная динамика после химиотерапии что это значит
- Что значит «отрицательная динамика»?
- Что считается отрицательной динамикой в онкологии?
- Причины отрицательной динамики
- Тактика лечения и прогнозы
От чего зависит действие химиотерапии
Часто действие химиотерапии направлено на уменьшение размера новообразования для последующего хирургического удаления опухоли. Если после хирургического вмешательства остались раковые клетки, есть вероятность, что болезнь вернется. Многое зависит от профессионализма хирурга, но вычистить все раковые клетки бывает просто невозможно.
Эффективность химиотерапии
Важно! Если действие химиотерапии через несколько курсов не дало положительных результатов, ищите другие методы, не теряйте времени, цена промедления может стоить жизни, обращайтесь к экспериментальным методам терапии.
Не стоит думать, что химиотерапия — это панацея от онкологии в общем. К сожалению, современная медицина не способна бороться со всеми видами злокачественных новообразований, и поэтому медикаментозное лечение может применяться, как способ сдерживать, контролировать и облегчать симптомы болезни.
Причины, по которым химиотерапия не дает положительных результатов:
1. Приобретенная толерантность к применяемым лекарственным средствам.
2. Врожденная устойчивость к препаратам.
Действие химиотерапии распространяется на 99% больных клеток, в то время как 1% никак не отреагирует на лечение, и продолжает свое размножение и рост.
Химиопрепараты делят на две группы
Цитостатики. Не дают раковым клеткам размножаться, препятствуют их делению. При онкологии очень важен апоптоз злокачественных новообразований, регулируемая программа клеточной гибели. Дата смерти каждой клетки предопределена, но важно вовремя остановить ее размножение.
Цитотоксики. Это яды растений или искусственно созданных форм, которые, попадая в организм пациента, нарушают целостность оболочки раковой клетки. Цитотоксики полностью убивают очаг злокачественного образования, не допуская его восстановления.
Дозы препаратов
Любые действия химиотерапии влияют на человеческий организм разрушающе, и поэтому, выбирая дозировку, специалист должен рассчитать ее так, чтобы она давала максимально терапевтический эффект, но при этом не убивала больного. В маленьких дозах прием цитостатиков и цитотоксиков бесполезен, так как они не могут остановить деление и размножение раковых клеток. Большие дозировки – опасны, они могут стать причиной необратимых последствий и привести к летальному исходу.
Чтобы не совершить ошибку в назначении препаратов, онкологи используют личный опыт, протоколы и наблюдения за тем, как развивается заболевание. Терапия при раке основывается на прекращении роста опухоли и остановке передвижения болезнетворных клеток по организму. Химиотерапия заключается в применении выбранных медикаментов для того, чтобы выполнить эти две задачи.
Когда бывает устойчивость к лечебным препаратам
Раковые клетки, которые не поддаются назначенной терапии, являются большим препятствием для всего лечения, в связи с чем их интенсивно изучают и ищут методы уничтожения. Толерантность к препаратам развивается на фоне биохимических процессов, способных преодолевать ущерб, который могут нанести медикаменты. Чтобы снизить устойчивость назначаются более высокие дозы химиопрепаратов. Правда, это может привести к новой проблеме – разрушение здоровых клеток, в зону риска входит костный мозг, ответственный за процесс кроветворения. Большие дозировки рекомендованы только в тех случаях, когда можно пересадить костный мозг или стволовые клетки. Чем крупнее новообразование, тем устойчивее оно к химиотерапии.
Почему химиотерапия не помогает на 3-4 стадии
Концентрация химических веществ в организме пациента снижается примерно через месяц после химиотерапии. В это время активизируются оставшиеся в живых раковые клетки. Если замечается привыкание злокачественных опухолей к действующим препаратам, врач должен поменять схему терапии. Правда, есть опасность, что через некоторое время раковые очаги снова приобретут устойчивость и начнут расти.
Рецидив рака
Появление рецидива зависит от формы онкологии. Он появляется сразу же после окончания лечения или через длительный период, который занимает не один год. Если после хирургического вмешательства или лучевой терапии остались клетки рака, весь злокачественный процесс начинается сначала.
Токсичность красной химиотерапии
Красный состав более токсичен по сравнению с другими расцветками, связанно это с составом препарата, в котором присутствуют цитотоксины, цитостатики в более концентрированном, ядовитом виде.
Активные действующие вещества вводятся больным в форме раствора, который окрашивается в следующие цвета:
— желтый;
— белый;
— синий;
— красный.
Именно красный раствор является причиной самых тяжелых последствий после лечения. Его применяют для уничтожения быстро растущих, агрессивных злокачественных новообразований. К основным недостаткам химиотерапии относят ее вред для здоровых тканей. Химиопрепараты разрушают группы клеток костного мозга, слизистой оболочки рта, дыхательной системы и ЖКТ.
Иммуномодуляторы
Действия химиотерапии уничтожают все клетки, которым свойственно быстрое деление, это могут быть не только раковые образования, но и эритроциты, тромбоциты, лейкоциты.
Такое негативное влияние на тельца крови может вызвать:
— снижение иммунитета;
— анемию;
— кислородное голодание органов и тканей;
— увеличение времени коагуляции.
Недостаток лейкоцитов может способствовать нарушению работы иммунной системы, что негативно сказывается на защитных функциях организма.
В комплексе с химиопрепаратами назначаются иммуномодуляторы, чтобы снизить угнетение и разрушение иммунной системы.
Для чего назначаются иммуномодуляторы?
Иммуномодуляторы назначаются на разных стадиях лечения, так как они помогают иммунитету обезопасить здоровые ткани. Без такой терапии многие больные не смогли бы пережить целый спектр побочных действий.
Иммуномодуляторы назначаются в следующих целях:
— устранение побочной симптоматики после химиотерапии;
— восстановление иммунитета после удаления опухоли хирургическим путем;
— компенсирование влияния иммунодепрессантов при комплексной или радиотерапии;
— профилактика появления новых раковых клеток и метастаз.
Суть паллиативной химиотерапии
При невозможности избавить пациента от онкологии, врачи делают все, чтобы облегчить симптоматику и самочувствие больного. Паллиативная помощь проводится для:
— снижения болевых ощущений разной интенсивности;
— улучшения функций метаболизма, дыхания, кровотока, питания;
— поддержания работы жизненно важных органов тела;
— повышения работоспособности сосудов мозга и сердечно-сосудистой системы.
Паллиативная химиотерапия замедляет миграцию раковых клеток и способствует контролю их роста при невозможности полного уничтожения злокачественного новообразования. Смерть больного может наступить, если организм больше не в силах компенсировать полученный ущерб и ресурсы восстановления тканей окончились или раковые клетки проникли в жизненно важные органы, а также в следствие интоксикации организма.
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Источник
Отрицательная динамика после химиотерапии что это значит
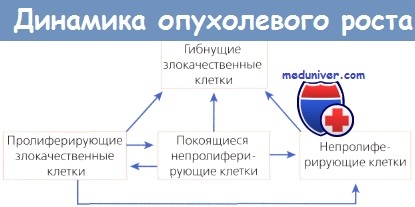
Время удвоения размера опухоли зависит от скорости как деления клеток, так и их гибели. Время генерации нельзя считать продолжительным просто из-за того, что опухоль медленно растет. Возможно, медленный рост опухоли обусловлен коротким временем генерации в сочетании с высоким показателем клеточной гибели.
Небольшая опухоль, обнаруженная с помощью рентгенологического или физикального исследования, необязательно представляет собой раннюю стадию развития опухоли, поэтому необходимо провести серию исследований, чтобы оценить скорость роста, что поможет установить стадию заболевания. Крупные опухоли (диаметр более 2—3 см) увеличиваются гораздо медленнее, чем маленькие, т. к. их клетки, особенно те, которые находятся в самом центре (дальше всего от кровоснабжения), имеют длительное время генерации. Конкуренция за питательные и другие вещества снижает активность всей массы опухоли.
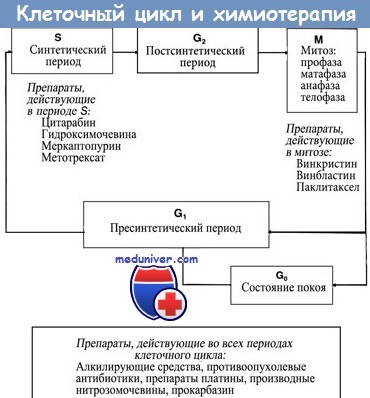
Для успешной химиотерапии (XT) злокачественных новообразований необходимо использовать физиологическое ограничение, чтобы дифференцированно уничтожать опухолевые клетки, но максимально сохранять нормальные. Для создания терапевтических режимов может быть использован тот факт, что скорость клеточного роста опухолевых клеток больше по сравнению с нормальными тканями. В любой момент времени сравнительно большое количество раковых клеток будет находиться в фазе синтеза ДНК (S-фаза) клеточного цикла, в течение которого фазоспецифические препараты (те, которые ингибируют синтез ДНК) могут действовать.
Таким образом, краткосрочная высокодозная химиотерапия (ХТ) с помощью препаратов, влияющих на синтез ДНК, таких как метотрексат, более эффективно уничтожают быстроделящиеся опухолевые клетки, при этом сохраняется сравнительно большое число нормальных элементов костного мозга. Ксожалению, клетки костного мозга, эпителия ЖКТ и волосяные фолликулы имеют время генерации, сравнимое с таковым опухолей, поэтому они чувствительны к веществам, которые ингибируют синтез ДНК.
Однако по сравнению с более синхронно растущей клеточной популяцией опухоли в конкретный момент времени лишь немногие клетки костного мозга находятся в S-фазе, что объясняет избирательную токсичность фазоспецифических препаратов. Курс терапии, длящийся несколько дней или даже недель, необходим, чтобы уничтожить медленнорастущие опухоли, в которых небольшая часть клеток находится на стадии синтеза ДНК в конкретный момент времени. Препараты, действие которых не зависит от синтеза ДНК (т. е. фазонеспецифические препараты), такие как алкилирующие средства, более эффективны в отношении крупных медленнорастущих опухолей.
Клетки, оставшиеся после лечения, имеют тенденцию к более быстрому делению и более восприимчивы к действию фазоспецифических препаратов. Таким образом, химиопрепараты гибко взаимодействуют друг с другом.
Появление повышенной чувствительности опухолевых клеток при возвращении к норме после воздействия на них алкилирующих средств служит обоснованием для сочетания фазонеспецифических и фазоспецифических препаратов во многих новых схемах XT. Кроме того, если препараты с различными механизмами токсичности комбинируются, безопасно применять дозы препаратов, используемые в ионотерапии.
Каждый выбранный препарат для сочетанной терапии должен также обладать противоопухолевой активностью и в монотерапии. Когда возможно, чередующиеся курсы химиотерапии (XT) должны способствовать восстановлению численности нормальных клеток, если в ходе лечения их количество уменьшилось. В случаях, когда известны антидоты к химиотерапевтическим препаратам, например лейковорин (цитроворум-фактор, кальция фолинат) для метотрексата, их можно использовать, чтобы ускорить восстановление нормальных клеток.
Конечно, существует опасность восстановления сублетально поврежденных опухолевых клеток, которую необходимо оценить в каждом новом режиме лечения. Хотя необходимы тщательные исследования, чтобы сравнить каждую новую комбинацию с монотерапией, в настоящее время наблюдается тенденция к использованию комбинаций препаратов, применяемых одновременно или последовательно.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Что значит «отрицательная динамика»?
Отрицательная динамика при злокачественных новообразованиях беспокоит не только пациента, но и лечащего врача. Такая ситуация может быть связана с множеством факторов, начиная от индивидуальных особенностей организма пациента и заканчивая выбором тактики лечения. Рассмотрим основные причины прогрессирования заболевания, и как можно минимизировать эти риски.
Что считается отрицательной динамикой в онкологии?
Под отрицательной динамикой понимают все случаи, когда состояние пациента ухудшается, как правило, это означает, что злокачественное новообразование продолжает расти:
- увеличение первичного очага (самой опухоли) в размерах;
- врастание в близлежащие анатомические структуры (органы, сосуды);
- появление регионарных или отдаленных метастазов (в лимфатических узлах или других органах).
Отрицательная динамика всегда определяется по результатам лабораторно-инструментальных исследований. Общее самочувствие пациента и клиническая картина заболевания здесь играют второстепенную роль, хотя тоже могут учитываться.
Безусловно, важна любая жалоба или появившийся симптом. Они требуют внимания врача, выяснения причины и быстрого устранения. Но состояние пациента со злокачественным новообразованием зависит не только от распространенности опухолевого процесса, но и от проводимого лечения, возраста и сопутствующих заболеваний. Например, плохое самочувствие обычно связано не с ростом опухоли на фоне лечения, а вызвано проводимой химиотерапией.
Поэтому основной метод контроля эффективности противоопухолевого лечения — это обследование в строго установленные сроки. Объем диагностических исследований и их периодичность зависят от характеристик опухолевого процесса (локализация, распространенность, проводимое лечение).
Причины отрицательной динамики
Все причины условно можно разделить на 2 большие группы. Первая — отказ пациента от противоопухолевой терапии. Здесь стоит отметить, что речь идет о вариантах лечения, имеющих доказанную эффективность: хирургическое вмешательство, химио- и лучевая терапия и другие. Самолечение различными народными средствами и другими способами — это не противоопухолевая терапия. Поэтому в такой ситуации рост опухоли можно считать закономерным последствием безответственного отношения к своему здоровью.
Второй вариант развития событий — пациент получает противоопухолевое лечение, но несмотря на это, отмечается отрицательная динамика. В этом случае рост опухоли может быть связан со следующими факторами:
- неадекватностью проводимого лечения — выбранный метод терапии не соответствует распространенности и стадии процесса, например, объем операции не обеспечивает радикального удаления опухоли, или новообразование нечувствительно к выбранной схеме химиотерапии;
- поздним обращением за медицинской помощью — запущенные формы злокачественных новообразований хуже поддаются лечению;
- агрессивностью самой опухоли — сейчас многие пациенты знают о том, что новообразования бывают разной степени злокачественности; например, низкодифференциированные («незрелые») опухоли более агрессивны, чем высокодифференцированные («зрелые»);
- с тактическими ошибками в лечении — например, несоблюдение правил абластики и антибластики при хирургических вмешательствах, необоснованное уменьшение суммарных доз химио- или лучевой терапии и др.
Отдельно рассматриваются индивидуальные особенности организма пациента. Сюда относится и противоопухолевый клеточный иммунитет, пол, возраст, наличие хронических заболеваний и другие факторы. Особое место в успешном лечении играет комплаентность — приверженность пациента к лечению и соблюдению всех рекомендаций лечащего врача.
Несмотря на современное развитие диагностики, позднее выявление опухолей и несвоевременное обращение за медицинской помощью — это основные причины прогрессирования заболевания, рецидивов и метастазирования. Именно степень распространенности злокачественного процесса во многом определяет успешность проводимого лечения. Чем раньше диагностирована опухоль, тем больше вероятность излечения пациента.
Тактика лечения и прогнозы
Если говорить о тактике лечения, то стоит всегда рассматривать каждый отдельный случай. После полного обследования и выявления факта прогрессирования, для пациента определяется вариант радикального лечения, если это возможно. При этом общие принципы противоопухолевой терапии схожи с первичным лечением.
Например, при прогрессировании заболевания после резекции (удаления части органа) может проводиться полное удаление органа с последующей лучевой или химиотерапией. При этом схемы и режимы химио- или лучевой терапии подбирают особенно тщательно. Врачи учитывают сроки прогрессирования опухоли, эффект от проводимого ранее лечения и другие факторы.
Если отрицательная динамика сопровождается появлением отдаленных метастазов, то лечение, как правило, сводится к паллиативному и симптоматическому. Иногда рассматривается вопрос о лечении метастатических форм рака. Например, при единичных метастазах в головном мозге, возможно их хирургическое удаление при условии анатомической доступности или же проведение лучевой терапии.
Прогнозы зависят от множества факторов и не могут быть определены заранее. Здесь учитываются морфологические особенности опухоли, распространенность процесса, эффективность проводимого лечения и индивидуальные особенности пациента.
Источник