- Мутация EGFR – это хорошо или плохо?
- Мутации гена EGFR
- Роль рецептора EGFR и мутаций гена EGFR в патогенезе немелкоклеточного рака легкого
- Что такое EGFR?
- Зачем определять статус мутации гена EGFR?
- Какие биоматериалы могут быть отправлены на EGFR-тестирование?
- О Программе тестирования мутаций гена EGFR у пациентов с немелкоклеточным раком легкого
- Каким пациентам необходимо молекулярно-генетическое тестирование на наличие мутации гена EGFR?
Мутация EGFR – это хорошо или плохо?
Когда в 1962 году американский ученый обнаружил в экстракте слюнной железы мышей сложное вещество, эпидермальный фактор роста (EGF), состоящий из более чем пяти десятков аминокислот, он и не представлял, что сделал первый шаг к большому открытию, которому будет суждено изменить представление о раке легкого. Но лишь в начале XXI века станет достоверно известно, что мутации рецептора, с которым связывается EGF, могут становиться отправной точкой в развитии одной из самых агрессивных опухолей – рака легкого.
Что такое эпидермальный фактор роста?
Следует отметить, что EGF – белок, необходимый нашему организму. Так, находящийся в слюнных железах эпидермальный фактор роста обеспечивает нормальный рост эпителия пищевода и желудка. Кроме того, EGF содержится в плазме крови, моче, молоке.
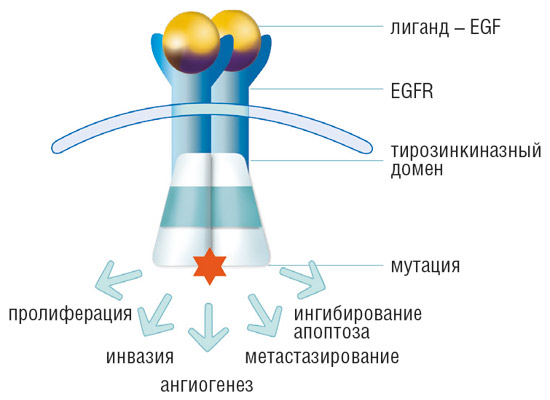
Свою работу EGF выполняет, связываясь с рецептором эпидермального фактора роста, EGFR, расположенным на поверхности клеток. Это приводит к активации ферментов тирозинкиназ, которые и передают сигнал о необходимости активной деятельности. В результате происходят несколько последовательных процессов, в том числе увеличение скорости выработки белков и синтез молекулы, которая обеспечивает хранение и реализацию программы развития живых организмов, ДНК. Итогом этого и становится деление клеток.
В 90-х годах прошлого века стала очевидна роль рецептора эпидермального фактора роста как онкогена, играющего одну из ведущих ролей в развитии ряда злокачественных заболеваний.
Эпидермальный фактор роста и рак
В конце XX века было проведено несколько исследований, подтверждающих значение EGF в развитии злокачественных заболеваний. В 1990 году американские ученые доказали, что блокирование связывания эпидермального фактора роста с рецепторами и, как следствие, предотвращение активации фермента тирозинкиназы останавливает рост злокачественных клеток [1].
Конечно, далеко не у всех и не всегда эпидермальный фактор роста «запускает» процессы ненормируемого деления клеток. Чтобы нормальный белок, необходимый для жизнедеятельности нашего организма, вдруг стал его злейшим врагом, в молекуле рецептора эпидермального фактора роста должны произойти генетические изменения, или мутации, которые приводят к многократному увеличению числа рецепторов EGF – их гиперэкспрессии.
Причиной мутаций могут быть потенциально агрессивные факторы окружающей среды, например, токсины, а также курение, поступление канцерогенных веществ с пищей. В некоторых случаях «поломки» в рецепторе эпидермального фактора роста накапливаются на протяжении нескольких поколений, передаваясь от родителей детям. Тогда говорят о наследственных мутациях.
Следует отметить, что «поломки» в молекуле рецептора эпидермального фактора роста связаны с несколькими видами рака. Прежде всего, это немелкоклеточный рак легкого (НМРЛ). Гораздо реже мутации и, как следствие, гиперэкспрессия EGFR приводят к развитию опухолей шеи, головного мозга, толстой кишки, яичника, шейки матки, мочевого пузыря, почки, молочной железы, эндометрия.
Есть ли у вас мутация эпидермального фактора роста?
У некоторых категорий больных вероятность «поломки» значительно повышена. Так, известно, что мутация рецептора эпидермального фактора роста гораздо чаще происходит у людей, которые никогда не курили. Это вовсе не означает, что приверженцы табакокурения реже болеют раком легкого – напротив, известно, что вредная привычка становится причиной развития заболевания в 90% случаев. Просто у курильщиков рак легкого развивается по другому механизму.
Показательные результаты, отражающие распределение мутаций эпидермального фактора роста среди россиян, были получены в одном крупном отечественном исследовании, в котором были изучены данные более 10 тысяч больных раком легкого [2]. Они показали, что мутации EGFR обнаруживались:
- У 20,2% больных аденокарциномой, 4,2% больных плоскоклеточным раком и 6,7% больных крупноклеточной карциномой легкого
- У 38,2% некурящих женщин и только у 15,5% некурящих мужчин
- У 22% курящих женщин и 6,2% курящих мужчин
Кроме того, в исследовании было выявлено, что вероятность появления «поломки» в рецепторе эпидермального фактора роста увеличивается у больных аденокарциномой с возрастом, вырастая от 3,7% в 18-30 лет до 18,5% в 81-100 лет.
Результаты зарубежного исследования, в котором участвовали более 2000 больных аденокарциномой легкого [3], показали, что мутация EGFR была выявлена:
- У 15% больных, которые курили в прошлом
- 6% больных, куривших в настоящем
- 52% больных, которые никогда не курили
Эти данные подтверждают: мутации рецептора эпидермального фактора роста могут быть обнаружены и у тех, кто не представляет жизни без сигареты, просто гораздо реже, чем у приверженцев здорового образа жизни.
Несмотря на вполне однозначную тенденцию распространения «драйвер-мутации» EGFR, точный ответ на вопрос, есть ли эта «поломка» у вас, можно получить только по результатам молекулярно-генетического тестирования, которое проводят всем больным раком легкого.
Если у вас обнаружена мутация EGFR
Еще каких-то десять лет назад у половины больных раком легкого было гораздо меньше шансов успешно бороться с опухолью. Однако сегодня стали доступны препараты, которые позволили в корне изменить эту ситуацию. Речь идет о таргетной терапии, которая стала доступной в последнее десятилетие.
Наличие мутации эпидермального фактора роста, подтвержденное результатами молекулярно-генетического исследования, предоставляет онкологам возможность ввести в схему лечения таргетные препараты. Создание таргетных лекарственных средств для лечения рака легкого стало прорывом в современной онкологии.
Таргетные препараты действуют на первопричину злокачественного заболевания, влияя на сам механизм, запускающий неограниченный клеточный рост и деление. Они блокируют фермент тирозинкиназу, которая передает сигнал к «началу боевых действий» и, собственно, активирует процессы размножения и роста клеток.
Таргетная терапия рака позволяет значительно отдалить его прогрессирование, в том числе и по сравнению со стандартной химиотерапией. Это – значимое преимущество таргетных лекарств.
Способность таргетных препаратов (ингибиторов тирозинкиназы EGFR) продлевать время до прогрессирования опухоли была доказана в крупном анализе, изучающем результаты 23 исследований, в которых участвовало более 14 тысяч больных немелкоклеточным раком легкого с мутацией рецептора эпидермального фактора роста [6].
Важно отметить, что при наличии мутации EGFR лечение рака, как правило, не исчерпывается только таргетными препаратами. Вы должны быть готовым к сложной, длительной и комплексной терапии, в том числе оперативному вмешательству, лучевой терапии и др.
Если у вас не обнаружена мутация EGFR
Отрицательный результат молекулярно-генетического анализа на мутацию EGFR еще не говорит о том, что таргетная терапия вам не поможет. Прежде всего, важно выяснить, обнаружены ли в вашей опухоли какие-либо другие «поломки». Хотя мутация рецептора эпидермального фактора роста является самой распространенной среди больных раком легкого, не исключена вероятность и других, более редких «ошибок».
В современных протоколах, на которые опираются онкологи при подборе индивидуальной схемы лечения НМРЛ, настоятельно рекомендуют проводить развернутый молекулярно-генетический анализ для выявления не только самых распространенных «драйвер-мутаций», но и редких «поломок». Современный выбор таргетных препаратов позволяет подобрать «целевое» лекарство для большинства известных мутаций при раке легкого.
Если же в образце вашей опухоли не было обнаружено ни одной генетической «ошибки», таргетная терапия вам действительно не показана. Препараты, которые созданы для того, чтобы попадать «в яблочко», бесцельно не принимают, поскольку они просто не будут работать. Но у онкологов есть и другие терапевтические возможности, которые в вашем случае будут эффективны: это химиотерапия и, возможно, иммунотерапия. И все же вы должны помнить – индивидуальную схему лечения будет определять ваш лечащий врач, опираясь на данные о гистологическом типе вашей опухоли, стадии заболевания и др.
- Divgi C.R., et al. Phase I and Imaging Trial of Indium 111-Labeled Anti-Epidermal Growth Factor Receptor Monoclonal Antibody 225 in Patients With Squamous Cell Lung Carcinoma. JNCI J. Natl. Cancer Inst. Oxford University Press, 1991. Vol.83, №2, P. 97-104.
- Imyanitov E.N., et al. Distribution of EGFR Mutations in 10,607 Russian Patients with Lung Cancer. Mol. Diagn. Ther. Springer International Publishing, 2016. Vol.20, №4, P. 40-406.
- D’Angelo S.P., et al. Incidence of EGFR exon 19 deletions and L858R in tumor specimens from men and cigarette smokers with lung adenocarcinomas. J. Clin. Oncol. American Society of Clinical Oncology , 2011. Vol.29, №15, P. 2066-2070.
- Sharma S.V., et al. Epidermal growth factor receptor mutations in lung cancer. Nat. Rev. Cancer. 2007. Vol.7, №3, P. 169-181.
- Lynch T.J., et al. Activating Mutations in the Epidermal Growth Factor Receptor Underlying Responsiveness of Non-Small-Cell Lung Cancer to Gefitinib. N. Engl. J. Med. Massachusetts Medical Society, 2004. Vol.350, №21, P. 2129-2139.
- Lee C.K., et al. Impact of EGFR Inhibitor in Non-Small Cell Lung Cancer on Progression-Free and Overall Survival: A Meta-Analysis. JNCI J. Natl. Cancer Inst. Oxford University Press, 2013. Vol.105, №9, P. 595-605.
Copyright © 2008 | | E-mail: | Конфиденциальность 

При копировании материалов
ссылка на сайт обязательна.
Источник
Мутации гена EGFR
Роль рецептора EGFR и мутаций гена EGFR в патогенезе немелкоклеточного рака легкого
Многочисленные биологические исследования выявили повышенную активность рецептора EGFR и каскада, запускающегося при активации этого рецептора, у больных немелкоклеточным раком легкого.
Что такое EGFR?
- EGFR – трансмембранный рецептор, активирующийся при связывании с эпидермальным фактором роста, трансформирующим фактором роста-α, амфирегулином.
- При активации EGFR внутри клетки запускается каскад биохимических реакций, приводящих к повышению пролиферации малигнизированных (опухолевых) клеток, росту опухоли, стимуляции процессов инвазии, патологического ангиогенеза и метастазирования.
- Рецептор EGFR кодируется геном EGFR.
В ряде опухолей обнаруживаются аномальные рецепторы эпидермального фактора роста, что обусловлено наличием мутации в соответствующем гене. В клетках с мутацией происходит активация сигнального пути EGFR, что, в свою очередь, инициирует процессы злокачественной трансформации в большинстве опухолей. Сигнальные пути контролируют процессы пролиферации, апоптоза – одного из механизмов клеточной гибели, утраты способности клеток к дифференцировке, процессы ангиогенеза и метастазирования.
Зачем определять статус мутации гена EGFR?
Тест на мутацию гена EGFR предназначен для отбора больных местно-распространенным или метастатическим немелкоклеточным раком легкого на терапию низкомолекулярными ингибиторами EGFR (ингибиторами тирозинкиназы).
Наличие мутаций гена EGFR позволяет выделить группу пациентов с наибольшей вероятностью выраженного ответа на терапию ингибиторами тирозинкиназы (гефитиниб).
Известны активирующие мутации гена EGFR, связанные с чувствительностью либо устойчивостью к ингибиторам тирозинкиназы. Подавляющее большинство мутаций, связанных с чувствительностью (
90%), – это делеции в 19 экзоне (Del19) или замена L858R в 21 экзоне. Опухоли с мутациями Del19 или L858R наиболее чувствительны к терапии ингибиторами тирозинкиназы EGFR. Прочие мутации, связанные с чувствительностью (G719X, L861Q, S768I и некоторые другие), составляют в сумме
5% мутантных случаев.
Инсерции 20 экзона связаны с устойчивостью к ингибиторам тирозинкиназы и составляют
3% опухолей с мутациями. Еще одна мутация, связанная с устойчивостью, – T790M. Частота выявления этой мутации после проведения химиотерапии ингибиторами тирозинкиназы составляет примерно 50%, однако в 1-3% случаев мутация может возникать de novo. Мутация T790M в гене EGFR является наиболее частой причиной возникновения резистентности к проводимой таргетной терапии. Своевременное выявление этой мутации позволяет выяснить причину резистентности и принять решение о смене терапии у пациента. Поэтому для назначения эффективной таргетной терапии всем больным немелкоклеточным раком легкого необходим анализ как на наличие мутаций чувствительности, так и на наличие/отсутствие мутаций устойчивости к ингибиторам тирозинкиназы.
Определение статуса мутации гена EGFR и персонализированный подход к выбору терапии, основанный на результатах молекулярно-генетического тестирования, позволят сделать лечение немелкоклеточного рака легкого более эффективным и приблизиться к международным тенденциям клинической практики.
Какие биоматериалы могут быть отправлены на EGFR-тестирование?
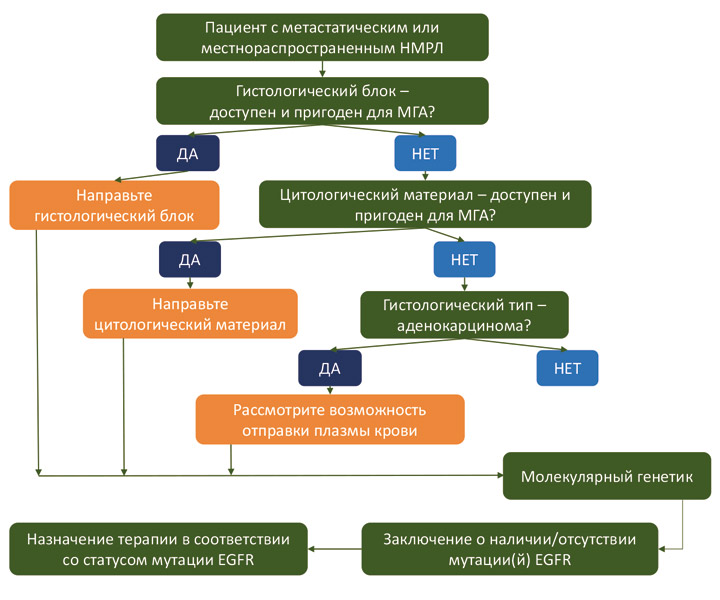
Анализ можно выполнить с использованием гистологического материала, цитологического материала или образца плазмы крови. Предпочтительна отправка гистологического материала, так как именно в этом случае достигается максимальная чувствительность анализа. Результативность тестирования по цитологическому материалу сопоставима с результатами, полученными для гистологических блоков. Если у пациента есть цитологический материал, то (в отсутствие гистологического) он представляет собой приемлемую альтернативу для EGFR-тестирования. В случаях, когда у пациента с аденокарциномой легкого отсутствует материал опухоли, следует рассмотреть возможность отправки плазмы крови на EGFR-тест. Несмотря на относительно низкую чувствительность и высокую трудоемкость анализа по плазме крови, он может быть единственной опцией для пациентов, чей опухолевый материал (гистологический или цитологический) утрачен или полностью израсходован на другие исследования.
Алгоритм выбора биоматериала для выполнения EGFR-тестирования приведен на схеме ниже:
Видеоинструкция по получению плазмы крови для EGFR-тестирования:
О Программе тестирования мутаций гена EGFR у пациентов с немелкоклеточным раком легкого
- Тестирование в рамках Программы проводится на всей территории страны.
- Отправка материала и тестирование проводится бесплатно для врачей и пациентов.
Каким пациентам необходимо молекулярно-генетическое тестирование на наличие мутации гена EGFR?
Пациентам с распространенным (местно-распространенным или метастатическим) немелкоклеточным раком лёгкого (в частности: аденокарцинома легкого, крупноклеточный рак, плоскоклеточный и аденоплоскоклеточный рак и др.).
Благодарим ООО «АстраЗенека Фармасьютикалз» за спонсорскую поддержку тестирования.
- Reck M, Clint L. Lung Cancer. 2009 Jan; 63(1): 1-9.
- Lynch T, Bell DW. Sordella Retal. N Engl J Med. 2004 May 20; 350(21): 2129-3.
- Herbst RS, Hyemach JV, Lippman SM. N Engl J Med. 2008 Sep 25; 359(13): 1367-80.
- Gazdar AF, Shigematsu H, Herz J, Minna JD. Trends Mol Med. 2004 Oct; 10(10): 481-6.
- Mok T, et al. N Engl J Med 2009; 361: 947-957.
- Han J, et al. J Clin Oncol 2012; 30: 1122-1228.
- Maemondo M, et al. N Engl J Med 2010; 362: 2380-2388.
- Mitsudomi T, et al. Lancet Oncol 2010; 11: 121-128.
- Zhou C et al. Lancet Oncol 2011; 12: 735-742.
- Rosell R, et al. Lancet Oncol 2012; 13: 239-246.
- Gridelli C, et al. J Clinical Oncol 2012; 30: 3002-3011.
- Wu Y, et al. Lancet Oncol 2014; 15: 213-222.
- Sequist L, et al. J Clin Oncol 2013; 31: 3327-3334.
- Haratani K, Hayashi H, Tanaka T, et al. Ann Oncol 2017; 28(7): 1532-1539.
Войти
в базу данных
Для того, чтобы отправить материал на диагностику, вы должны быть зарегистрированным пользователем. Если у вас уже есть логин и пароль, то повторная регистрация не требуется.
Если вы новый пользователь, пожалуйста, пройдите процедуру регистрации.
Источник