- АРТЕРИО-ВЕНОЗНЫЕ МАЛЬФОРМАЦИИ
- Общие сведения
- Показания и выбор метода лечения
- Принципы микрохирургического удаления АВМ
- Эндоваскулярное лечение АВМ головного мозга
- Лучевое лечение АВМ головного мозга
- Заключение
- Артериовенозные мальформации сосудов головного мозга: лечение, операции и последствия
- Статистика заболеваемости и последствий патологии
- В какой части головы локализируются АВМ головного мозга?
- Причины развития артериовенозного порока и симптомы
- Виды церебральных мальформаций венозно-артериального русла
- Методы лечения мальформаций сосудов головного мозга
- Где лучше оперироваться и цены операции
АРТЕРИО-ВЕНОЗНЫЕ МАЛЬФОРМАЦИИ

Общие сведения
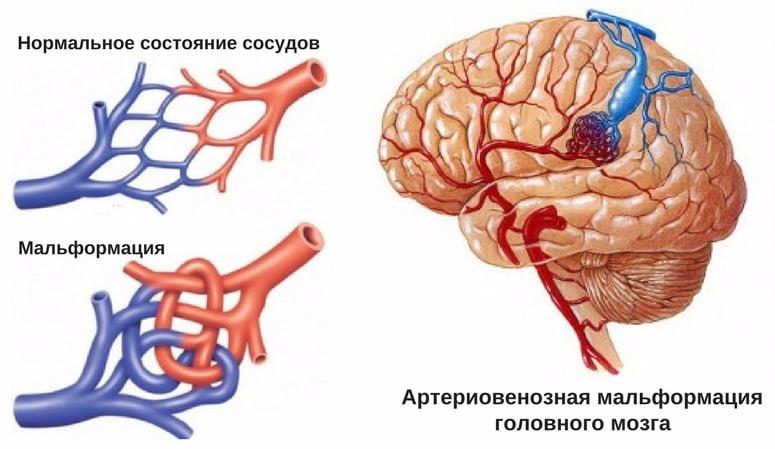
Схематическое изображение АВМ
Артерио-венозная мальформация (АВМ) — врожденный порок развития сосудов, представляющий собой конгломерат артерий и вен, лишенных промежуточного капиллярного звена. АВМ могут манифестировать кровоизлияниями, проявляющимися соответствующей симптоматикой и/или эпилептическими приступами. У большинства больных заболевание проявляется в возрасте 20–40 лет, пик кровоизлияний приходится на возраст 15–20 лет. Кровоизлияние из АВМ часто приводит к стойкой инвалидизации (до 50% случаев) и не редко летально (до 10% случаев). Риск кровоизлияния из неразорвавшейся АВМ составляет 2–4% в год, риск повторного кровоизлияния: 6-18%.
Показания и выбор метода лечения
К настоящему моменту используются три метода лечения АВМ: прямое микрохирургическое удаление, эндоваскулярная эмболизация и лучевое лечение. Показания к использованию каждого из методов в достаточной степени отработаны. В ряде случаев используется комбинация методик. Для определения возможности прямого микрохирургического иссечения мальформации используется классификация Spetzler-Martin, в которой учитывается размер АВМ, ее локализация по отношению к функционально важным зонам мозга и особенности дренирования крови.
| Классификация АВМ Spetzler-Martin | |
| Оцениваемый признак | Баллы |
 |
| Иссечение АВМ после эмболизации композицией Onyx |
Лучевое лечение АВМ головного мозга
Leksell Gamma Knife
Лучевая терапия (гамма-нож, облучение протонным пучком) наиболее эффективна при маленьких компактных мальформациях диаметром не более 3 см. Так, при мальформациях менее 1 см в диаметре полной облитерации можно достичь почти в 90 % случаев, а при мальформациях диаметром более 3 см лишь — до 30%. Отрицательной стороной лучевой терапии АВМ является то, что облитерация сосудов АВМ наступает спустя 1–3 года после лечения. Как показали недавние исследования, предварительная эмболизация АВМ снижает эффективность радиохирургии. По данным НИИ нейрохирургии после стереотаксического облучения полной облитерации удается достичь в более чем 70% случаев. У 10% больных наблюдается уменьшение размеров АВМ и редукция кровотока.
Заключение
Оптимальным методом лечения АВМ следует считать мультимодальный подход с использованием комбинаций всех методов. Микрохирургическое иссечение в настоящее время остается основным радикальным методом лечения АВМ головного мозга. Благодаря дифференцированному подходу по отбору пациентов в большинстве случаев удается достичь благоприятных результатов. Эмболизация имеет существенное значение в структуре комбинированных методов лечения. Метод высокоэффективен при лечении фистульных АВМ и АВМ вены Галена мурального типа. Лучевая терапия — метод выбора при распространенных и неоперабельных АВМ, а также при частичном иссечении или неполной облитерации АВМ после ее эндоваскулярной эмболизации.
Источник
Артериовенозные мальформации сосудов головного мозга: лечение, операции и последствия
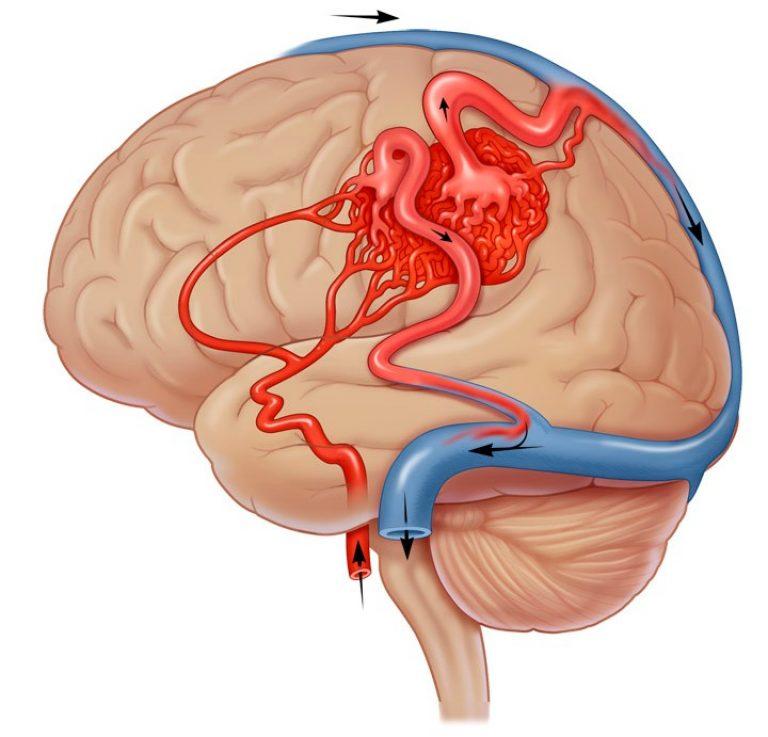
Артериовенозная мальформация (АВМ) головного мозга – это локальный дефект архитектоники внутричерепных сосудов, при котором формируется беспорядочное соединение между артериями и венами с образованием извитого сосудистого клубка. Патология возникает вследствие ошибки морфогенеза, а потому в основном является врожденной. Может быть одиночной или распространенной.
При мозговой АВМ кровоток осуществляется аномально: кровь из артериального бассейна прямиком, обходя капиллярную сеть, перебрасывается в венозную магистраль. В зоне мальформации отсутствует нормальная промежуточная капиллярная сеть, а связующий узел представлен фистулами или шунтами в количестве 1 и более единиц. Стенки артерий дегенерированы и не имеют надлежащего мышечного слоя. Вены, как правило, расширены и истончены по причине нарушенной ауторегуляции мозгового кровотока.
АВМ головного мозга, как и аневризмы, опасны внезапным внутримозговым кровоизлиянием, которое возникает вследствие разрыва стенки патологического сосуда. Разорвавшаяся мальформация чревата ишемией мозга, отеком, гематомой, прогрессией неврологического дефицита, что не всегда для больного заканчивается благополучно.
Статистика заболеваемости и последствий патологии
Артериовенозная мальформация в структуре всех патологий с объемными образованиями в тканях головного мозга в среднем составляет 2,7%. В общей статистике острых нетравматических геморрагий в субарахноидальное пространство, 8,5%-9% случаев кровоизлияний происходят по причине мальформаций. Инсультов головного мозга – 1%.
Встречаемость заболевания происходит со следующей средней частотой в год: 4 случая на 100 тыс. населения. Некоторые зарубежные авторы указывают другую цифру – 15-18 случаев. Несмотря на врожденную природу развития, клинически проявляется только у 20%-30% детей. Причем возрастной пик обнаружения АВМ ГМ у детей приходится на младенчество (≈13,5%) и возраст 8-9 лет (столько же %). Считается, что у ребенка с таким диагностированным сосудистым нарушением риски разрыва гораздо выше.
По статистике, мальформации проявляют себя по большей мере в возрасте 30-40 лет, поэтому диагностируются чаще у людей именно этой возрастной группы. Заболевание обычно протекает скрыто в течение десятков лет, чем и объясняется такая тенденция его определения далеко не в детские годы. Половой закономерности в развитии церебральных АВМ у мужского и женского пола пациентов не обнаружено.
При наличии мальформации ГМ вероятность разрыва составляет от 2% до 5% в год, с каждым последующим годом риски увеличиваются. Если кровоизлияние уже состоялось, риск его повторного рецидива существенно возрастает, вплоть до 18%.
Летальные исходы из-за внутричерепного кровоизлияния, которое часто является первым проявлением болезни (в 55%-75% случаев), случаются у 10%-25% пациентов. Смертность вследствие разрыва, согласно исследованиям, больший процент имеет у детей (23%-25%), чем у взрослых людей (10%-15%). Инвалидизация от последствий заболевания отмечается у 30%-50% больных. Примерно к 10%-20% пациентов возвращается полноценное или приближенное к норме качество жизни. Причина такой грозной тенденции заключается в поздней диагностике, несвоевременном получении квалифицированной медицинской помощи.
В какой части головы локализируются АВМ головного мозга?
Распространенная локализация артериовенозной аномалии – это супратенториальное пространство (верхние отделы мозга), проходящее над палаткой мозжечка. Чтобы было понятнее, изъяснимся проще: сосудистый дефект примерно в 85% случаев обнаруживается в больших полушариях. Преобладают поражения сосудистых звеньев теменной, лобной, затылочной, височной долей больших полушарий.
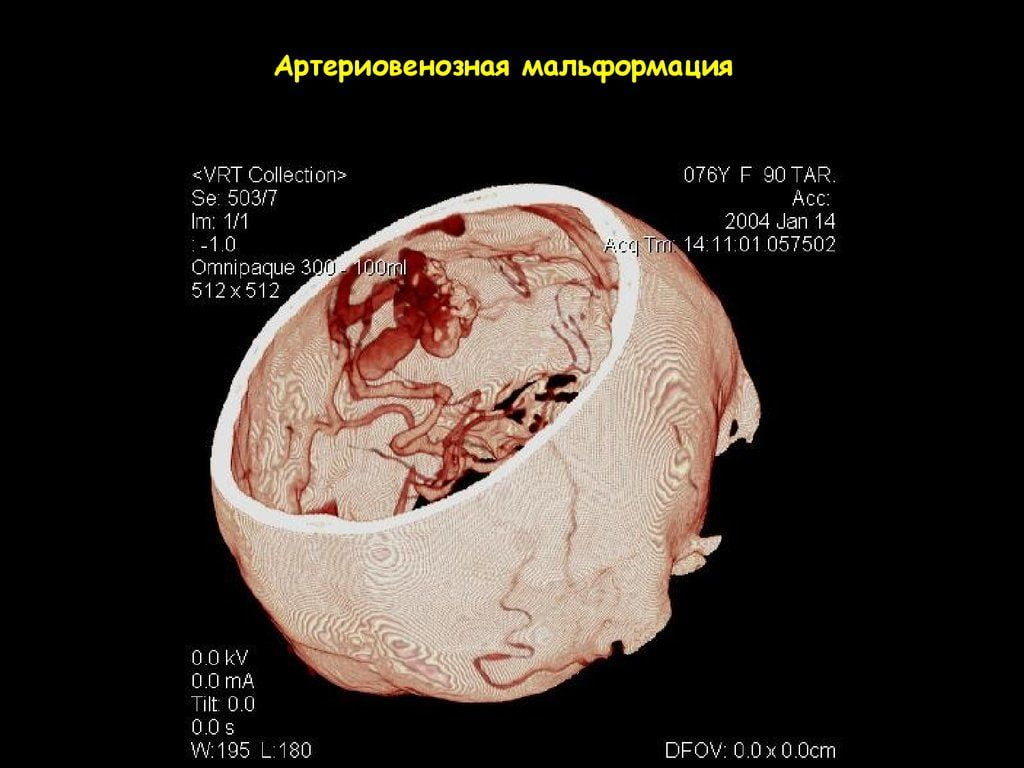
В целом, АВМ могут располагаться в любом полюсе головного мозга, причем как в поверхностных частях, так и глубинных слоях (таламусе и др.). Достоверно определить точную локализацию очага возможно только после прохождения аппаратного исследования с возможностями визуализации мягких тканей. К базовым принципам диагностики относят МРТ и метод ангиографии. Эти методы позволяют качественно оценить порядок ветвления артерий и построение вен, их соединение между собой, калибр ядра АВМ, афференты артерий, дренирующие вены.
Причины развития артериовенозного порока и симптомы
Заболевание является врожденным, поэтому анормальная закладка сосудов в определенных зонах мозга происходит в ходе внутриутробного периода. Достоверные причины развития патологии до текущего момента так и не установлены. Но, по словам специалистов, на аномальное строение сосудистой системы ГМ у плода предположительно могут способствовать негативные факторы в течение беременности:
- получение организмом матери высоких доз радиации;
- внутриутробные инфекции, передающиеся в дородовом периоде от матери к ребенку;
- хронические или острые интоксикации;
- курение и прием алкогольных напитков;
- наркотические средства, в том числе из ряда медикаментов;
- лекарственные препараты, обладающие тератогенным действием;
- хронические болезни у беременной в анамнезе (клубочковый нефрит, диабет, бронхиальная астма, пр.).
Специалисты также полагают, что в формировании порока может играть роль и генетический фактор. Наследственность до недавнего времени не воспринималась как причина патологии серьезно. Сегодня же все больше поступает сообщений о причастности и данного фактора. Так, в ряде случаев у кровных родственников больного определяются аналогичного типа сосудистые пороки. Предположительно их вызывает передающаяся по наследству генная мутация, затрагивающая хромосому 5q, локус СМС1 и RASA1.
Как было сказано ранее, для заболевания характерно продолжительное «немое» течение, которое может продолжаться десятилетиями. О диагнозе либо узнают случайно в момент диагностического обследования структур головного мозга, либо уже после случившегося разрыва мальформации. В немногочисленных вариантах болезнь может давать о себе знать до того как лопнет сосуд. Тогда клиника патологии чаще проявляется такими симптомами, как:
- шум в ушах (звон, гул, шипение и т.п.);
- частые головные боли;
- судорожный синдром, который схож с эпилептическими приступами;
- неврологические симптомы (парестезии, ощущения онемения, покалывания, вялость и апатия, пр.).
Клиническая картина при разрыве АВМ подобна всем типам внутричерепных кровоизлияний:
- резкое появление сильной головной боли, быстро прогрессирующей;
- головокружение, спутанность сознания;
- обмороки, вплоть до развития комы;
- тошнота, рвота;
- выпадение чувствительности половины тела;
- нарушение зрения, слуха;
- экспрессивная афазия, дизартрия (нарушения произношения);
- быстро нарастающий неврологический дефицит.
У детей заболевание зачастую проявляется отставанием в психическом развитии, задержкой речевых функций, эпиприступами, симптомами сердечной недостаточности, когнитивными нарушениями.
Виды церебральных мальформаций венозно-артериального русла
Патологические образования принято различать по топографо-анатомическому признаку, гемодинамической активности, размерам. Первый параметр характеризует место расположения мальформации в головном мозге, отсюда происходят их названия:
- поверхностные АВМ – сосредоточены в коре больших полушарий мозга (на поверхности мозга) и прилежащих структурах белого вещества;
- глубинные АВМ – локализуются в глубине мозговых извилин, базальных ганглиях, внутри желудочков, в структурах ствола ГМ.
По гемодинамической активности выделяют мальформации:
- активные – к ним причисляют смешанного вида АВМ ГМ (самая частая разновидность, при которой обнаруживается частичная деструкция капилляров) и фистулезного типа (артерия прямо переходит в вену, капиллярная сеть полностью разрушена);
- неактивные – капиллярные (телеангиоэктазии), венозные, артериовенозные кавернозные.
Поражение также оценивается по размерам, учитывается диаметр только клубка мальформации. При диагностике размеров используют следующие наименования АВМ:
- микромальформации – менее 10 мм;
- малые – от 10 мм до 20 мм;
- средние – 20-40 мм
- большие – 40-60 мм
- гигантские – более 6 см в диаметре.
Для предупреждения тяжелой геморрагии и связанных с ней необратимых осложнений крайне важно выявить и устранить очаг в ближайшее время, до разрыва. Почему? Объяснение куда более убедительное – при разрывах слишком большой процент людей погибает (до 75% пациентов) от обширного кровоизлияния, несопоставимого с жизнью.
Необходимо понимать, что сосуды АВМ слишком подвержены прорывам, так как они серьезно истощены на почве ненормального строения и нарушенного тока крови. Одновременно с этим, крупные порочные образования сдавливают и повреждают окружающие мозговые ткани, что несет дополнительную угрозу состоятельности функций ЦНС. Поэтому, если диагноз подтвержден клинически, оттягивать с лечением ни в коем случае нельзя.
Методы лечения мальформаций сосудов головного мозга
Терапия заключается в полной резекции или полноценной облитерации сосудистого дефекта хирургическим путем. Существует 3 вида высокотехнологичных операций, которые применяются в этих целях: эндоваскулярное лечение, стереотаксическая радиохирургия, микрохирургическое вмешательство.
- Эндоваскулярная операция. Метод подходит для лечения глубоко расположенных и крупных образований. Вмешательство выполняется под рентгенологическим контролем, анестезиологическое обеспечение – наркоз общего типа. Эта малоинвазивная тактика нередко является начальным этапом лечения перед предстоящей открытой операцией.
- К патологической части головного мозга через бедренную артерию по сосудам подводят тонкую трубочку катетера.
- Через установленный проводник в область мальформации подается специальный клеевый биоматериал, похожий на монтажную пену.
- Нейрохирург пенным составом перекрывает участки поражения, то есть тромбирует аномально развитые сосуды при сохранении здоровых.
- Эмболизация позволяет «выключить» патологическое сплетение из общей системы мозгового кровообращения.
- После выполненной операции под стационарным наблюдением пациент обычно находится 1-5 суток.
- Стереотаксическая радиохирургия. Лечебная тактика хоть и относится к ангионейрохирургии, но не является травматичной. Это означает, что никаких разрезов, введения внутрисосудистых зондов вообще не будет. Подходит для лечения сосудистого порока небольших размеров (до 3,5 см) или в том случае, когда очаг расположен в неоперабельной секции мозга.
- Радиохирургия предполагает разрушение ангиом системами вида Кибер-нож или Гамма-нож.
- Аппараты работают по принципу прицеленного воздействия на аномалию радиоактивным облучением.
- Лучи испускаются с разных сторон и сходятся в одной точке только дефектной зоны, здоровые структуры не затрагиваются. В результате сосуды АВМ срастаются, очаг подавляется.
- На Кибер- или Гамма-ноже процедуры абсолютно безболезненные, во время лечения пациент находится в сознании. Аппараты, на кушетке которых нужно будет просто неподвижно лежать (от 30 минут до 1,5 часов), напоминают традиционные томографы.
- При лечении Гамма-ножом на голову надевается специальный шлем и жестко фиксируется. Чтобы пациент, которому ставят шлем, не испытывал чувства дискомфорта, делают поверхностное местное обезболивание отдельных участков головы. Операция на Кибер-ноже не требует анестезии и помещения головы в жесткую конструкцию.
- В госпитализации нет необходимости. Но возможно понадобится пройти не один сеанс радиохирургии, чтобы окончательно ликвидировать остаточные явления АВМ ГМ. Иногда процесс облитерации длится 2-4 года.
- Прямое микрохирургическое удаление. Микрохирургия при данном диагнозе – единственный метод, который дает максимально высокие шансы на радикальное излечение патологии, сведение до минимума рисков рецидива. Является «золотым стандартом» в лечении данного заболевания с поверхностной локализацией и компактными формами узла.
- Микрохирургическая операция не обходится без типичной краниотомии, обязательно выполняется экономное вскрытие черепа для проведения основных хирургических манипуляций на мозге.
- Вмешательство проходит под общей эндотрахеальной анестезией, под контролем сверхмощного интраоперационного микроскопа и ультразвукового оборудования.
- Для предотвращения кровяного сброса по питающему артериальному сосуду и вене применяется метод биполярной коагуляции, то есть осуществляется прижигание.
- Далее единым блоком через трепанационное окно производится одномоментное иссечение всего тела мальформации с минимальными кровопотерями.
- В конце операционного сеанса отверстие в черепе закрывается костным лоскутом, на кожные покровы накладывается шов.
- Выписка возможна ориентировочно через 14 суток после операции. Далее нужно продолжить послеоперационное восстановление в специализированном центре реабилитации. Продолжительность реабилитации устанавливается индивидуально.
Видео открытой операции можно посмотреть по ссылке: https://www.youtube.com/watch?v=WA2FTX1NK1Y
В определенных ситуациях невозможно сразу приступить к прямой микрохирургии ввиду высоких интраоперационных рисков, особенно при АВМ больших размеров. Или же другой вариант: ангиома после стереотаксии или катетерной эмболизации лишь частично компенсирована, что крайне плохо. Поэтому иногда целесообразно обращаться к поэтапному лечению, используя последовательную комбинацию нескольких ангионейрохирургических методов.
Где лучше оперироваться и цены операции
Грамотно спланированный алгоритм лечебных действий поможет полностью удалить сосудистый конгломерат не в ущерб жизненно важным тканям. Адекватность терапии с учетом принципа индивидуальности убережет от прогрессии неврологических отклонений, возможного раннего рецидива со всеми вытекающими последствиями.
Оперировать высший орган ЦНС, который отвечает за множество функций в организме (двигательные способности, память, мышление, речь, обоняние, зрение, слух и пр.), следует доверять мирового уровня нейрохирургам. Кроме того, медучреждение должно быть снаряжено широкой базой высокотехнологичного интраоперационного оборудования передового образца.
В зарубежных странах с высокоразвитой нейрохирургией услуги стоят дорого, зато там, что называется, возвращают пациентов к жизни. Среди популярных направлений, одинаково продвинутых в хирургии головного мозга, выделяют Чехию, Израиль и Германию. В чешских клиниках цены на медицинскую помощь по поводу артериовенозных мальформаций самые низкие. Невысокая стоимость, совершенная квалификация чешских врачей-нейрохирургов сделали Чехию самым востребованным направлением. В это государство стремятся попасть не только пациенты из России и Украины, но и Германии, Израиля, других стран. И коротко о ценах.
Источник