- Дегенеративные изменения нейтрофилов
- Токсическая (токсогенная) зернистость нейтрофилов
- Метод Фрейфельд
- Токсическая зернистость нейтрофилов (фотографии)
- Тельца Деле
- Тельца Деле (микрофотографии)
- Цитоплазматические вакуоли
- Вакуолизация (микрофотографии)
- Гиперсегментация сегментоядерных нейтрофилов
- Гиперсегментация нейтрофилов (фотографии)
- Гипосегментация ядра (пельгероид, псевдопельгеровская аномалия)
- Пельгероид, псевдопельгеровская аномалия (фотографии)
- Другие дегенеративные изменения нейтрофилов
- Кариорексис (микрофотографии)
- Литература:
- Похожие статьи
- Морфология клеток эритроцитарного ростка
- Морфология клеток моноцитарного ростка
- Конституциональные аномалии нейтрофилов
- Патологические включения в эритроцитах
- Морфология клеток лимфоидного ростка
- Гиперсегментация ядер лейкоцитов что это значит
Дегенеративные изменения нейтрофилов
Дегенеративные изменения нейтрофилов возникают при различных патологических состояниях (инфекциях, воздействии химических веществ, заболеваниях кроветворного аппарата, действии проникающих излучений, попадании внутрь радиоактивных веществ и др.) и могут затрагивать и ядро, и цитоплазму. К ним относятся:
Токсическая (токсогенная) зернистость нейтрофилов
Токсическая (токсогенная) зернистость нейтрофилов — грубая зернистость, сходная с азурофильными гранулами. Образование ее происходит внутри клетки в результате физико-химических изменений белковой структуры цитоплазмы под влиянием продуктов интоксикации. Наблюдается при инфекционных или воспалительных процессах. Может сопровождаться присутствием цитоплазматических вакуолей и телец Деле.
Токсическая зернистость нейтрофилов нередко появляется раньше ядерного сдвига. Ее нарастание при гнойно-септических заболеваниях, крупозной пневмонии и ряде воспалительных заболеваний указывает на прогрессирование патологического процесса и возможность неблагоприятного исхода. В большом количестве токсическая зернистость нейтрофилов появляется при распаде опухолевой ткани под влиянием лучевой терапии. Наиболее выражена токсическая зернистость при крупозной пневмонии в период рассасывания воспалительного инфильтрата, при скарлатине, септикопиемии, перитоните, флегмоне и прочих гнойных процессах. Особенно важное значение имеет она в диагностике острого живота (например, гангренозного аппендицита, протекающего с незначительно повышенной температурой тела и, нередко, при отсутствии лейкоцитоза).
Токсическую зернистость нейтрофилов можно обнаружить при окраске мазков обычным способом. Однако, даже при качественной окраске, пылевидная токсогенная зернистость может быть не видна, а при перекрашивании мазка (даже незначительном) за токсогенную можно принять специфическую зернистость нейтрофильных гранулоцитов. Поэтому для выявления токсической зернистости нейтрофилов предложены специальные методы окраски, из которых наиболее распространенным и доступным является метод Фрейфельд
Метод Фрейфельд
Для окраски мазка используют следующие красители:
- 1 г основного фуксина растворяют при слабом нагревании в 15 г этилового спирта (96), охлаждают и добавляют 100 мл 5% раствора карболовой кислоты.
- 1% водный раствор метиленового синего.
Рабочую смесь готовят непосредственно перед окраской, так как она непригодна для хранения. К 20 мл водопроводной воды приливают 7 капель первой краски, смешивают, прибавляют 5 капель второй краски и снова перемешивают.
Мазки крови, фиксированные в течение 3 минут метиловым спиртом, красят в течение 1 часа приготовленной рабочей смесью красителя, а затем смывают водой и высушивают. Препарат, уже окрашенный по Романовскому, может быть окрашен этим способом без предварительного обесцвечивания.
В результате такой окраски в цитоплазме нейтрофилов выявляется синеватая зернистость различного размера (от пылевидной до хлопьевидной) в зависимости от тяжести патологического процесса. Подсчитывают количество клеток с токсической зернистостью в процентах (на 100 нейтрофильных гранулоцитов). В анализе указывают также величину зернистости (пылевидная, мелкая, средняя, крупная, хлопьевидная).
Токсическая зернистость нейтрофилов (фотографии)
Тельца Деле
Тельца (включения) Деле (Князькова-Деле, Доули) — светло-синие глыбки различного размера и формы, представляющие собой РНК из фрагментов шероховатого эндоплазматического ретикулума. Появляются при инфекционных и воспалительных заболеваниях (иногда даже при легком течении). Часто встречаются в сочетании с токсической зернистостью и цитоплазматическими вакуолями.
Тельца Деле (микрофотографии)
Цитоплазматические вакуоли
Цитоплазматические вакуоли — наблюдаются при тяжелых инфекциях, часто в сочетании с токсической зернистостью и тельцами Деле. При остром сепсисе, вызванном анаэробной инфекцией, и выраженном лейкоцитозе наблюдается вакуолизация практически всех нейтрофилов. Иногда вакуолизация выявляется при аномалии Джордана (семейной вакуолизации лейкоцитов).
Вакуолизация (микрофотографии)
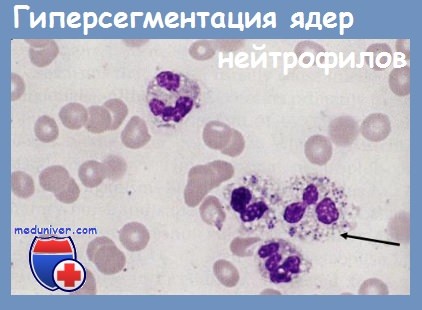
Гиперсегментация сегментоядерных нейтрофилов
Гиперсегментация сегментоядерных нейтрофилов — ядро имеет более пяти долей, соединенных тонкой хроматиновой нитью. Встречаются при мегалобластных анемиях. Может отмечаться (редко) у здоровых людей как наследственная (семейная) конституциональная особенность.
Гиперсегментация нейтрофилов (фотографии)
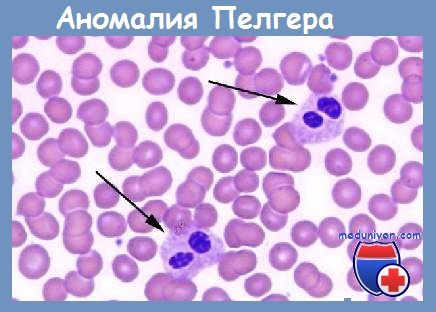
Гипосегментация ядра (пельгероид, псевдопельгеровская аномалия)
Гипосегментация ядра (пельгероид, псевдопельгеровская аномалия) — увеличение количества двусегментированных нейтрофилов, а также палочкоядерных нейтрофилов и нейтрофилов с круглым ядром. При этом хроматин имеет плотную структуру. Встречается при лейкозах, миелопролиферативных заболеваниях, МДС, агранулоцитозе, множественной миеломе, микседеме, малярии, при инфекционных заболеваниях, при приеме некоторых лекарственных препаратов. Образование их связывают с блокадой ферментов, ответственных за сегментацию ядер. Следует отличать от пельгеровской аномалии (при пельгероиде изменения со стороны нейтрофилов носят непостоянный характер, в отличие от пельгеровской аномалии).
Пельгероид, псевдопельгеровская аномалия (фотографии)
Другие дегенеративные изменения нейтрофилов
Кольцеобразные ядра — ядра имеют форму кольца. Наблюдаются при тяжелом алкоголизме.
Хроматинолиз — при распаде хроматин теряет свою нормальную структуру — растворяется. Ядро окрашивается в светлый цвет, контуры его сохраняются.
Кариолиз — растворение лишь части ядра с сохранением его нормальной структуры. В местах растворения ядро теряет способность окрашиваться основными красками, контуры его нечеткие, размытые.
Фрагментоз — процесс при котором от ядра отделяются отдельные фрагменты (частицы). Они могут быть связаны с ядром тонкими нитями базихроматина.
Пикноз — уплотнение базихроматина ядра. Ядро при этом становится темным, бесструктурным. Размер клетки уменьшается. Процесс пикнотизации распространяется либо на все ядро, либо на отдельные его участки или сегменты.
Кариорексис — распад ядра на отдельные части, не связанные между собой, округлой формы и резко пикнотичные, темные бесструктурные образования.
Кариорексис (микрофотографии)
Цитолиз — распад клетки. Цитоплазма чаще отсутствует. Ядро теряет свою обычную структуру, контуры его расплывчатые. В тяжелых случаях можно обнаружить только остатки ядра и зернистость.
Литература:
- Л. В. Козловская, А. Ю. Николаев. Учебное пособие по клиническим лабораторным методам исследования. Москва, Медицина, 1985 г.
- Фред Дж. Шиффман. «Патофизиология крови». Пер. с англ. — М. — СПб.: «Издательство БИНОМ» — «Невский Диалект», 2000 г.
- Руководство к практическим занятиям по клинической лабораторной диагностике. Под ред. проф. М. А. Базарновой, проф. В. Т. Морозовой. Киев, «Вища школа», 1988 г.
- Руководство по клинической лабораторной диагностике. (Части 1 — 2) Под ред. проф. М. А. Базарновой, академика АМН СССР А. И. Воробьева. Киев, «Вища школа», 1991 г.
- Справочник по клиническим лабораторным методам исследования. Под ред. Е. А. Кост. Москва «Медицина» 1975 г.
Похожие статьи
Морфология клеток эритроцитарного ростка
К морфологически идентифицируемым клеткам эритроцитарного ростка относятся эритробласт, пронормоцит, нормобласты (базофильные, полихроматофильные и оксифильные), ретикулоциты и эритроциты.
Раздел: Гемоцитология
Морфология клеток моноцитарного ростка
Монобласт — родоначальная клетка моноцитарного ряда. Размер 12 — 20 мкм. Ядро большое, чаще круглое, нежносетчатое, светло-фиолетового цвета, содержит 2 — 3 ядрышка. Цитоплазма монобласта сравнительно небольшая, без зернистости, окрашена в голубоватые тона.
Раздел: Гемоцитология
Конституциональные аномалии нейтрофилов
Пельгеровская аномалия нейтрофилов — изменение крови, наследуемое по доминантному типу. Особенность развития пельгеровских лейкоцитов выражается главным образом в морфологическом изменении ядер нейтрофилов — нарушении процесса их сегментации (ядро старое, а форма его юная). Структура ядер пельгеровских нейтрофилов грубоглыбчатая, пикнотическая. Большинство пельгеровских нейтрофилов имеет однодолевое, несегментированное ядро, по форме сходное с палочкоядерными клетками, а также в виде эллипса, окружности, боба или почки, оно короче, чем у обычного нейтрофила. Реже встречаются ядра с намечающейся перетяжкой посередине, напоминающие по форме гимнастическую гирю или земляной орех.
Раздел: Гемоцитология
Патологические включения в эритроцитах
Тельца Жолли (тельца Хауэлла-Жолли) — мелкие круглые фиолетово-красные включения размером 1 — 2 мкм, встречаются по 1 (реже по 2 — 3) в одном эритроците. Предсталяют собой остаток ядра после удаления его РЭС. Выявляются при интенсивном гемолизе и «прегрузке» РЭС, после спленэктомии, при мегалобластной анемии..
Раздел: Гемоцитология
Морфология клеток лимфоидного ростка
Основным местом образования лимфоцитов служит кроветворная ткань селезенки и лимфатических узлов. В костном мозге и периферической крови в норме встречаются только зрелые лимфоциты. При патологии в костном мозге и периферической крови могут появляться незрелые и атипические формы клеток лимфоидного ростка.
Раздел: Гемоцитология
Источник
Гиперсегментация ядер лейкоцитов что это значит
Лейкоцитарные аномалии делятся на две группы: нейтрофильные гранулоцитарные аномалии и эозинофильные гранулоцитарные аномалии.
Среди аномалий нейтрофильных гранулоцитов известны: 1. Аномалия гиперсегментирования ядер нейтрофильных гранулоцитов. Нормально, большинство сегментированных нейтрофильных гранулоцитов имеет трехдолъчатые ядра; при описываемой здесь аномалии преобладают нейтрофилы с четырьмя или даже более нуклеарными дольками. У женщин констатируется повышение пропорции хромозомальных лридатков. В костном мозге промиэлоциты и миэлоциты имеют инцизированное ядро; кроме этого, появляются «гигантские» метамиэлоциты, как при мегалобластических анемиях. Undritz считает, что эти клетки являются предшественниками гиперсегментированных нейтрофилов.
Аномалия передается доминантно. Проявление носит гетерозиготный или гомозиготный характер. Аномалия является чисто гематологической; даже носители-гомозиготы не представляют какого-либо клинического проявления. Эту аномалию описал Undritz в 1943 г.
Реактивное нуклеарное гиперсегментирование появляется при мегалобластических анемиях, где после исчезновения мегалобластов вследствие специфического лечения, гиперсегментирование нейтрофилов может персистировать еще долгое время. Реактивное гиперсегментирование появляется также при различных хронических анемиях, при аноксемиях, декомпенсированных кардио-пневмопатиях. Иногда, при тяжелых инфекциях, вместо отклонения «влево» лейкоцитарной формулы, появляется гиперсегментирование нейтрофилов.
2. Аномалия Давидсона (Davidson) характеризуется наследственно-конституционной полиплоидией нейтрофильных гранулоцитов (тетраплоидия). Известно, что в нормальном состоянии, двуядерные нейтрофильные гранулоциты (два отдельных ядра) существуют лишь в пропорции 0—2°/00. При аномалии Давидсона мы находим 3—16°/00 двуядерных нейтрофилов, имеющих по два диплоидных ядра, нормального вида.
Аномалия передается доминантно и имеет гетерозиготный характер. Описали ее Davidson и сотр. (цитируемые Undritz). Аномалия не сопровождается никаким клиническим или биологическим проявлением.
Подобное, реактивное проявление встречается при кровяных пролиферативных процессах, при токсиинфекционных процессах и после повторных применений ионизирующих излучений.
3. Наследственно-конституционная аномалия размножения в нейтрофилах специфических половых нуклеарных придатков. Нормально, у женщин 3—5% сегментированных нейтрофильных лейкоцитов имеют специфически половые нуклеарные придатки, которые обнаружили Davidson и Smith в 1954 г. При вышеупомянутой аномалии, которую открыл Undritz в 1967 г., пропорция этих придатков возрастает в среднем до 13% у гетерозиготов и до 35% в единственном случае гомозигота, известном до настоящего времени.
Гетерозиготы не представляют никаких клинических или биологических проявлений. В единственном случае гомозигота констатировалась небольшая анемия, которая могла произойти и по другим причинам.
Вышеописанные образования зависят от числа нуклеарных долек.
4. Так, при аномалии Пелгера в гетерозиготной форме, число придатков ниже 1%, а в единственном гомозиготном случае у женщины не было найдено ни одного нуклеарного придатка. С другой стороны, при наследственно-конституционном гиперсегментировании нейтрофилов, пропорция этих образований достигает, у гетерозиготов, 5,5% (по сравнению с 1—3% у нормальных лиц), а у гомозиготов, до 13%. При этой аномалии, рост числа специфически-половых нуклеарных придатков не находится в зависимости от числа нуклеарных долек.
5. Аномалия Земана (Seman) соответствует наследственно-конституционному размножению неспецифических нуклеарных придатков нейтрофилов, констатированную Земаном в 1959 г. (цитированный Undritz), в одной семье, где у вообще здоровых лиц, необычайно, процент нейтрофильных гранулоцитов представлял неспецифические нуклеарные придатки („small clubs», „sessile nodules», „rackets» и т.д.). Передача аномалии имеет доминантный характер; проявление повидимому гетерозиготное.
Клинические проявления отсутствуют. Undritz высказывает некоторые сомнения в связи с существованием этой аномалии. Впрочем, в связи с обоими аномалиями (Земана и предыдущей), существуют некоторые разногласия, на которые мы считаем целесообразным обратить внимание читателей: «специфически-половой нуклеарный придаток», который описали Davidson и Smith, был представлен первыми авторами как имеющим форму «барабанной палочки» (drum-stiks); несколько позже Kosenow и сотр. (цитированные Bessis) утверждали, что и образования, называющиеся „sessile nodules», которые другие авторы, во главе с Undritz (1974), считают неспецифическими для женского пола, являются все-таки специфическими и равнозначными с „drum-sticks» в определении пола.
С другой стороны, в связи с аномалией, описанной Seman, никто не упомянул о том, какая пропорция нуклеарных придатков является нормальной и где начинается аномалия. Так, мы находим у многих больных разные формы придатков в очень высокой пропорции, то же самое и у нормальных лиц, так что мы не располагаем сколько-нибудь определенным критерием, который позволил бы утверждать, что мы имеем дело с аномалией. В наше описание мы включили обе аномалии, так как они фигурируют во всех трудах по гематологии, но с упомянутыми оговорками.
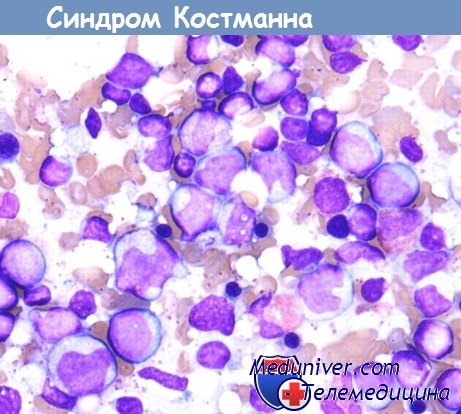
6. Аномалия Костмана (Kostmann) — наследственно-конституционный анейтроцитоз, доходящий до полного отсутствия нейтрофильных гранулоцитов в периферической крови, причем эозинофилы и базофилы присутствуют в нормальной пропорции. Лейкоцитарная формула показывает очень высокий лимфомоноцитоз.
Аномалия передается рецессивно; ее проявление наблюдается только у гомозигота. Kostmann (цитированный Undritz) обнаружил эту аномалию у 14 грудных детей, которые принадлежали родственным семьям, проживавшим на очень ограниченной территории в Швеции. Другие случаи не отмечались.
Аномалия сопровождается такой симптоматологией, которую можно считать естественным последствием анейтроцитоз а: различные инфекционные локализации (фурункулы, абсцессы, флегмоны), с лихорадкой и фатальной эволюцией в течение максимум одного года. До сих пор не был найден никакой эффективный антибиотик. Гетерозиготные родители асимптоматичны. Дифференциальная диагностика производится по отношению ко всем токсиинфекционным, аллергическим, иммунологическим, туморальным и пр. «агранулоцитозам».
7. Аномалия Гицига (Hitzig), считается более доброкачественной формой предыдущей аномалии. Речь идет о семейной нейтропении, сопровождающейся гипергаммаглобулинемией, передающейся доминантно, с гетерозиготным проявлением. Undritz считает, что гомозиготы не были обнаружены, потому что они нежизнеспособны. Эту аномалию описал Hitzig в 1959 г. У гетерозиготов инфекционные осложнения нелетальны. Дифференциальная диагностика производится по отношению ко всем нейтропениям, которые встречаются в практике.
Среди аномалий эозинофильных гранулоцитов известны:
1. Аномалия гиперсегментации ядер эозинофильных гранулоцитов. При этой аномалии, 80—90% эозинофилъных гранулоцитов, имеют три нуклеарные дольки, вместо двух, как это констатируется в нормальном состоянии. Аномалия передается доминантно. Проявление — гетерозиготное. Аномалию описал Undritz в 1943 г.; с тех пор было отмечено множество семейных случаев в Швеции. Клинические проявления отсутствуют.
Реактивное гиперсегментирование эозинофилов встречается при аллергиях, пернициозной анемии, болезни Годжкина и при тропической эозинофилии.
2. Аномалия Презентей (Presentey) соответствует наследственно-конституционному дефициту пероксидаз в эозинофилъных гранулоцитах. В нейтрофилах и моноцитах, реакция остается позитивной (Undritz).
С генетической точки зрения, способ передачи еще не выяснен. Согласно Presentey, передача происходит рецессивно; Undritz, наоборот, утверждает, что эта аномалия передается доминантно. Проявление гетерозиготное. Не существует никаких клинических проявлений. Дифференциальная диагностика производится с отсутствием пероксидаз благодаря порочной технике.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник