Значение слова «гетерозигота»
- Ге́терозиго́тными называют диплоидные или полиплоидные ядра, клетки или многоклеточные организмы, копии генов, которые в гомологичных хромосомах представлены разными аллелями. Когда говорят, что данный организм гетерозиготен (или гетерозиготен по гену X), это означает, что копии генов (или данного гена) в каждой из гомологичных хромосом несколько отличаются друг от друга.
У гетерозиготных индивидов на основе каждого из аллелей синтезируются несколько отличающиеся варианты белка (или транспортных или рибосомальных РНК), кодируемых данным геном. В результате в организме появляется смесь этих вариантов. Если внешне проявляется эффект только одного из них, то такой аллель называют доминантным, а тот, эффект которого не получает внешнего выражения — рецессивным. По традиции при схематическом изображении скрещивания доминирующий аллель обозначают заглавной буквой, а рецессивный — строчной (например, A и a); иногда применяются другие обозначения, например сокращенное название гена со знаками плюс и минус. Собственно гетерозиготные обозначаются aA или Aa.
При полном доминировании (как в классических опытах Менделя при наследовании формы горошин) гетерозиготная особь выглядит как доминантная гомозигота. При скрещивании гомозиготных растений с гладкими горошинами (AA) с гомозиготными растениями с морщинистыми горошинами (aa), у гетерозиготного потомства (Aa) горошины гладкие.
При неполном доминировании наблюдается промежуточный вариант (как при наследовании цвета венчика цветков у многих растений). Например, при скрещивании гомозиготных красных гвоздик (RR) с гомозиготными белыми (rr) у гетерозиготного потомства (Rr) венчики цветков розовые.
Если внешние проявления представляют собой смесь действия обоих аллелей, как при наследовании групп крови у человека, то говорят о кодоминировании.
Следует отметить, что понятия доминантности и рецессивности были сформулированы в рамках классической генетики, и объяснение их с позиций молекулярной генетики наталкивается на определенные терминологические и концептуальные трудности.
гетерозиго́та
1. генет. клетка (или организм), содержащая два различных аллеля в конкретном локусе гомологичных хромосом
Источник
ГЕТЕРОЗИГО́ТНОСТЬ
В книжной версии
Том 7. Москва, 2007, стр. 38-39
Скопировать библиографическую ссылку:
ГЕТЕРОЗИГО́ТНОСТЬ (от гетеро … и зигота ), наличие в генотипе разл. аллелей гена (генов) или разных по структуре гомологичных хромосом. Организм (клетку, вирус) с таким генотипом называют гетерозиготой (термин предложен У. Бэтсоном в 1902). Гетерозиготы обычно условно обозначают лат. символами, напр. Аа , где А – доминантный аллель, оказывающий более сильное влияние на проявление признака, а – рецессивный аллель, подавляемый доминантным. Источник Г. – гибридизация или мутация. Г. обеспечивает изменчивость для микроэволюции природных популяций. Обладая более разнообразным набором аллелей, гетерозиготные особи лучше приспособлены к разл. колебаниям условий внешней среды, отличаются большей жизнестойкостью, продуктивностью, устойчивостью к разл. заболеваниям. В селекции Г. используют для получения исходного материала и гетерозиса. Г. по аллелям гена, предотвращающего самоопыление, у мн. растений поддерживается автоматически. Г., обусловленная хромосомными перестройками ( инверсии и транслокации ), сопровождается снижением плодовитости и долей нормальных потомков человека и др. организмов. Это служит одной из причин стерильности межвидовых гибридов. У человека в гетерозиготном состоянии находится в среднем ок. 10% его генов. Г. здоровых родителей по одинаковому «неблагоприятному» рецессивному аллелю даёт 25% риска рождения детей с наследств. болезнью.
Источник
Гетерозиготная женщина что это значит
В отличие от скрининга на генетические заболевания у новорожденных или генетическую предрасположенность у пациентов, скрининг на носительство менделирующих болезней имеет как основную цель идентификацию здоровых индивидуумов, имеющих высокий риск (25%) рождения детей с тяжелой аутосомно-рецессивной или Х-сцепленной патологией. Принципы скрининга гетерозиготного носительства показаны в блоке.
Для того чтобы обеспечить достаточное выявление носителей, имеющиеся программы скрининга гетерозигот фокусируются на конкретных этнических группах с высокой частотой мутантных аллелей. Скрининг гетерозиготного носительства добровольный и направлен на людей, идентифицирующих самих себя как участников конкретной этнической группы высокого риска.
Скрининг гетерозиготного носительства широко используют для ряда заболеваний со сравнительно высокой частотой носительства: болезни Тея-Сакса — прототип такого скрининга, болезней Гоше и Канавана в популяции евреев ашкенази; серповидноклеточной анемии в популяции афроамериканцев Северной Америки; b-талассемии в областях с высокой встречаемостью, особенно на Кипре и Сардинии или в крупных кровнородственных семьях из Пакистана.
Технология одновременного обнаружения множества различных мутантных аллелей в гене в ходе единственной процедуры (мультиплексное исследование) делает возможным выполнять популяционный скрининг гетерозигот по муковисцидозу, изучая непосредственно ген CFTR на наличие мутаций. Наибольшая сложность при скрининге носительства мутаций в гене CFTR прямым обнаружением мутантных аллелей — выраженная аллельная гетерогенность во многих популяциях и различия в составе аллелей в разных этнических группах.
Например, тестирование с применением базовой панели на 23 мутации (F508 и 22 наиболее частые мутации, обнаруженные у европеоидов неиспанского происхождения), предлагаемое Американским институтом медицинской генетики, может идентифицировать почти 88% всех мутаций и, следовательно, около 80% пар с риском муковисцидоза (т.е. тех, где оба партнера гетерозиготны по мутациям гена CFTR) указанного этнического происхождения. Внесение в панель дополнительных аллелей только незначительно увеличивает чувствительность теста у европеоидов неиспанского происхождения.
Критерии программ скрининга гетерозиготного носительства:
• Высокая частота носителей, по крайней мере, в конкретной популяции.
• Доступность недорогого и достоверного теста с очень низким числом ложноотрицательных и ложноположительных результатов.
• Доступ к генетическому консультированию для пар, идентифицированных как гетерозиготные носители.
• Доступность пренатальной диагностики.
• Приемлемость в обществе и добровольное участие популяции, подлежащей скринингу.
В других популяциях, например испанцев, азиатов и афроамериканцев, частоты и распределение мутантных аллелей совершенно другие. Базовая панель из 23 аллелей обнаружит только 72% носителей среди испанцев, 64% носителей среди афроамериканцев и 49% носителей среди американцев азиатского происхождения. Для таких популяций необходимы расширенные, этнически специфичные панели. Таким образом, многие диагностические лаборатории используют панель мутаций, определяющую мутации F508 плюс четыре десятка других аллелей. В отличие от этого, в популяции евреев ашкенази тестирование только на пять мутаций обнаруживает 94% носителей, что показывает более высокую чувствительность при определении меньшего числа мутаций.
Влияние скрининга носительства при более низкой встречаемости генетического заболевания может оказаться весьма выраженным. Скрининг носительства при болезни Тея-Сакса в популяции евреев ашкенази проводят с 1969 г. Скрининг сопровождался пренатальной диагностикой, уже снизившей встречаемость болезни Тея-Сакса в этой этнической группе на 65-85%.
Предотвращение b-талассемии за счет обнаружения носительства и пренатальной диагностики привело к аналогичному снижению встречаемости болезни на Кипре и Сардинии. В отличие от этого, попытки выявить носителей серповидноклеточной анемии в США в сообществе афроамериканцев оказались менее эффективными и повлияли в меньшей степени на встречаемость болезни.
Успех скрининга носительства при болезни Тея-Сакса и b-талассемии, а также относительная неудача при серповидноклеточной анемии подчеркивают значение общественного согласия на исследования, уровня образования и доступность генетического консультирования и пренатальной диагностики как критически важных требований для эффективности программы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Новая генетика (геномика) в профилактике осложнений беременности
Особенностью многих вариантных генов является то, что они могут долгое время никак себя не проявлять. Патологические симптомы могут возникнуть при дополнительных условиях (особенности питания, беременность, прием лекарств, образ жизни и т. д.). Выяснение этих дополнительных условий помогает эффективно предотвращать развитие заболеваний и их осложнений у носителей вариантных генов.
Тромбофилия как фактор риска осложнений беременности
Тромбофилией называется склонность к развитию тромбов (кровяных сгустков). Тромбофилия может быть угрожающим жизни состоянием, если тромб запирает кровоток. Тромбофилия может быть наследственным нарушением, но может быть связана и с внешними причинами, такими как хирургические операции, ожирение, беременность, использование гормональных контрацептивов, антифосфолипидный синдром, повышение уровня гомоцистеина или долгий период неподвижности. Врачи подозревают наличие тромбофилии у пациентов, имевших тромбозы в прошлом, или у родственников которых были случаи тромбозов, инсультов, инфарктов в молодом возрасте (до 40 — 50 лет). Однако у многих людей с тромбофилией нет никаких симптомов, или эти симптомы проходят незамеченными, поскольку тенденция к тромбофилии недостаточно сильно выражена. Исследования последних лет показали, что наличие тромбофилии сопряжено с повышенным риском развития осложнений беременности (привычное невынашивание, плацентарная недостаточность, задержка роста плода, поздний токсикоз (гестоз)). К числу генных маркеров наследственных тромбофилий относятся мутация метилентетрагидрофолатредуктазы, лейденская мутация и мутация гена протромбина G20210A.
Исследования последних лет показали, что у пациенток с привычным невынашиванием беременности часто обнаруживаются один или несколько генетических маркеров тромбофилии. Например, в одном из исследований было обнаружено наличие лейденской мутации у 19% пациенток с невынашиванием беременности, тогда как в контрольной группе лейденская мутация была обнаружена только у 4% женщин.
Мутация метилентетрагидрофолат-редуктазы
фермента с нарушениями обмена гомоцистеина. Примерно в те же годы было показано, что повышение уровня гомоцистеина является независимым фактором риска развития сосудистых осложнений. Начались попытки выяснения генетической природы дефицита MTHFR. Клонирование гена MTHFR в 1993 г. стало основой для определения мутаций, связанных с различными степенями дефицита данного фермента.
Фолатный цикл
Фермент 5,10-метилентетрагидрофолат-редуктаза относится к группе флавопротеинов и состоит из двух одинаковых субъединиц с молекулярной массой около 70 кДа. MTHFR является ключевым ферментом фолатного цикла. Фолат и фолиевая кислота (синтетический витамин, отсутсвующий в естественных продуктах) являются двумя формами семейства веществ, связанных с птероилглютаминовой кислотой (ПтеГлу). Эта кислота является сложной молекулой, состоящей из птероидной кислоты и одного (моноглютаматы) или нескольких (до 9, полиглютаматы) остатков глютаминовой кислоты (см. рис. 1). Пища, особенно свежая зелень, печень, дрожжи и некоторые фрукты в основном содержат восстановленные полиглютаматы, которые должны быть гидролизованы с помощью фермента птероилполиглютамат-гидролазы до моноглютамата, чтобы они могли быть абсорбированы в проксимальном отделе тонкого кишечника. После всасывания фолат-моноглютамат быстро восстанавливается до тетрагидрофолата, поскольку только восстановленные формы фолата обладают биологической активностью. После метилирования фолаты поступают в кровь в виде 5-метилтетрагидрофолата. Кроме пищи, постоянное поступление 5-метилтетрагидрофолата обеспечивается кишечно-печеночным циклом: птерил-моноглютамат всасывается из кишечника и поступает в печень, где он восстанавливается и метилируется до 5-метилтетрагидрофолата. Образовавшийся 5-метилтетрагидрофолат выделяется с желчью в кишечник, где он затем всасывается и разносится с кровью по всему организму.
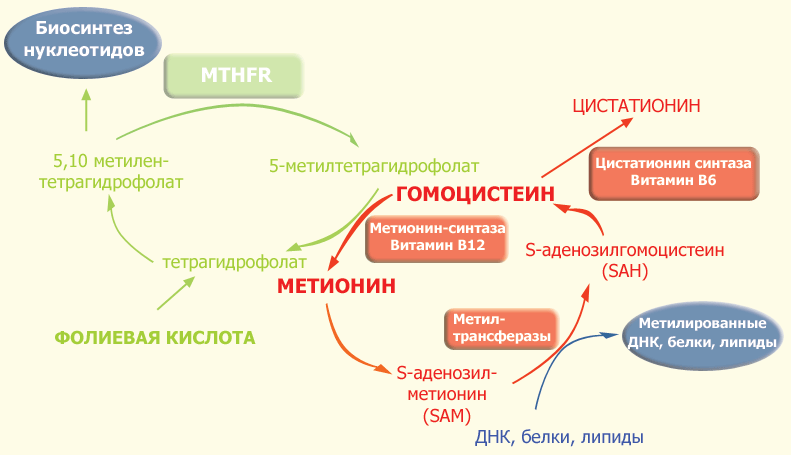 |
| Рис. 1. Фолатный цикл и цикл метионина. |
В ткани поступление 5-метилтетрагидрофолата внутрь клетки происходит с помощью эндоцитоза при участии специфических фолатных рецепторов. Описаны три изоформы фолатных рецепторов. Внутри клетки 5-метилтетрагидрофолат служит донором метильных групп и основным источником тетрагидрофолата. Последний выступает в качестве акцептора большого числа моноуглеродных групп, превращаясь в разные виды фолатов, служащих в свою очередь специфическими коферментами в целом ряде внутриклеточных реакций. К ним относятся 5-формилтетрагидрофолат (фолиниевая кислота, лейковорин), 10-формилтетрагидрофолат и 5,10-метилентетрагидрофолат.
Одной из реакций, требующих наличия 5,10-метилентетрагидрофолата и 5-метилтетрагидрофолата, является синтез метионина из гомоцистеина (путь реметилирования в обмене гомоцистеина). В этой реакции MTHFR играет ключевую роль, восстанавливая 5,10-метилентетрагидрофолат до 5-метилтетрагидрофолата, являясь таким образом катализатором единственной внутри клетки реакции образования 5-метилтетрагидрофолата. Хотя в сыворотке и других тканевых жидкостях обнаруживаются разные формы фолатов, главной формой фолата в плазме является 5-метилтетрагидрофолат, несущий на себе метильную группу, необходимую для превращения гомоцистеина в метионин. В этой реации метильная группа вначале переносится на коб(I)аламин (форма витамина B12), превращая его в метилкобаламин, который затем отдает метильную группу гомоцистеину, образуя метионин с помощью фермента метионин-синтазы. Однако в некоторых случаях коб(I)аламин может окисляться в коб(II)аламин, что приводит к подавлению метионин-синтазы. Для поддержания активности фермента необходимо восстановительное метилирование с помощью фермента метионин-синтаза-редуктазы.
Поскольку кобаламин (витамин B12) служит акцептором метильной группы 5-метилтетрагидрофолата, дефицит этого витамина приводит к «ловушке для фолата». Это тупиковый путь метаболизма, поскольку метилтетрагидрофолат не может при этом восстанавливаться до тетрагидрофолата и возвращаться в фолатный пул. Неспособность регенирировать метионин приводит к истощению запаса метионина и выбросу в кровь избытка гомоцистеина.
Источник









