Гемохроматоз 1 типа гетерозиготной форме что значит
Этиология и встречаемость наследственного гемохроматоза. Наследственный гемохроматоз (MIM №235200) — болезнь накопления железа, встречающаяся у некоторых лиц с гомозиготными или компаундными гетерозиготными мутациями в гене HFE. Большинство пациентов (90-95%) с наследственным гемохроматозом гомозиготны по мутации Cys282Tyr; оставшиеся 5-10% больных — компаундные гетерозиготы по Cys282Tyr и другой мутации, His63Asp. Гомозиготность по мутации His63Asp не ведет к клиническому гемохроматозу, если нет дополнительных причин перегрузки железом.
Частота носительства у белой популяции Северной Америки составляет приблизительно 11% по Cys282Tyr и приблизительно 27% для His63Asp, это означает, что примерно 1 из 330 человек — гомозигота по мутации Cys282Tyr и еще 1 из 135 — ком-паундная гетерозигота по патогенным мутациям в гене HFE. Частота этих мутаций гораздо более низкая среди монголоидов, негроидов и американских индейцев.
Клиническую пенетрантность наследственного гемохроматоза определить трудно; оценки изменяются от 10 до 70%, в зависимости от того, определяется ли наследственный гемохроматоз как органная патология, вызванная накоплением железа, или биохимическим подтверждением повышения насыщения ферритина и уровня трансферрина.
В семейных исследованиях, например, от 75 до 90% гомозиготных родственников больных оказались бессимптомными. Популяционные исследования оценивают пенетрантность наследственного гемохроматоза на основе биохимического подтверждения от 25 до 50%, но пенетрантность может быть более высокой, если выполняется биопсия печени для выявления скрытого цирроза.
Независимо от того, какова пенетрантность, ясно, что мужчины поражаются более часто, чем женщины, и сложные гетерозиготы Cys282Tyr/His63Asp имеют значительно более низкий риск наследственного гемохроматоза, чем гомозиготы Cys282Tyr. Хотя точная величина пенетрантности у гомозигот Cys282Tyr требует окончательного определения, ясно, что пенетрантность неполная.
Патогенез наследственного гемохроматоза
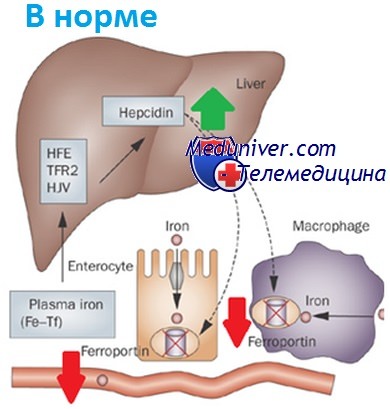
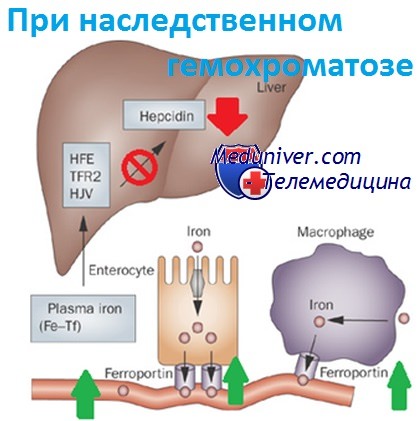
Наследственный гемохроматоз — заболевание, связанное с избытком железа. Запасы железа определяются в основном поглощением его из пищи энтероцитами тонкого кишечника и выходом эндогенного железа из макрофагов, фагоцитирующих эритроциты.
Освобождение железа энтероцитами и макрофагами регулируется циркулирующим гормоном обмена железа, гепсидином, синтезируемым в печени и блокирующим поглощение железа, когда его достаточно. Мутантный белок HFE создает помехи сигналам гепсидина, что приводит к стимуляции энтероцитов и макрофагов к выбросу железа. Таким образом, организм продолжает усваивать железо и использовать его повторно, несмотря на его избыток.
Симптоматика избытка железа развивается лишь у небольшого числа лиц с двумя мутациями в гене HFE. Ранние симптомы включают утомляемость, боли в суставах, снижение либидо и боли в животе. Дополнительные признаки — выявление при обычном обследовании повышенного насыщения трансферрина железом или ферритина. Поздние признаки избытка железа — гепатомегалия, цирроз, печеночно-клеточная карцинома, сахарный диабет, кардиомиопатия, гипогонадизм, артрит и повышенная пигментация кожи. У мужчин симптомы появляются в возрасте 40-60 лет.
Считают, что у женщин симптоматика проявляется вдвое или в десять раз реже, чем у мужчин, симптомы могут не проявиться даже в постменопаузе. Прогноз для пациентов, диагностированных и начавших лечение до развития цирроза печени, отличный. Больные циррозом, получающие эффективное лечение кровопусканиями, все же имеют 10-30% риска развития опухоли печени.
Особенности фенотипических проявлений наследственного гемохроматоза:
• Возраст начала: 40-60 лет у мужчин; в постменопаузе у женщин
• Утомляемость, слабость, гиперпигментация («бронзовая кожа»), сахарный диабет, цирроз, кардиомиопатия
• Высокая насыщенность трансферрина сыворотки железом
• Высокий ферритин сыворотки
Лечение наследственного гемохроматоза
Индивидуумам с генотипом группы риска следует ежегодно контролировать уровень ферритина сыворотки крови. Если содержание ферритина превышает 50 нг/мл, показано кровопускание для удаления некоторого количества крови и поддержания рекомендованной нормальной концентрации ферритина. Кровопускание повторяют до тех пор, пока не будет достигнута нормальная концентрация ферритина. Невозможность достичь нормальной концентрации ферритина в течение 3 мес от начала кровопусканий — плохой прогностический признак.
Как только концентрация ферритина станет ниже 50 нг/ мл, поддерживающие кровопускания проводят каждые 3-4 мес у мужчин и каждые 6-12 мес у женщин. Больным с клиническими проявлениями и начальной концентрацией ферритина более 1000 нг/мл выполняют биопсию печени для уточнения наличия цирроза. Кровопускания пациентам с биохимическими отклонениями необходимо проводить еженедельно, пока гематокрит не составит 75% начального, а концентрация ферритина станет ниже 50 нг/мл.
Риски наследования наследственного гемохроматоза
Наследственный гемохроматоз — аутосомно-рецессивное заболевание с неполной пенетрантностью. Сибсы больного имеют 25% шанс иметь две мутации. Ребенок больного — облигатный носитель с 5% риском иметь две мутации, если оба родителя европеоиды. Из-за очень низкой пенетрантности этой болезни тотальный популяционный скрининг на наличие мутаций гена HFE не считают целесообразным.
Тем не менее из-за распространенности заболевания, неточной определенности пенетрантности и доступности легкого и эффективного лечения, может оказаться оправданным однократное определение насыщения трансферрина сыворотки и концентрации ферритина среди взрослых мужчин северо-европейского происхождения.
Пример наследственного гемохроматоза. С.Ф., 30-летний ранее здоровый мужчина европейского происхождения, направлен на консультацию в клинику генетики, поскольку у его 55-летнего отца только что диагностирован цирроз печени, вызванный наследственным гемохроматозом. Анамнестические сведения и данные медицинского осмотра в норме.
Насыщение трансферрина железом оказалось 48% (в норме 20-50%). Уровень ферритина сыворотки крови также в норме (
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Гемохроматоз
Гемохроматоз характеризуется патологичным накоплением железа, которое избыточно поглощается из пищи и напитков. Избыток железа накапливается в тканях и крупных органах, вызывая их повреждение. Характерным признаком заболевания является изменение цвета кожи, которая приобретает бронзовый оттенок.
Гемохроматоз может быть первичным и вторичным. Как первичное заболевание он возникает в результате генетических изменений, вторично проявляется на фоне другого заболевания.
Избыток железа депонируется в печени, сердце, поджелудочной железе, а также и других органах. Поражение печени является общим и ранним признаком наследственного гемохроматоза. Накопление железа в поджелудочной железе, сопровождается снижением экзо- и эндокринной функций и развитием сахарного диабета. Наследственный гемохроматоз может привести к развитию сахарного диабета, преждевременному старению и раку.
Факторы риска
Существуют некоторые известные факторы риска гемохроматоза:
- Генетические факторы. Наличие двух копий мутированного гена «высокого железа» или гена HFE является самым большим фактором риска наследственного гемохроматоза. Каждый человек наследует одну копию гена от отца, другую от матери.
- Семейная история. Если в семье есть родственник, страдающий гемохроматозом: родитель, ребенок, брат или сестра, то шанс развития заболевания увеличивается в несколько раз.
- Этничность. Люди британского, скандинавского, голландского, немецкого, ирландского и французского происхождения имеют более высокий риск наличия мутации гена хроматоза и развития гемохроматоза.
- Пол. Мужчины значительно чаще страдают гемохроматозом, чем женщины. Первые признаки и симптомы заболевания проявляются в возрасте от 40 до 60 лет. Гемохроматоз у женщин встречается реже. У женщин заболевание манифестирует в основном в период постменопаузы, поскольку в течение репродуктивного периода происходят физиологические потери железа.
Механизм избыточного накопления железа
Только 10% потребляемого железа поглощается организмом. Уровень поглощаемого железа зависит от запасов организма, если их достаточно, то кишечник уменьшает всасывание железа из пищи, тем самым предотвращая избыточное накопление микроэлемента.
У людей с гемохроматозом повышена абсорбция железа до 30% в кишечнике при нормальном его содержании в пище. При такой скорости всасывания, организм не успевает отработать излишнее железо, поэтому оно накапливается в тканях. Первоначально железо откладывается в клетках печени в форме легко мобилизуемого водорастворимого белка ферритина, содержащего 23% железа, позднее — в форме окруженных однослойной мембраной гранул белка гемосидерина, содержащих 35% железа. Избыточное железо токсично для организма. Оно представляет мощный проксидант, поэтому запускает свободно-радикальные реакции, приводящие к повреждению клеточных структур. Образуется «ржавчина».
Наследственный гемохроматоз: генетические причины
HFE — это ген, который контролирует количество поглощаемого железа. Существует две мутации в гене, ответственные за развитие заболевания: C282Y и H63D. Заболевание передается по аутосомно-рецессивной схеме наследования. Большинство людей с наследственным гемохроматозом унаследовали две копии C282Y, одну от матери и другую от отца. Около 31% людей с двумя копиями C282Y развивают симптомы к 50 годам.
Человек, который наследует только один ген с мутацией C282Y, не обязательно будет страдать синдромом перегрузки железом. Однако, всасывание железа в его организме будет происходить активнее, он будет носителем.
Если оба родителя являются носителями, существует вероятность 25% унаследовать два мутированных гена, по одному от каждого родителя. Только некоторый процент людей с двумя копиями мутации C282Y никогда не испытывают симптомов.
Некоторые люди могут наследовать одну C282Y и одну мутацию H63D. У небольшой части этих людей будут проявлены симптомы гемохроматоза.
Наследование двух копий H63D происходит редко. Наличие двух копий мутации H63D может увеличить риск развития гемохроматоза, но эти данные не подтверждены.
Вторичный гемохроматоз: результат состояния
При вторичном гемохроматозе, генетические мутации отсутствуют. Такое состояние развивается при:
- Хронических заболеваниях печени (гепатит С, алкогольная болезнь печени).
- Переливании крови и некоторых видах анемии.
- Редких наследственных заболевания, например, атрансферринемия или ацерулоплазминемия.
- Генетических нарушениях синтеза одной из цепей гемоглобина, например, талассемии.
- Длительном приеме добавок и витаминов, содержащих железо или употребление сверхдоз препаратов.
- Длительном нахождении на почечном диализе.
Неонатальный гемохроматоз
У новорожденных с неонатальным гемохроматозом, железо способно накапливаться быстро в печени. Часто дети рождаются мертвыми, либо быстро погибают после рождения. Исследования показывают, что причина не генетическая. Такое состояние является проявлением следствия выработки материнских антител против клеток печени ребенка.
Симптомы гемохроматоза
Наиболее ранними признаки гемохроматоза являются:
- боль в животе;
- отсутствие менструации;
- высокий уровень сахара в крови;
- сниженная функция щитовидной железы;
- потеря либидо, сексуального влечения;
- уменьшение размера яичек;
- бронзовый цвет кожи;
- выраженная слабость, быстрая утомляемость;
- потеря веса.
Со временем развиваются более тяжелые симптомы:
- артрит;
- цирроз печени;
- сахарный диабет 2-го типа;
- застойная сердечная недостаточность и кардиомиопатии;
- панкреатит.
Диагностика гемохроматоза
Гемохроматоз трудно диагностировать на основании симптомов, поскольку они неспецифичны и характерны для других состояний.
Существует два анализа крови, которые могут диагностировать перегрузку железом:
- Анализ насыщения трансферрином железа. Трансферрин — это белок, который несет железо в крови. Этот тест измеряет количество железа, связанного с трансферрином. Значения насыщенности более 45% слишком высоки.
- Сывороточный ферритин. Этот анализ крови измеряет количество железа, которое хранится в организме. Уровни ферритина в сыворотке помогают проводить контроль лечения.
Для определения предрасположенности к избыточному всасыванию микроэлемента необходимо пройти генетическое исследование.
Источник
Гемохроматоз 1 типа гетерозиготной форме что значит
Гемохроматоз — полисистемное заболевание, наследуемое по аутосомно-рецессивному типу. Обусловлено генетическим дефектом, который приводит к повышенному всасыванию железа.
Генетическое исследование направлено на выявление основных мутаций в гене HFE (C282Y, H63D, S65C), ответственном за развитие наследственного гемохроматоза 1-го типа. Результаты исследования позволяют выявить причину развития данной патологии и назначить своевременное адекватное лечение.
Hemochromatosis, iron metabolism.
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Гемохроматоз – наследственное заболевание, передающееся по аутосомно-рецессивному типу, связано с нарушением обмена железа в организме. Гемохроматоз является одним из самых распространенных генетических заболеваний у белого населения. Встречается у мужчин в 24 раза чаще, чем у женщин. От 85 до 90 процентов людей с гомозиготной мутацией C282Y гена HFE имеют фенотипические проявления. Только у 10 процентов людей, гомозиготных по C282Y, есть клинические проявления гемохроматоза с повреждениями органов.
Симптомы наследственного гемохроматоза неспецифичны и обычно отсутствуют на ранних стадиях. Если симптомы есть, то они могут включать в себя общую слабость, летаргию, артралгию и импотенцию. Более поздние проявления включают в себя артралгию, остеопороз, цирроз печени, гепатоцеллюлярный рак, кардиомиопатию, аритмии, сахарный диабет и гипогонадизм.
Диагноз подтверждается повышенным уровнем ферритина в сыворотке крови и повышенным процентным содержанием насыщения трансферрина. Дальнейшая диагностика заключается в генетическом обследовании для выявления подфенотипов. Биопсия печени проводится для определения степени фиброза или для диагностики нетипичного наследственного гемохроматоза с другими генетическими дефектами. Основным лечением наследственного гемохроматоза является флеботомическая терапия (кровопускание). Флеботомия уменьшает запасы железа в организме, стимулирует эритропоэз и мобилизует железо из паренхиматозных клеток и других мест хранения.
Для чего используется исследование?
- Для выявления мутациЙ в гене HFE, ответственных за развитие наследственного гемохроматоза.
Когда назначается исследование?
- При наличии клинических симптомов и отклонений в лабораторных анализах, свидетельствующих о нарушении метаболизма железа:
— гиперпигментация (бронзовый цвет кожи, не связанный с загаром);
— гепатомегалия (увеличение печени);
— сахарный диабет неясной этиологии;
— нарушения со стороны деятельности сердца;
Что означают результаты?
По результатам исследования выдается заключение генетика с рекомендациями.
Исследуемые генетические локусы не могут доказывать наличие или отсутствие определенных заболеваний и представляют собой генетические факторы риска. Так как оцениваемые признаки являются многофакторными, для конечных рекомендаций необходимы клинические данные, то есть результат генетического теста требует консультации врача наряду с другими лабораторными исследованиями.
В отчете есть таблица с полиморфизмами генов и их интепретацией.
Если пациент является гомозиготным носителем мутаций C282Y, H63D или сложным гетерозиготным носителем мутаций C282Y/H63D, то диагноз «наследственный гемохроматоз» считается установленным. Для верификации диагноза в этих случаях не требуется проведения биопсии печени.
12 Железосвязывающая способность сыворотки
220 Комплексный анализ на витамины группы B (B1, B2, B3, B5, B6, B9, B12)
19 Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с микроскопией мазка крови при выявлении патологических изменений)
Кто назначает исследование?
Гематолог, врач общей практики, врач-терапевт.
- Crownover BK, Covey CJ. Hereditary hemochromatosis. / Am Fam Physician. 2013 Feb 1;87(3):183-90.
- Adams PC, Barton JC. How I treat hemochromatosis. / Blood. 2010 Jul 22;116(3):317-25.
Источник