- Приращение плаценты
- МКБ-10
- Общие сведения
- Причины
- Патогенез
- Классификация
- Симптомы приращения плаценты
- Осложнения
- Диагностика
- Лечение приращения плаценты
- Прогноз и профилактика
- Особенности диагностики истинного врастания плаценты
- Введение
- Ультразвуковая диагностика
- Ретроплацентарная сонолюцентная зона
- Сосудистые лакуны
- Истончение миометрия
- Прерывание линии мочевого пузыря
- Наличие экзофитных масс
- Цветная допплерография
- Магнитно-резонансная томография
Приращение плаценты
Приращение плаценты — это аномалия врастания хориальных ворсин с инвазией трофобласта в базальную отпадающую оболочку, миометрий, периметрий, окружающие органы. Проявляется отсутствием признаков отделения плаценты, профузным маточным кровотечением в последовом периоде, симптомами вовлечения смежных органов (тазовыми болями, примесью крови в кале и моче, запорами и др.). Для диагностики применяют УЗИ тазовых органов, ЦДК, МРТ-пельвиометрию, определение уровня АФП. Лечение предполагает проведение ручного отделения плаценты, надвлагалищной ампутации матки, гистерэктомии, метропластики, донного варианта кесарева сечения.
МКБ-10
Общие сведения
Приращение плаценты было впервые описано в 1836 году английским гинекологом Джеймсом Симпсоном, морфологическую основу расстройства в 1889 году определил немецкий патолог Фредерик Харт. За последние 50 лет отмечается более чем десятикратное увеличение частоты патологии – с 1: 30 000 беременных в 1950-60-х годах до 1:2 500 в 2007 году, что напрямую связано со стремительным ростом числа кесаревых сечений. Зачастую патологическая глубокая инвазия хориона сочетается с предлежанием плаценты. По данным исследований, после первого оперативного родоразрешения риск приращения плацентарной ткани при ее предлежании повышается на 10%, а после 4-5-го — на 60% и более.
Причины
Патологическому врастанию ворсин хориона в маточные оболочки способствуют как локальные дистрофические изменения эндометрия, так и нарушения бластогенеза. Риск развития расстройства повышается по мере увеличения возраста женщины и количества выношенных ею беременностей. По мнению большинства специалистов в сфере акушерства, основными причинами приращения тканей плаценты являются:
- Рубцовые изменения маточной стенки. Предпосылками к возникновению локальной дистрофии эндометрия становятся рубцы после перенесенных оперативных вмешательств, инвазивных манипуляций — кесарева сечения, миомэктомии, аборта, диагностического выскабливания. Дистрофические изменения провоцируются нарушениями процессов кровообращения и рубцовым перерождением эпителия.
- Заболевания матки. Нормальная архитектоника эпителиальной оболочки может нарушаться при неспецифическом и специфическом эндометрите, вызванном возбудителями хламидиоза, гонореи, туберкулеза, других инфекционных заболеваний половых органов. Приращение часто наблюдается при синдроме Ашермана, деформации маточной полости одной крупной или множественными подслизистыми миомами.
- Высокая протеолитическая активность хориона. В части случаев аномалии бластогенеза проявляются не нарушениями гаметогенеза и формированием пороков развития плода, а повышенной инвазивной способностью хориона. Более глубокая имплантация наблюдается при нарушении ферментативного равновесия в системе гиалуронидаза – гиалуроновая кислота между бластоцистой и децидуальной оболочкой.
Дополнительными факторами риска, способствующими аномальному врастанию хориальных ворсин, являются низкое расположение или предлежание плаценты, многоплодие, переношенная беременность, аномалии развития (двурогая матка, наличие внутриматочной перегородки). Патологию чаще выявляют у пациенток, страдающих хроническим гломерулонефритом, тяжелыми формами гестозов, при которых отмечаются микроциркуляторные нарушения в различных органах, в том числе в эндометрии и миометрии.
Патогенез
Механизм приращения плаценты основан на несоответствии проникающей способности трофобласта толщине и строению децидуальной оболочки. Недостаточная толщина эндометрия может быть обусловлена физиологической гипотрофией (функциональный слой слизистой обычно более тонкий в нижнем маточном сегменте) и патологическими процессами. Ситуация усугубляется при повышении протеолитической активности ферментов, способствующих внедрению бластоцисты в стенку матки. При наличии посттравматических, воспалительных, дистрофических изменений наблюдается рубцовое перерождение губчатого слоя отпадающей оболочки плаценты, по которому происходит ее отторжение в третьем периоде родов. При врастании в уплотненную ткань плацентарных ворсин становится невозможным их самопроизвольное отделение от стенки матки.
Значительное истончение эпителия сопровождается частичным или полным отсутствием губчатого слоя. В результате хориальные ворсины отделены от миометрия скоплениями фибриноида, а в более тяжелых случаях непосредственно контактируют с мышечными волокнами и даже прорастают в них на различную глубину. Плацентарные септы частично формируются из миоцитов, происходит обильная васкуляризация миометрия, подлежащего под плацентарной площадкой. После родов кавернозно измененная мышечная ткань не может сокращаться под влиянием окситоцина, что приводит к развитию массивного маточного кровотечения.
Классификация
Критериями для систематизации основных вариантов приращения плаценты служат площадь аномального прикрепления плацентарной ткани, глубина ее врастания в матку. Такой подход обеспечивает более точное прогнозирование осложнений и выбор оптимальной врачебной тактики. Приращение бывает полным с вовлечением в процесс всей плаценты и частичным с наличием участков нормальной и патологической плацентации. В зависимости от глубины проникновения в оболочки матки выделяют следующие виды расстройства:
- Ложное приращение (placenta adhaerens). Имеет более благоприятный прогноз в плане сохранения матки. Встречается значительно чаще, чем истинное. Возникает при рубцовом перерождении губчатого слоя. Хориальные ворсины плотно врастают в децидуальную оболочку и достигают базальной мембраны, однако не проникают до миометрия. Плацента самостоятельно не отделяется, использование специальных приемов ручного разделения плацентарной ткани и матки позволяет обойтись без полостной операции.
- Истинное приращение. Развивается на фоне атрофии губчатого слоя, проявляется проникновением ворсин хориона до мышечных волокон (приращенная плацента), в миометрий (вросшая плацента) и за пределы матки (проросшая плацента). Ручное отделение плаценты невозможно. Зачастую единственным методом, позволяющим сохранить жизнь родильницы, становится хирургическое удаление матки. Частота приращенной плаценты составляет около 78% всех случаев истинного приращения, вросшей — 15%, проросшей — 7%.
Симптомы приращения плаценты
Клинические признаки расстройства во время беременности отсутствуют. Патология проявляется в родах отсутствием внешних признаков отделения детского места в течение получаса после изгнания ребенка: маточное дно не поднимается выше пупка, не наблюдается выпячивание плаценты над симфизом, оставшийся конец пуповины не удлиняется, втягивается после натуживания женщины и укорачивается при надавливании на живот. При полном ложном и истинном приращении послеродовое кровотечение не возникает, при частичном приращении и попытке отделить приросший послед вручную начинается профузное маточное кровотечение. О прорастании плаценты в брюшину и другие органы свидетельствуют тазовые боли различной интенсивности, затруднения дефекации, примесь крови в моче или кале.
Осложнения
При нарушении бластогенеза приращение плаценты может сочетаться с пороками развития плода, хотя и не служит их непосредственной причиной. В дородовом периоде у женщин с нарушением плацентации чаще возникает фетоплацентарная недостаточность, гипоксия плода с задержкой его развития, преждевременное старение плаценты. В родах приращение плацентарной ткани осложняется маточным кровотечением, которое без оказания экстренной помощи способно привести к значительной кровопотере, возникновению геморрагического шока, смерти женщины. В редких случаях у родильниц развивается воздушная эмболия, респираторный дистресс-синдром, ДВС-синдром.
Диагностика
Для своевременного выявления патологии скрининговое обследование проводится всем беременным из группы риска — многократно рожавшим, женщинам с аномалиями матки, низко расположенной или предлежащей плацентой, пациенткам, ранее перенесшим кесарево сечение, миомэктомию, повторные аборты. Наиболее информативными являются методы ультразвуковой диагностики приращения плаценты:
- Эхография. Признаками возможного аномального крепления плацентарной ткани по данным УЗИ матки и плода считаются уменьшение расстояния между ретроплацентарными сосудами и периметрием до 10 мм и менее, наличие в толще плаценты кист, гиперэхогенных включений. Вероятность приращения повышается при обнаружении гипо- и анэхогенных участков с кровотоком лакунарного типа в мышечной стенке матки.
- Цветовое допплеровское картирование (ЦДК). Метод считается золотым стандартом в пренатальной диагностике приращения. В ходе исследования точно определяется локализация аномальных сосудистых зон. Патогномоничным признаком расстройства является расширение субплацентарного венозного комплекса. ЦДК также обеспечивает точную оценку глубины проникновения хориальных ворсин в миометрий.
В последние годы с диагностической целью акушеры-гинекологи все чаще назначают МРТ-пельвиометрию, позволяющую в сомнительных случаях достоверно визуализировать неровности маточной стенки, патологическую неоднородность структуры миометрия и плацентарной ткани. Косвенным лабораторным признаком расстройства служит повышение уровня альфа-фетопротеина.
При выявлении патологии в родах важно быстро выполнить дифференциальную диагностику между ложным и истинным приращением при помощи ручного отделения последа. При плотном прикреплении плацентарную ткань удается отделить полностью и, таким образом, купировать профузное кровотечение. Об истинном приращении свидетельствует невозможность отделения плаценты единым массивом, разрывы тканей, отсутствие отдельных долек, оставшихся в матке. Заболевание дифференцируют с другими расстройствами, сопровождающимися массивными маточными кровотечениями: маточной гипотонией, ДВС-синдромом, коагулопатиями, беременностью с нормально прикрепленной плацентой в трубном углу удвоенной или двурогой матки и др. По показаниям пациентку консультирует уролог, проктолог, хирург, анестезиолог-реаниматолог.
Лечение приращения плаценты
Выявление патологии служит показанием для проведения хирургического вмешательства. При антенатальной диагностике приращения естественные роды противопоказаны, операция выполняется в плановом порядке на 37-39 неделях гестационного срока одновременно с кесаревым сечением, при обнаружении в родах — экстренно по жизненным показаниям. Рекомендованный объем вмешательства определяется типом приращения плаценты:
- Ручное отделение с выделением последа. Акушерское пособие для извлечения неотделившейся плаценты с плодными оболочками проводят под внутривенной анестезией при ложном приращении. В ходе вмешательства акушер отделяет и удаляет плотно прикрепленную плацентарную ткань вручную.
- Удаление матки. При проникновении ворсин хориона к миометрию или их врастании в гладкомышечные волокна традиционно осуществляется надвлагалищная ампутация или гистерэктомия. Несмотря на травматичность, до недавнего времени такие операции были единственным способом остановить кровотечение.
- Органосохраняющие вмешательства. Антенатальная диагностика с последующим проведением донного кесарева сечения или метропластики позволяет сохранить матку даже при истинном приращении. Подобные операции в России пока производят редко, однако накоплен положительный опыт их выполнения за рубежом.
При прорастании маточной стенки рекомендованы комбинированные урогинекологические и проктогинекологические вмешательства, направленные на полное удаление плацентарной ткани. Часто щадящие хирургические методы дополняют эндоваскулярными для профилактики или остановки маточного кровотечения (эмболизацией маточных артерий, временной баллонной окклюзией). При экстренной операции родильнице показано восстановление объема циркулирующей крови с проведением инфузионной терапии (переливания цельной крови, ее компонентов, коллоидных и кристаллоидных растворов). Симптоматическое лечение включает назначение утеротоников (при сохранении матки), гемостатиков, препаратов для поддержания давления и сердечной деятельности.
Прогноз и профилактика
Благоприятный исход приращения плаценты возможен только при своевременной диагностике и выборе оптимального способа лечения. Для улучшения прогноза используют антенатальный скрининг и плановое хирургическое родоразрешение с выполнением операции рекомендованного объема. Первичная профилактика предполагает отказ от необоснованных диагностических и лечебных внутриматочных вмешательств, планирование беременности, лечение воспалительных заболеваний матки, проведение кесарева сечения строго при наличии акушерских или экстрагенитальных показаний.
Источник
Особенности диагностики истинного врастания плаценты
Авторы: Charleen Sze-yan Cheung, Ben Chong-pun Chan
Введение
Патологически адгезивная плацента представляет собой спектр расстройств, характеризующихся аномальным креплением или проникновением плаценты в стенку матки. Гистологически это определяется согласно степени патологического проникновения. Истинное врастание плаценты (ВП) происходит, когда ворсинки плаценты распространяются в миометрий. При placenta percreta инвазии распространяются глубоко за пределы маточной серозы. С клинико-хирургической точки зрения разные степени инвазии могут сосуществовать у одного и того же пациента.
Подавляющее большинство женщин с ВП имеют идентифицируемый фактор риска. Предлежание плаценты и предшествующее кесарево сечение являются основными факторами риска. Риск возрастает с увеличением числа предыдущих кесаревых сечений. Травма и рубцевание миометрия в результате повторных дилатаций и выскабливания или других корректирующих операций также способствуют риску развития аномальной адгезии плаценты. Пожилой возраст матери также был определен как независимый фактор риска. Другие включают курение, многоплодие и периодические выкидыши.
ВП остается основной причиной материнских кровотечений и акушерской гистерэктомии. Выявление факторов риска, точная дородовая и предоперационная диагностика, многопрофильное ведение и соответствующее консультирование помогут в общем ведении женщин с ВП и в снижении материнской заболеваемости.
Ультразвуковая диагностика
УЗИ остается неинвазивным, широко доступным и экономически эффективным методом диагностики первой линии при ВП в клинической практике.
С 1980-х годов были разработаны многочисленные методы ультразвуковой визуализации, чтобы помочь в диагностике ВП антенатально.
Ретроплацентарная сонолюцентная зона
Описывается обычно как чистая зона между плацентой и миометрием. Эта область наблюдается с 12 недель и, как полагают, связана с расширенными сосудами decidua basalis. Недостаточность и прогрессирующая потеря decidua (рис. 1) были предположены и подтверждены гистологически.
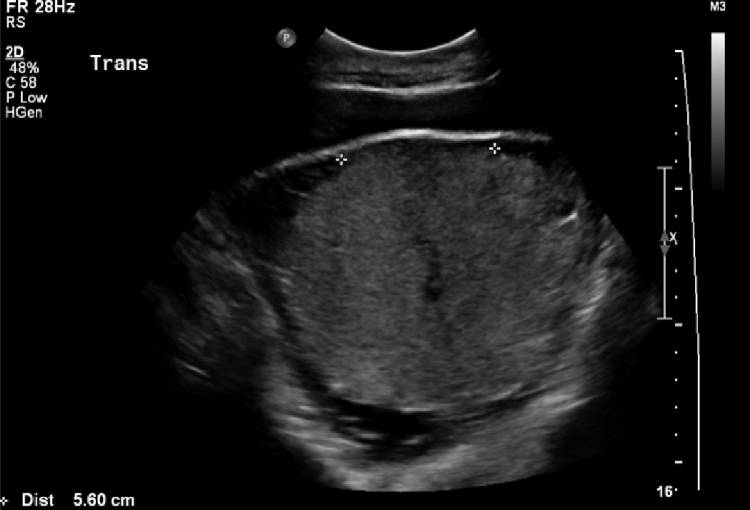
Рисунок 1 : Недостаточность ретроплацентарной сонолюцентной зоны.
Сосудистые лакуны
Многочисленные венозные структуры, встречающиеся по всему миометрию и плаценте были впервые описаны Керром де Мендонса в 1988 г. Последующие наблюдения за плацентарными лакунами описывали их как крупные и нерегулярные образования (вид «швейцарского сыра»). Эти лакуны не обязательно являются областями патологии. Сообщается, что наличие этого сонографического признака связано с самой высокой положительной прогностической ценностью для ВП (рис. 2). При выявлении во втором и третьем триместрах, чувствительность этого признака составляет 79%, с положительным прогностическим значением 92%.
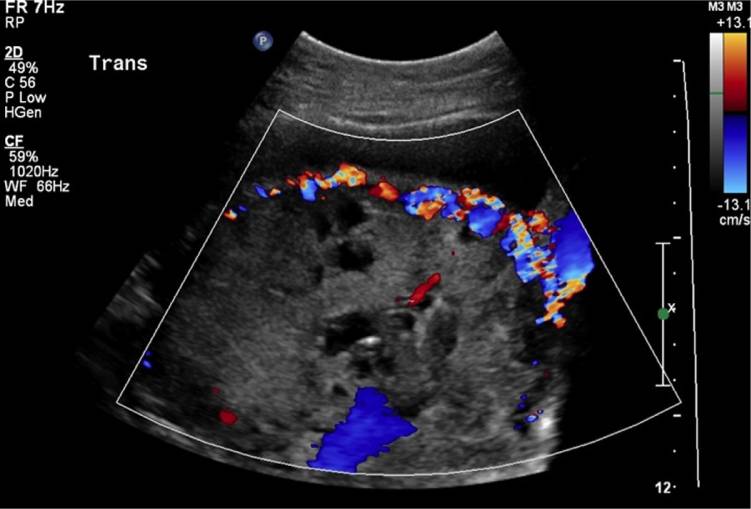
Рисунок 2 : Сосудистые лакуны.
Наличие сонографических критериев не является патогномоничным и должно интерпретироваться с осторожностью в клинических условиях. Хотя установлено, что они обладают высокой чувствительностью и положительной прогностической ценностью, наличие плацентарных лакун и отсутствие сонолюцентной зоны (нередко) наблюдались при предлежании плаценты без врастания.
Истончение миометрия
Прогрессирующее истончение миометрия указывает на близость плацентарной ткани к перитонеальной серозе или окружающим ее внутренностям, в частности к мочевому пузырю. Сегментарное истончение миометрия
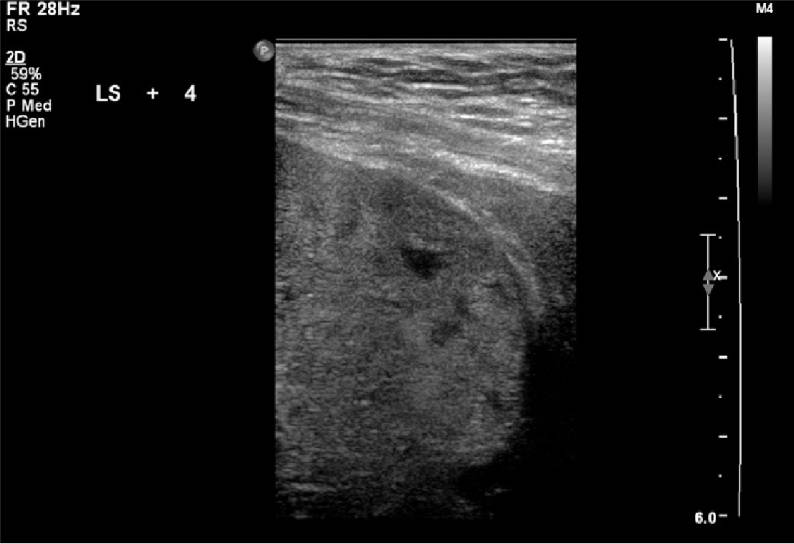
Рисунок 3 : Миометриальное истончение.
Прерывание линии мочевого пузыря
Недостаток ткани миометрия может привести к истончению или нарушению везикоутериновой линии, что, как было установлено, связано с высокой чувствительностью признака (рис. 4).
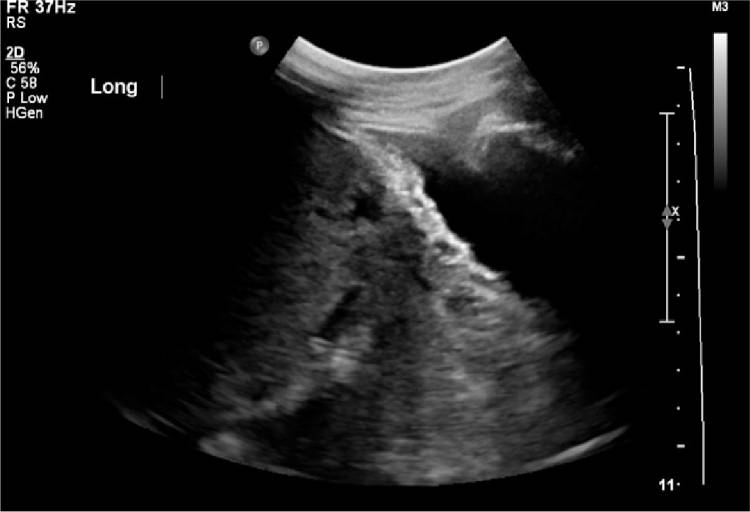
Рисунок 4 : Нарушение целостности линии мочевого пузыря.
Наличие экзофитных масс
В крайних случаях наличие внематочной плацентарной паренхимы может подтвердить диагноз placenta percreta .
Цветная допплерография
Цветной и энергетический допплер обеспечивают более высокую специфичность в диагностике ВП и, в частности, глубины инвазии. Сообщалось о паттерне турбулентного кровотока, распространяющегося из плаценты в окружающие ткани.
ПРАВИЛЬНО ЛИ ВЫ УХАЖИВАЕТЕ ЗА УЗ-АППАРАТОМ?
Скачайте руководство по уходу прямо сейчас
Другие критерии включают очаговый или диффузный внутрипаренхиматозный плацентарный лакунарный кровоток, везикулярную серозную межфазовую гиперваскулярность, выраженный ретроплацентарный венозный комплекс и потерю ретроплацентарных допплеровских сосудистых сигналов.
Магнитно-резонансная томография
УЗИ и МРТ сопоставимы в диагностике ВП. Последнее имеет дополнительное значение в определении глубины инвазии и изображении задней части плаценты.
МРТ часто рекомендуется, когда результаты УЗИ неубедительны. Результаты МРТ, свидетельствующие о ВП включают выпячивание матки, интенсивность гетерогенного сигнала внутри плаценты, темные внутриплацентарные полосы на изображениях, взвешенных по Т2 и прямую визуализацию инвазии плаценты в тазовые структуры.
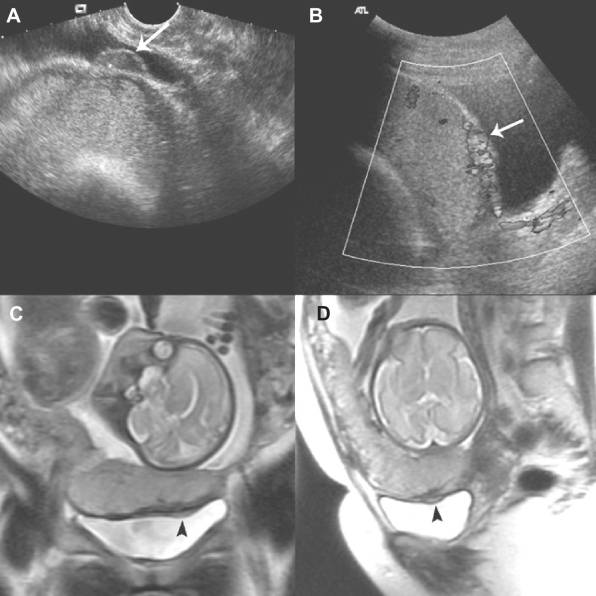
Рисунок 5 : Ультразвуковое исследование с использованием режима допплера, показавшее крупное предлежание плаценты с вовлечением стенки мочевого пузыря.
Примечания : (A) и (B) -Трансвагинальное УЗИ не выявило ткани миометрия между нижней стенкой матки и мочевым пузырем. Также можно увидеть аномальный сосуд, проходящий в стенке мочевого пузыря (белые стрелки). (C) и (D) – Корональные и сагиттальные магнитно-резонансные изображения показали выпуклость на стенке мочевого пузыря (черные стрелки).
Источник