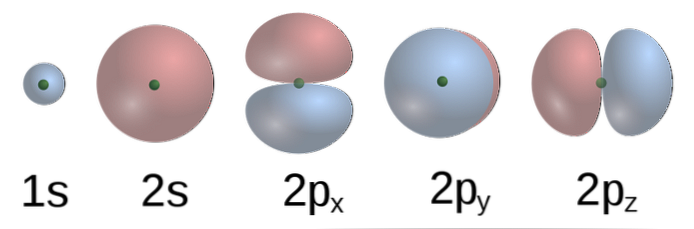- Химическая гибридизация sp, sp2, sp3
- Гибридизация зр 3
- интерпретация
- Отклонения углов ссылок
- Гибридизация зр 2
- Гибридизация зр
- Гибридизация атомных орбиталей
- Типы связей в молекулах органических веществ
- Гибридизация атомных орбиталей углерода
- sp 3 -Гибридизация
- sp 2 -Гибридизация
- sp-Гибридизация
- Добавить комментарий Отменить ответ
Химическая гибридизация sp, sp2, sp3
химическая гибридизация Это «микс» из атомных орбиталей, чье понятие было введено химик Лайнус Полинг в 1931 году для покрытия теории несовершенств валентной связи (ТРВ). Какие недостатки? К ним относятся: молекулярная геометрий и длины эквивалентные связи в молекулах, такие как метан (СНО4).
В соответствии с ТРВ в метана атомных орбиталей формы С четырех связей сг четыре атома H. 2р орбитали, с формами ∞ (нижней) части C расположены перпендикулярно друг к другу, так что Н должны быть отделены друг от друга другой под углом 90 °.
Кроме того, 2с орбиталь (сферическая) связывается с С 1s орбиты Н под углом 135 ° по отношению к другим трем Н. Однако экспериментально установлено, что углы в CH4 109,5º и что, кроме того, длины связей C-H эквивалентны.
Чтобы объяснить это, необходимо рассмотреть комбинацию исходных атомных орбиталей для формирования четырех вырожденных гибридных орбиталей (равной энергии). Здесь идет химическая химия. На что похожи гибридные орбитали? Это зависит от атомных орбиталей, которые их генерируют. Они также показывают смесь электронных характеристик этих.
- 1 sp3 гибридизация
- 1.1 Интерпретация
- 1.2 Отклонения углов звеньев
- 2 Гибридизация sp2
- 3 Гибридизация зр
- 4 Ссылки
Гибридизация зр 3
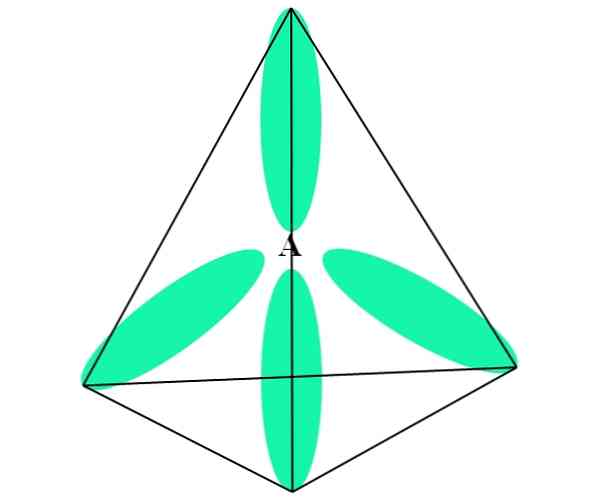
В случае СН4, Гибридизация кл 3 . Из этого подхода молекулярная геометрия объясняется четырьмя sp-орбиталями 3 разделены на 109,5º и направлены к вершинам тетраэдра.
На изображении выше вы можете увидеть, как sp орбитали 3 (зеленый) установить тетраэдрическую электронную среду вокруг атома (A, который является C для CH4).
Почему 109,5º, а не другие углы, чтобы «нарисовать» другую геометрию? Причина в том, что этот угол сводит к минимуму электронные отталкивания четырех атомов, которые связаны с.
Таким образом, молекула СН4 может быть представлен в виде тетраэдра (тетраэдрическая молекулярная геометрия).
Если вместо Н С образует связи с другими группами атомов, то что тогда будет его гибридизацией? Пока углерод образует четыре σ-связи (C-A), его гибридизация будет 3 .
Можно предположить, что в других органических соединениях, таких как СН3OH, CCl4, C (CH3)4, С6H12 (циклогексан) и др., углерод имеет sp-гибридизацию 3 .
Это имеет основополагающее значение для эскиза органических структур, где углерод с простыми связями представляет точки расхождения; то есть структура не остается в одной плоскости.
интерпретация
Какова простейшая интерпретация для этих гибридных орбиталей без учета математических аспектов (волновых функций)? Sp орбитали 3 подразумевают, что они были созданы четырьмя орбиталями: одна с и три р.
Поскольку комбинация этих атомных орбиталей должна быть идеальной, четыре sp-орбитали 3 в результате они идентичны и занимают разные ориентации в пространстве (например, на орбиталях рх, ри и рZ).
Вышеуказанное применимо к остальным возможным гибридизациям: количество образовавшихся гибридных орбиталей такое же, как и у комбинированных атомных орбиталей. Например, sp-гибридные орбитали 3 d 2 они образованы из шести атомных орбиталей: одна s, три p и две d.
Отклонения углов ссылок
Согласно теории электрона пара отталкивания слоя Valencia (VSEPR), пара свободных электронов занимает больше объема, чем атом связанного. Это приводит ссылка отходит уменьшение напряжения электроники и отвлечение углов 109,5º:
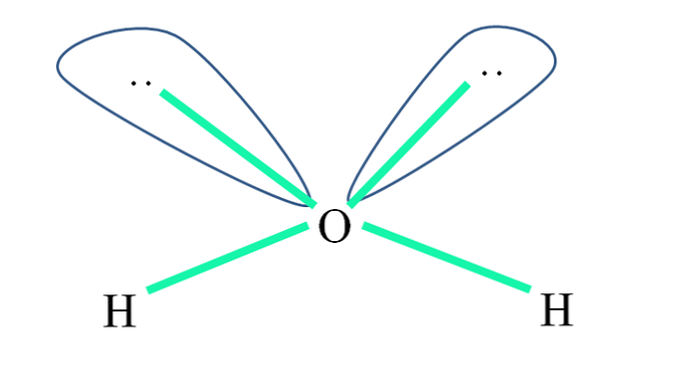
Например, в молекуле воды атомы H связаны со sp-орбиталями 3 (зеленым цветом), а также пары электронов, которые не являются общими «:» занимают эти орбитали.
Отталкиванием этих пар электронов, как правило, представлены в виде «двух шаров с глазами», который, из-за их объема, репелленты двух звеньев сг O-H.
Таким образом, в воде углы звеньев действительно равны 105º вместо 109,5º, ожидаемых для тетраэдрической геометрии..
Какая геометрия у H тогда?2O? Имеет угловую геометрию. Почему? Поскольку, хотя электронная геометрия является тетраэдрической, две пары неразделенных электронов отвлекают ее от угловой геометрии.
Гибридизация зр 2
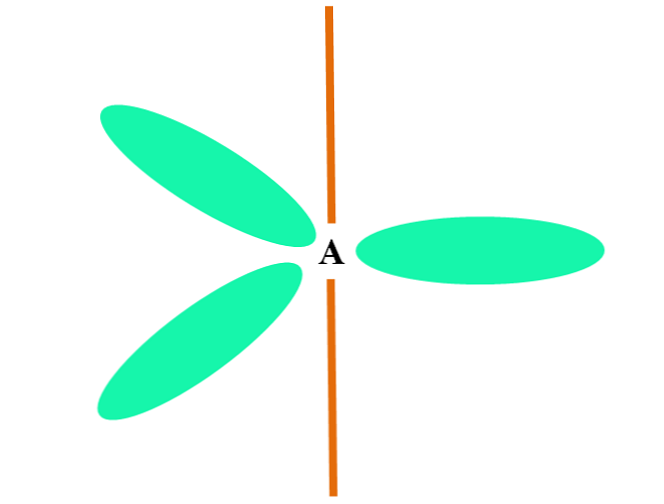
Когда атом объединяет две p и одну s орбитали, он генерирует три sp гибридных орбитали 2 ; тем не менее, орбитальная p остается неизменной (потому что их три), которая представлена оранжевой полосой на изображении выше.
Здесь три sp орбитали 2 они зеленого цвета, чтобы подчеркнуть их отличие от оранжевой полосы: «чистая» орбиталь.
Атом с sp-гибридизацией 2 может быть визуализирован как плоский тригональный пол (треугольник, нарисованный с помощью орбиталей sp 2 зеленого цвета), вершины которого разделены углами 120º и перпендикулярны полосе.
И какую роль играет чистая орбиталь? Это образует двойную связь (=). Sp орбитали 2 позволяют формировать три σ-связи, в то время как чистая p-орбитальная π-связь (двойная или тройная связь подразумевает одну или две π-связи).
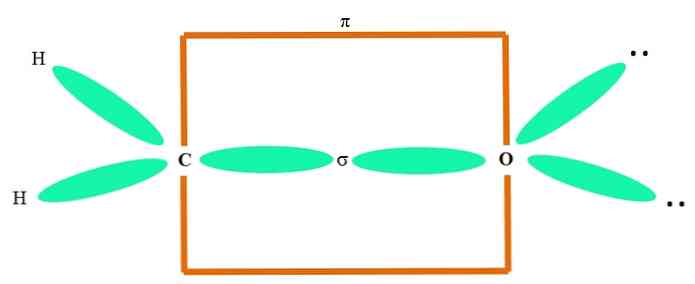
Например, чтобы нарисовать карбонильную группу и структуру молекулы формальдегида (H2С = о), происходит следующим образом:
Sp орбитали 2 оба из C и O образуют связь σ, а их чистые орбитали образуют связь π (оранжевый прямоугольник).
Видно, как остальные электронные группы (атомы H и неразделенные электронные пары) расположены в других sp-орбиталях. 2 , разделены на 120º.
Гибридизация зр
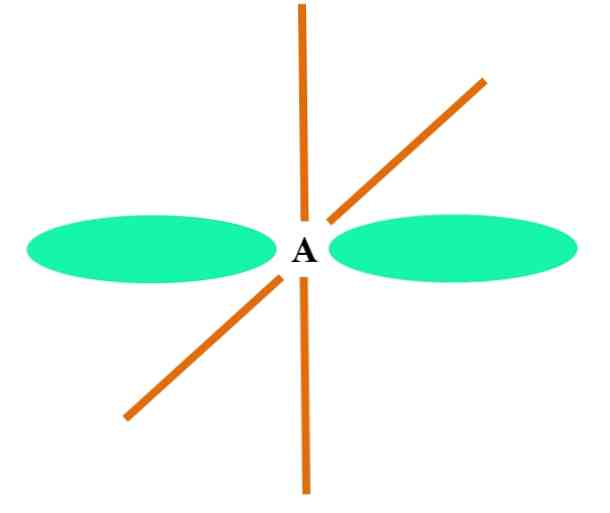
Верхнее изображение показывает атом А с sp-гибридизацией. Здесь орбиталь s и орбиталь s объединяются, чтобы создать две вырожденные sp орбитали. Однако теперь две чистые p-орбитали остаются неизменными, что позволяет A образовывать две двойные связи или тройную связь (≡).
Другими словами: если в структуре C соответствует вышеуказанному (= C = или C≡C), то его гибридизация является sp. Для других менее иллюстративных атомов — таких как переходные металлы — описание электронной и молекулярной геометрий является сложным, поскольку рассматриваются также орбитали d и даже f орбитали..
Гибридные орбитали разделены углом 180 °. По этой причине связанные атомы расположены в линейной молекулярной геометрии (B-A-B). Наконец, на изображении ниже вы можете увидеть структуру аниона цианида:
Источник
Гибридизация атомных орбиталей
Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Типы связей в молекулах органических веществ
Одна из характеристик химических связей — тип перекрывания орбиталей атомов в молекуле.
По характеру перекрывания различают σ-(сигма) и π‑(пи) связи.
| σ-Связь — это связь, в которой перекрывание орбиталей происходит вдоль оси, соединяющей ядра атомов. |
σ-Связь может быть образована любыми типами орбиталей (s, p, d, гибридизованными).
σ-Связь — это основная связь в молекуле, которая преимущественно образуется между атомами.
Между двумя атомами возможна только одна σ-связь.
 |  |
 |  |
 |  |
| π-Связь — это связь, в которой перекрывание орбиталей происходит в плоскости, перпендикулярной оси, соединяющей ядра атомов, сверху и снизу от оси связи. |
π-Связь образуется при перекрывании только р- (или d) орбиталей, перпендикулярных линии связи и параллельных друг другу.
π-Связь является дополнительной к σ-связи, она менее прочная и легче разрывается при химических реакциях.
| Одинарная связь С–С, С–Н, С–О | Двойная связь С=С, С=О | Тройная связь С≡С, С≡N |
| σ-связь | σ-связь + π-связь | σ-связь + две π-связи |
Гибридизация атомных орбиталей углерода
Электронная формула атома углерода в основном состоянии:
+6С 1s 2 2s 2 2p 2
+6С 1s 


В возбужденном состоянии: один электрон переходит с 2s-подуровня на 2р-подуровень.
+6С * 1s 2 2s 1 2p 3
+6С * 1s 2 

Таким образом, в возбужденном состоянии углерод содержит четыре неспаренных электрона, может образовать четыре химические связи и проявляет валентность IV в соединениях.
При образовании четырех химических связей атомом углерода происходит гибридизация атомных орбиталей.
| Гибридизация атомных орбиталей — это выравнивание электронной плотности атомных орбиталей разного типа с образованием новых, молекулярных орбиталей, форма и энергия которых одинаковы. |
В гибридизацию вступают атомные орбитали с небольшой разницей в энергии (как правило, орбитали одного энергетического уровня). В зависимости от числа и типа орбиталей, участвующих в гибридизации, для атома углерода возможны sp 3 , sp 2 и sp-гибридизация.
sp 3 -Гибридизация
В sp 3 -гибридизацию вступают одна s-орбиталь и три p-орбитали. При этом образуются четыре sp 3 -гибридные орбитали:
Изображение с портала orgchem.ru
| Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным. |
Поэтому четыре гибридные орбитали углерода в состоянии sp 3 -гибридизации направлены в пространстве под углом 109 о 28’ друг к другу, что соответствует тетраэдрическому строению.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода. Валентный угол Н–С–Н в метане равен 109 о 28’ |
Молекулам линейных алканов с большим числом атомов углерода соответствует зигзагообразное расположение атомов углерода.
| Например, пространственное строение н-бутана |
sp 2 -Гибридизация
В sp 2 -гибридизацию вступают одна s-орбиталь и две p-орбитали. Одна p-орбиталь не гибридизуется:
| Три sp 2 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным. |
Поэтому три sp 2 -гибридные орбитали атома углерода направлены в пространстве под углом 120 о друг к другу, что соответствует плоскому строению (треугольник).
При этом негибридная р-орбиталь располагается перпендикулярно плоскости, в которой расположены три гибридные sp 2 — орбитали.
Изображение с портала orgchem.ru
| Например, молекула этилена C2H4 имеет плоское строение. Сигма-связь между атомами углерода образуется за счет перекрывания sp 2 -гибридных орбиталей. Пи-связь между атомами углерода образуется за счет перекрывания негибридных р-орбиталей. |
Модель молекулы этилена:
sp-Гибридизация
В sp-гибридизацию вступают одна s-орбиталь и одна p-орбиталь. Две p-орбитали не вступают в гибридизацию:
| Две sp-гибридные орбитали атома углерода направлены в пространстве под углом 180 о друг к другу, что соответствует линейному строению. |
Изображение с портала orgchem.ru
При этом две р-орбитали располагаются перпендикулярно друг другу и перпендикулярно линии, на которой расположены гибридные орбитали.
| Например, молекула ацетилена имеет линейное строение. |
Добавить комментарий Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.
Источник