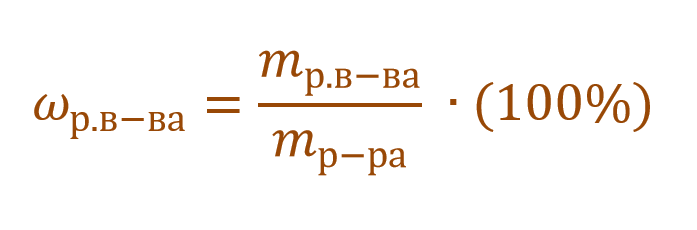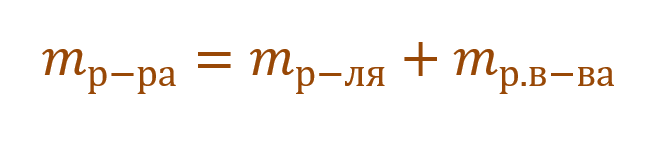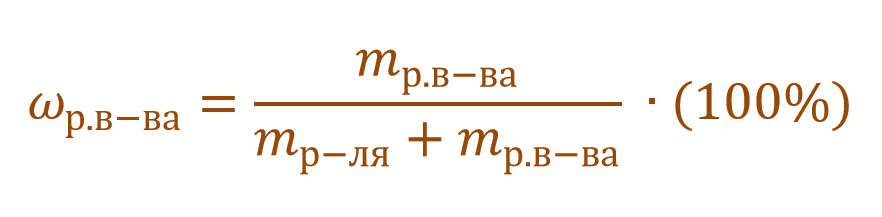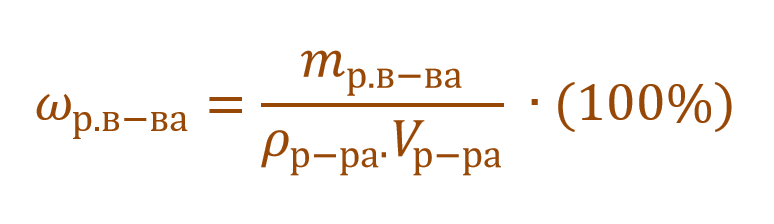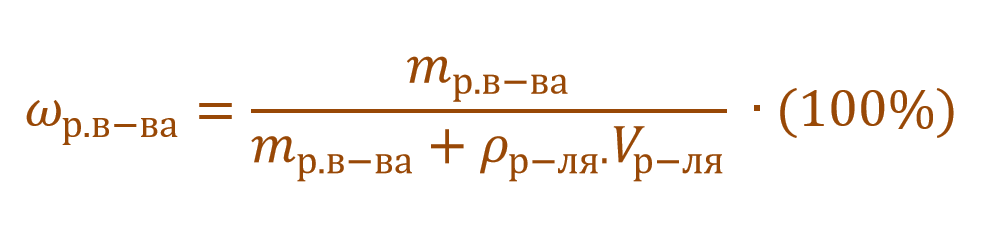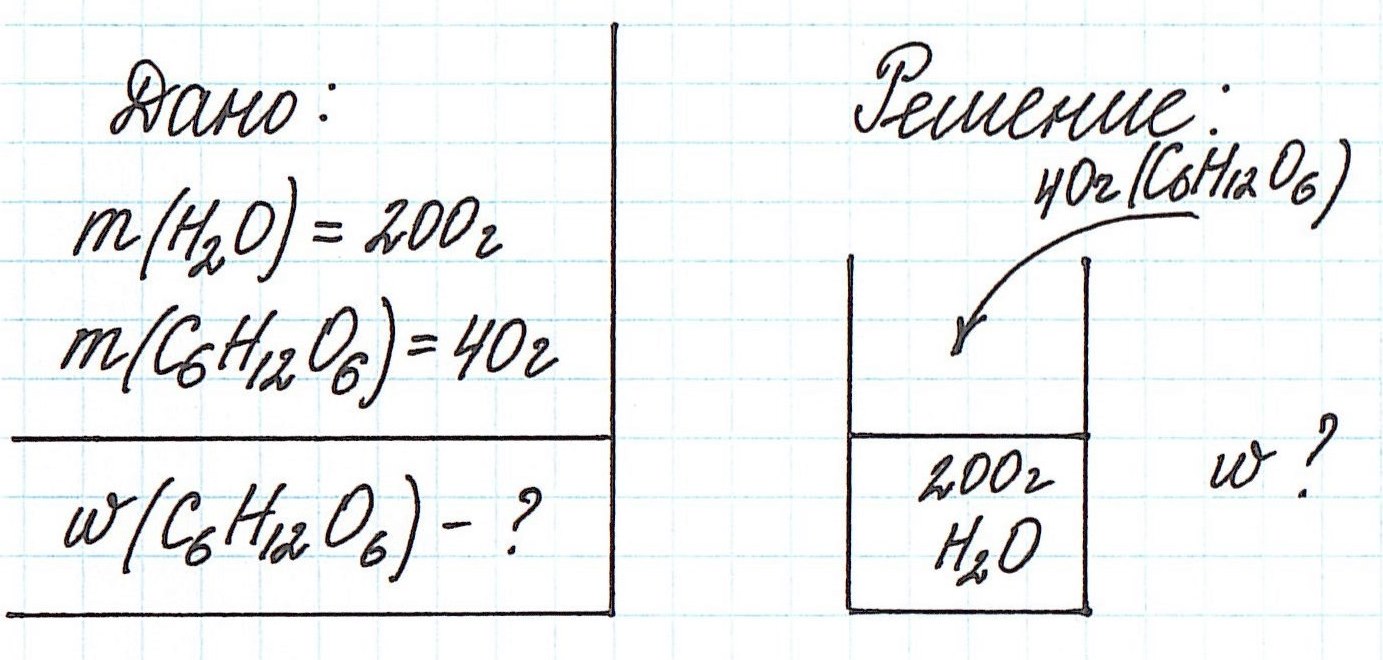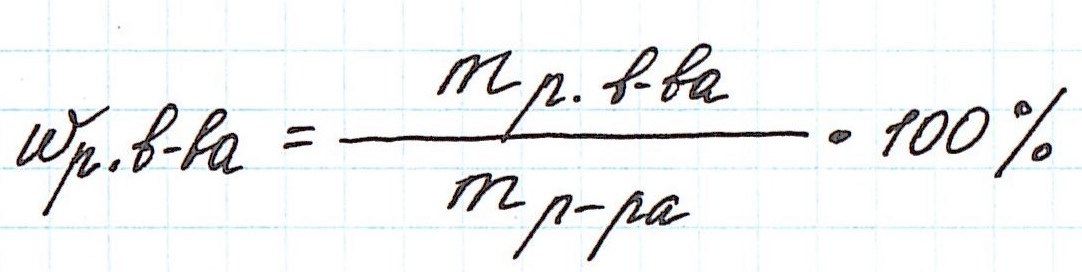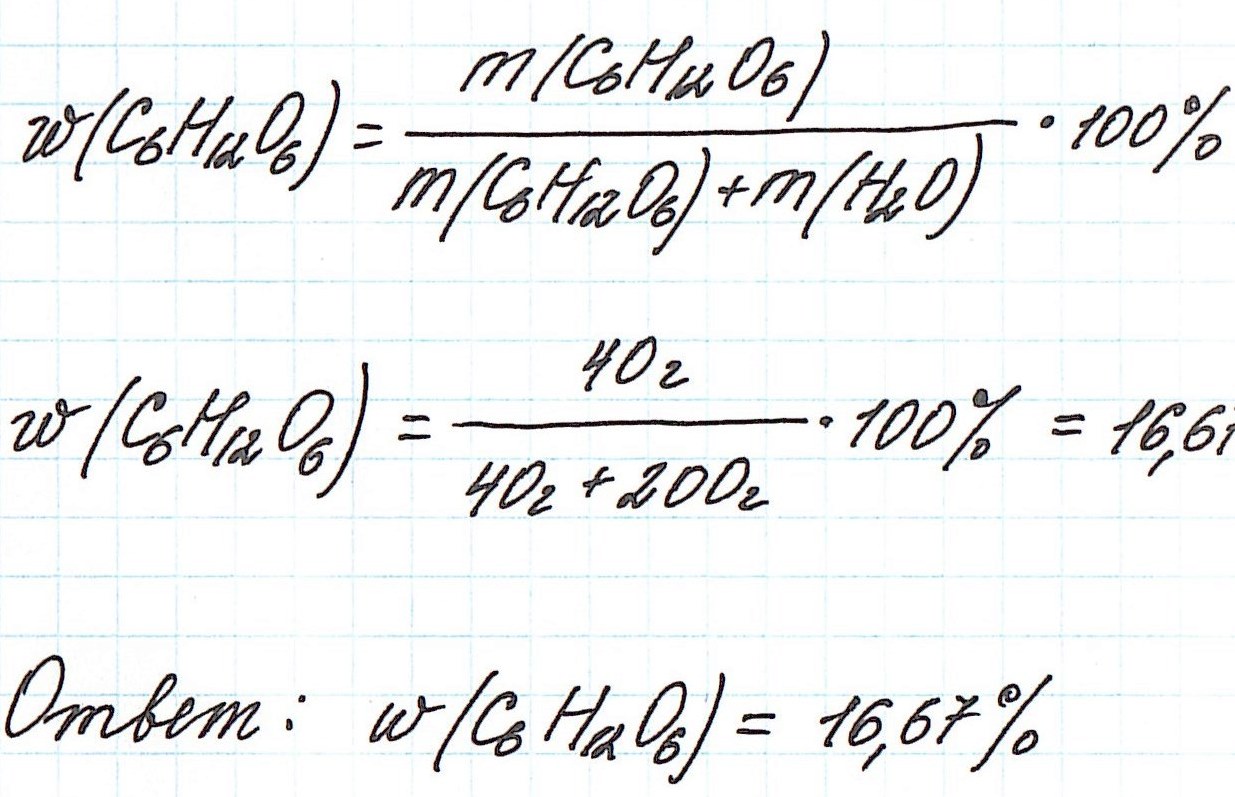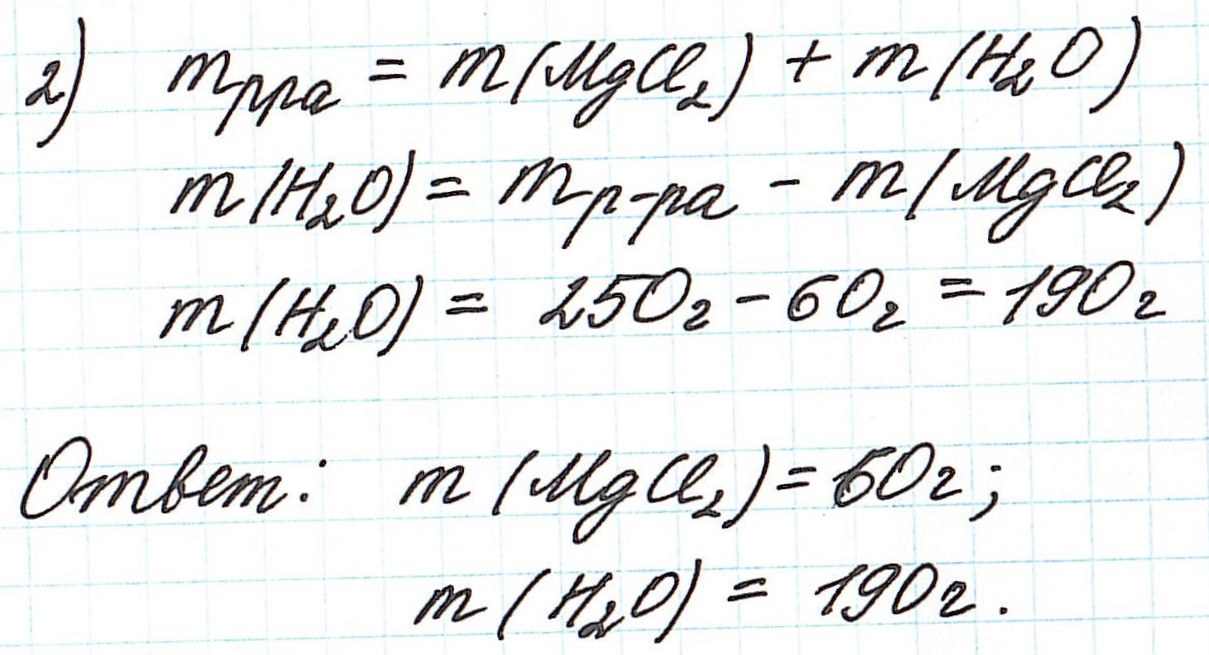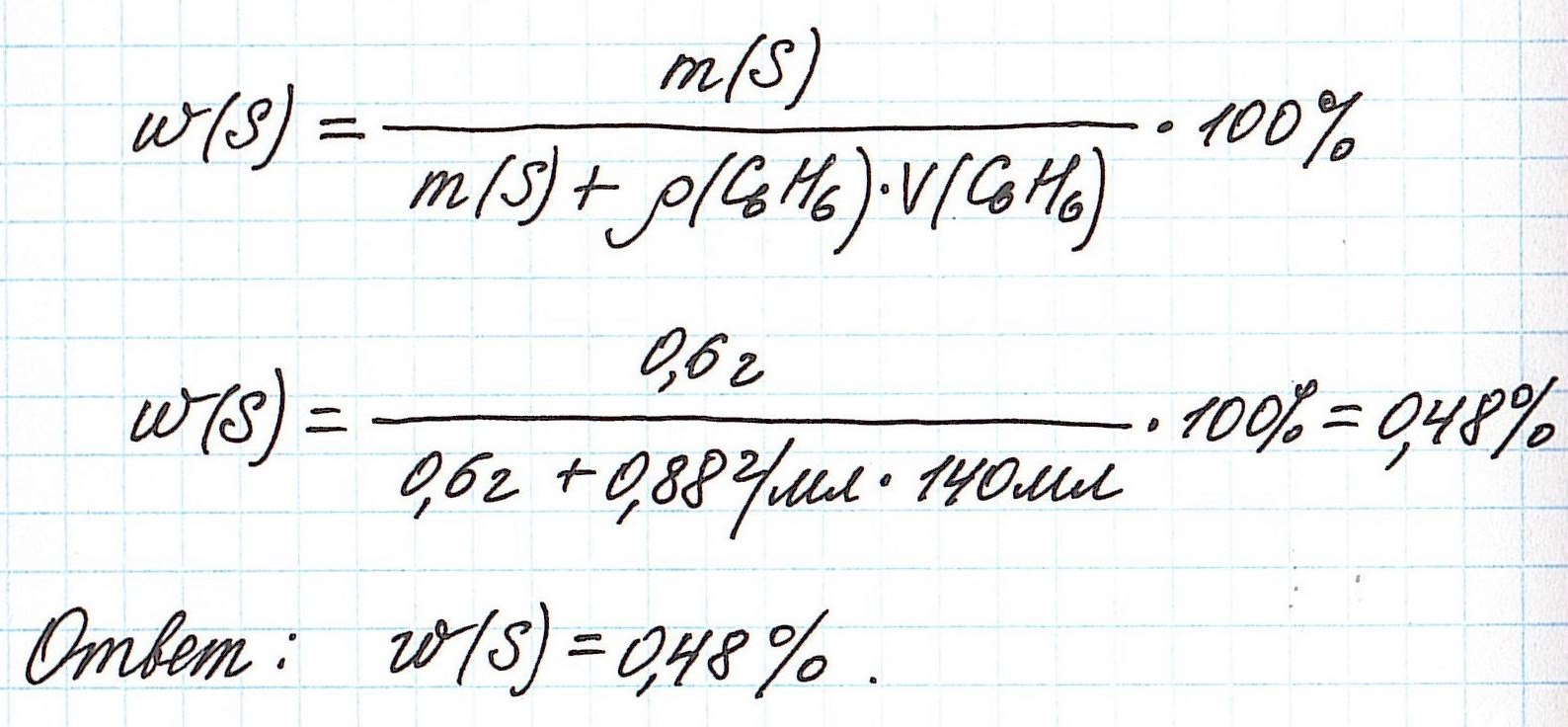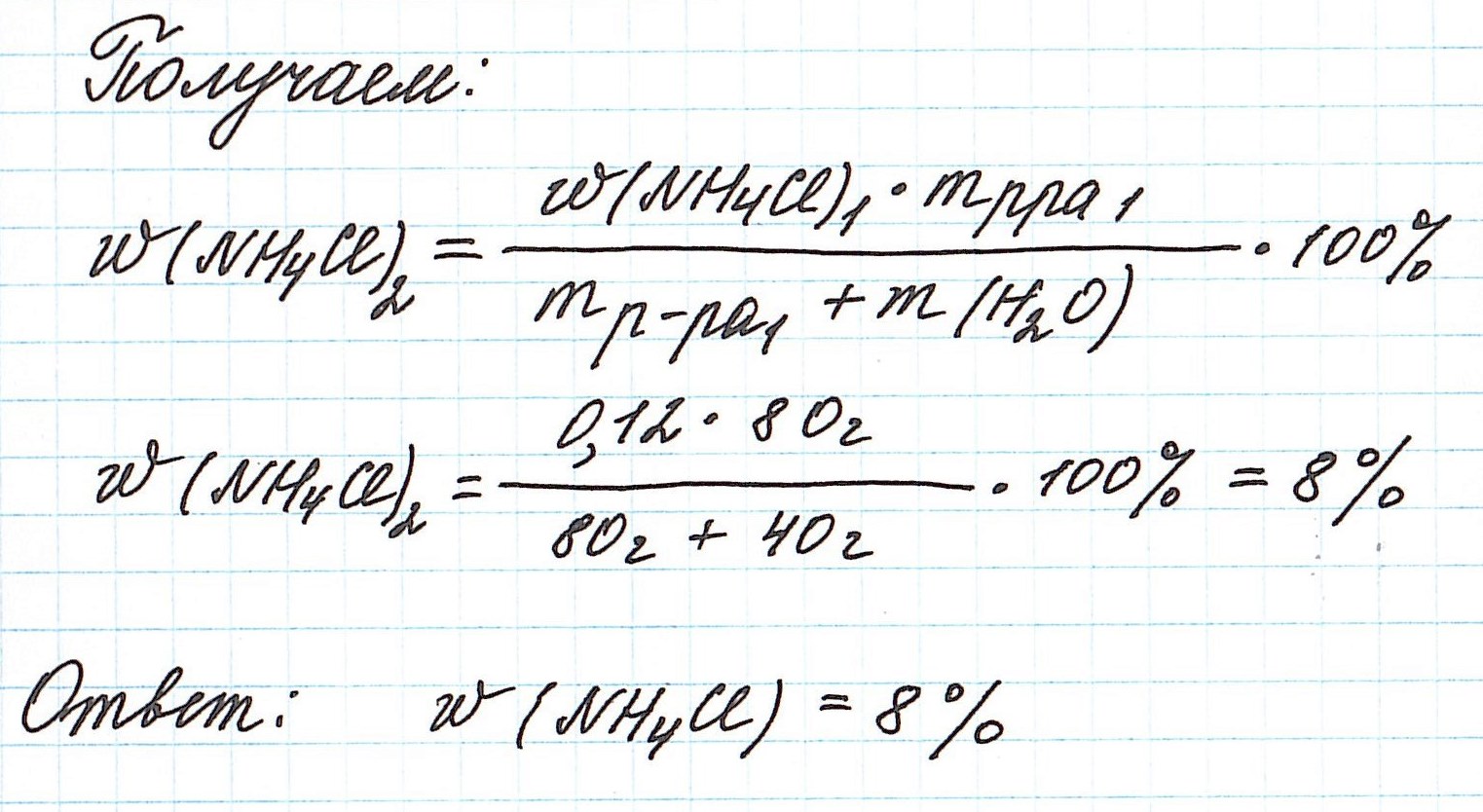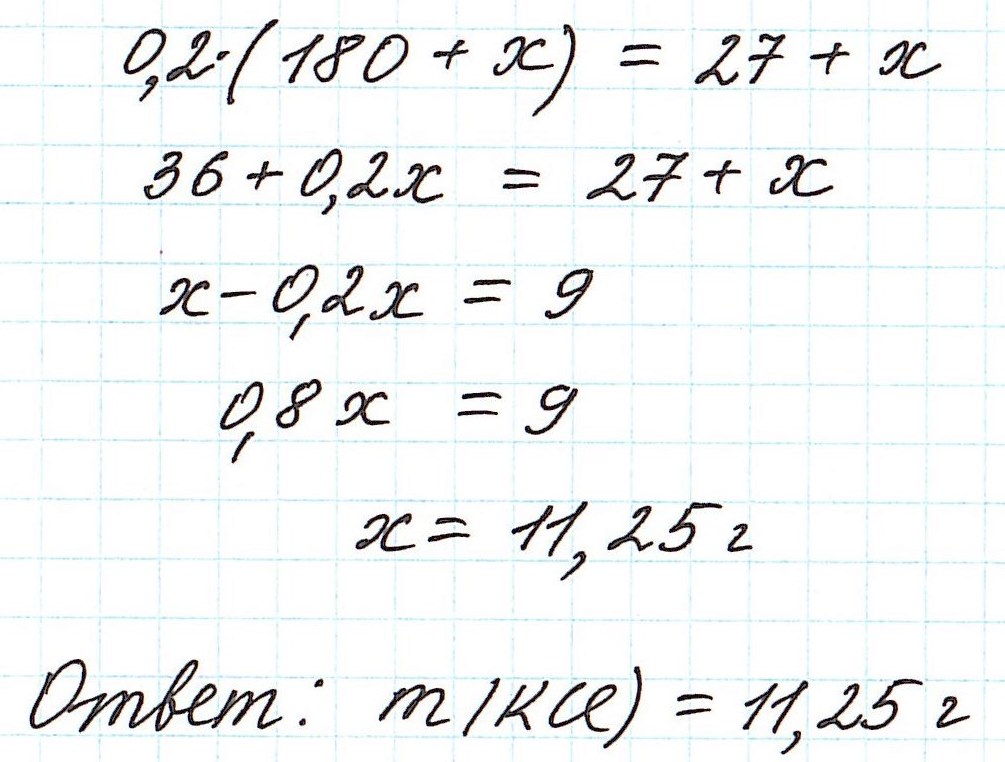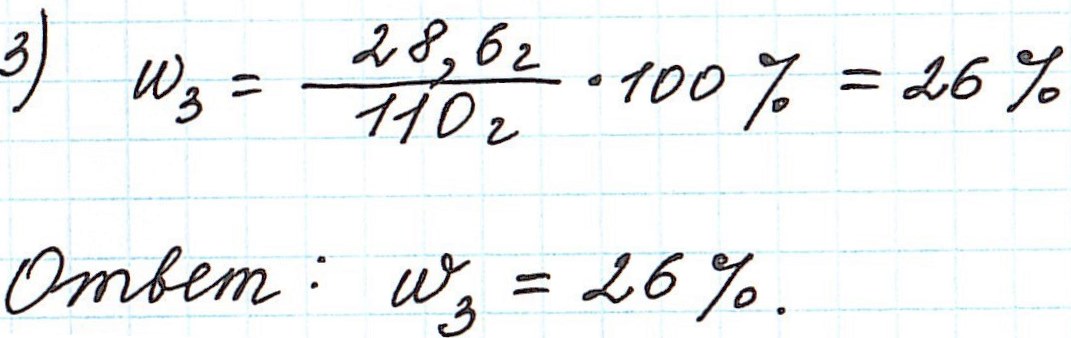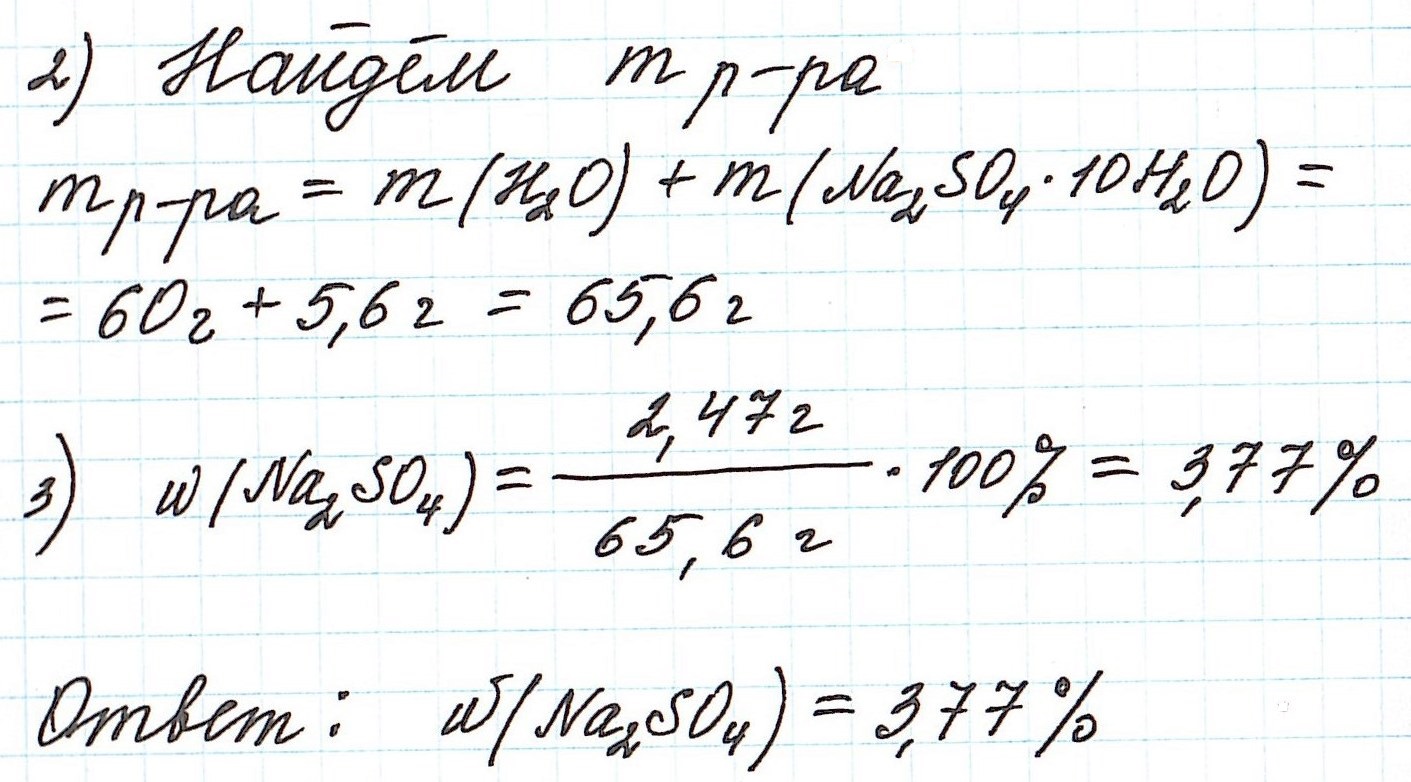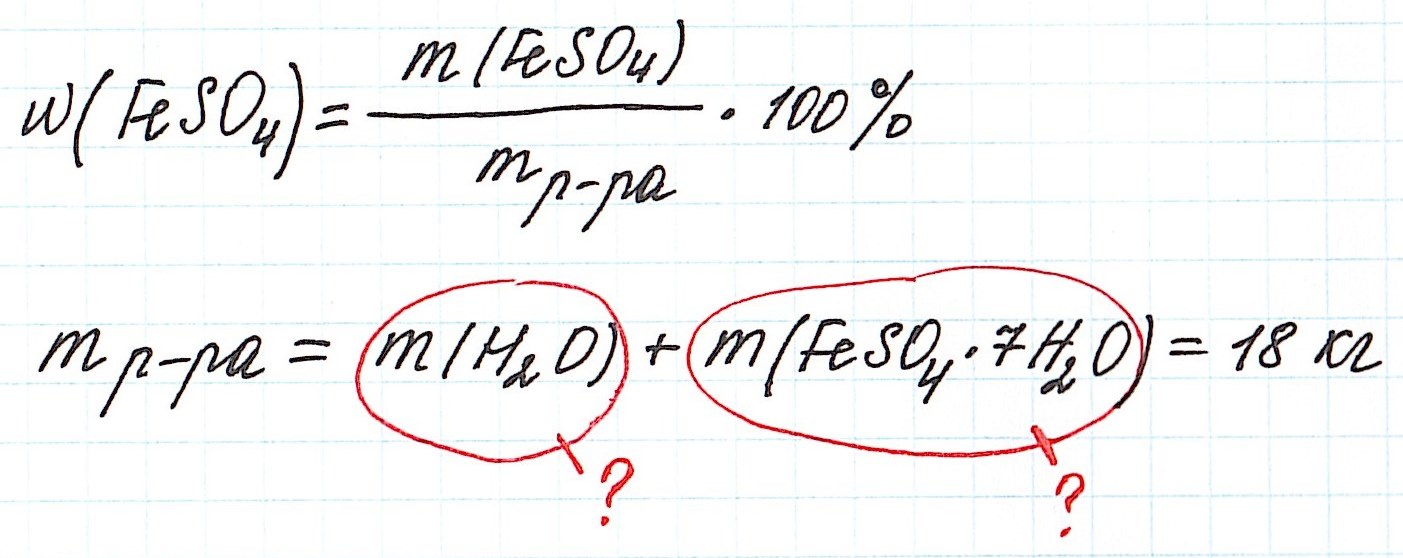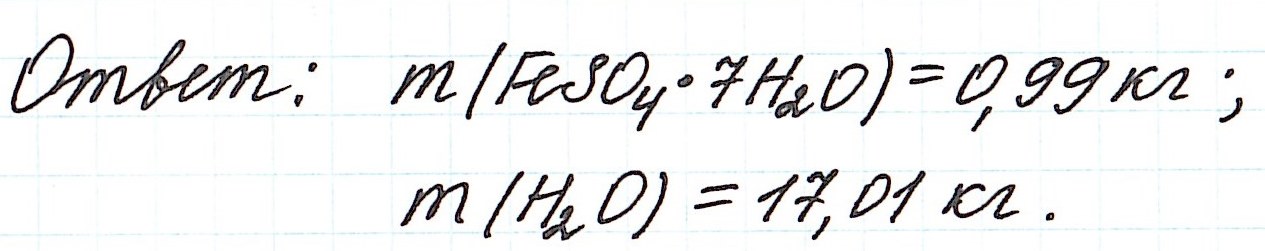- КОНЦЕНТРАЦИЯ РАСТВОРОВ
- СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРА: ПРОЦЕНТНАЯ КОНЦЕНТРАЦИЯ (ИЛИ МАССОВАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА)
- Концентрация – что это такое
- Формула концентрации раствора: основные виды
- Массовая доля растворенного вещества и примеры ее вычисления
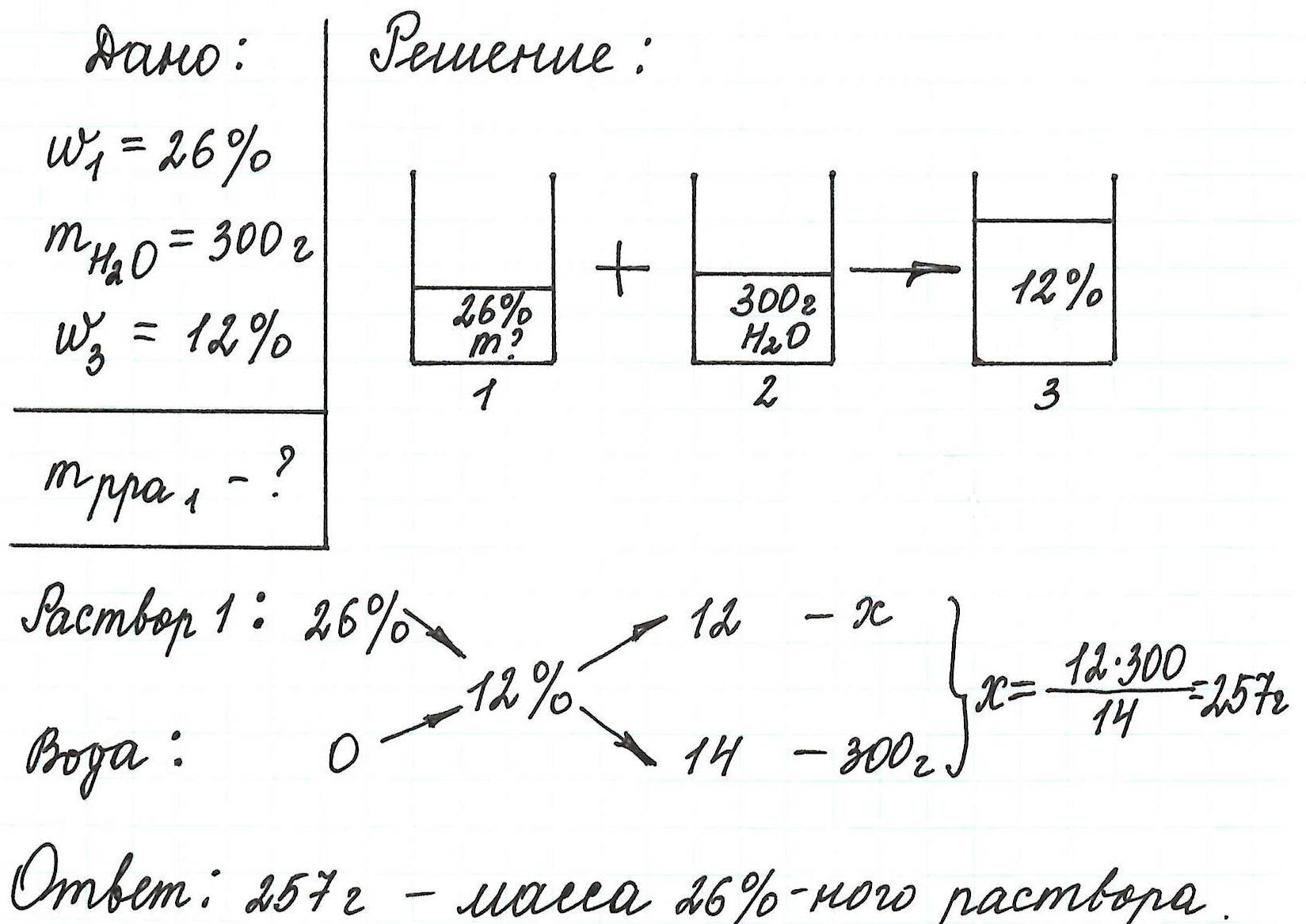
- Вычисление массовой доли растворенного вещества при разбавлении раствора водой
- Вычисление массовой доли растворенного вещества при концентрировании раствора путем упаривания
- Вычисление массовой доли растворенного вещества при концентрировании раствора путем добавления растворенного вещества
- Вычисление массовой доли растворенного вещества при смешивании двух растворов
- Вычисление массовой доли растворенного вещества с применением кристаллогидратов для приготовления раствора
- Правило «креста» в химии растворов как метод решения задач на процентную концентрацию растворов
КОНЦЕНТРАЦИЯ РАСТВОРОВ
Концентрации растворов обычно выражают в массовых (весовых) и объемных (для жидкостей) процентах, в молях или грамм-эквивалентах, содержащихся в единице объема раствора, а также титром и моляльностью.
Концентрации приблизительных растворов большей частью выражают в массовых процентах; точных — в молях, в грамм-эквивалентах, содержащихся в 1 л раствора, или титром.
При выражении концентрации в массовых процентах указывают содержание растворенного вещества (в граммах) в 100 г раствора (но не в 100 мл раствора!).
Так, если говорят, например, что взят 10%-ный раствор поваренной соли NaCl, это значит, что в 100 г раствора (а не в 100 мл его) содержится 10 г поваренной соли и 90 г воды.
Когда дана концентрация раствора, выраженная в массовых процентах (например, 25%-ный раствор NaCl), и хотят взять столько раствора, чтобы в нем содержалось определенное количество растворенного вещества (например, 5 г NaCl), то нужно брать раствор по массе (т. е. 20 г).
Покажем, что будет, если взять не 20 г раствора, а 20 мл. Плотность 25%-ного раствора NaCl равна 1,203 г/мл. Поэтому взяв 20 мл такого раствора, мы возьмем 20*1,203 = 24,06 г его. В этом количестве раствора будет содержаться уже не 5 г NaCl, а

Если известна плотность раствора, то, как указывалось выше, удобнее брать его по объему, а не по массе. Для нашего случая получаем объем, равный:

Сказанное относится преимущественно к концентрированным растворам; в случае же разбавленных (меньше 1%) получающаяся ошибка незначительна и ею можно пренебречь.
Концентрация раствора, выраженная в молях, содержащихся в 1 л раствора (но не в 1 л растворителя!) называется молярностью. Раствор, содержащий в 1 л 1 моль растворенного вещества, называется одномолярным или просто молярным. Молем (грамм-молекулой) какого-либо вещества называют молекулярный вес его, выраженный в граммах; 0,001 моль называют миллимолем, этой величиной пользуются для выражения концентрации при некоторых исследованиях.
Пример. Моль серной кислоты равен 98,08 г, поэтому молярный раствор ее должен содержать это количество в 1 л раствора (но не в 1 л воды).
Если концентрация выражена числом грамм-эквивалентов, содержащихся в 1 л раствора, то такое выражение концентрации называется нормальностью. Раствор, содержащий в 1 л один грамм-эквивалент вещества, называется однонормальным или часто просто нормальным.
Грамм-эквивалентом вещества является такое количество его, выраженное в граммах, которое в данной реакции соединяется, вытесняет или эквивалентно 1,008 г водорода (т. е. 1 г-атом). Грамм-эквивалент одного и того же вещества может иметь различную величину в зависимости от той химической реакции, в которой это вещество участвует.
Грамм-эквивалент E в реакциях замещения вычисляют путем деления молекулярного веса на основность кислоты или полученной из нее соли, кислотность основания или при окислительно-восстановительных реакциях — на число переходящих электронов n:

Ввиду того что нормальные растворы для большийства аналитических целей и работ слишком концентрированы, обычно готовят более разбавленные растворы (полунормальные, децинормальные и т. д.). При записях нормальность обозначают русской буквой н. или латинской буквой N; перед буквенным обозначением ставят число, указывающее, какая часть грамм-эквивалента (или сколько грамм-эквивалентов) взята для приготовления. 1 л раствора. Так, полунормальный раствор обозначается 0,5 н., децинормальный 0,1 н. и т. д.
Титром называют содержание вещества в граммах в 1 мл раствора. Выражая концентрацию раствора при помощи титра, указывают число граммов вещества, содержащихся в 1 мл раствора. Пусть, например, в 1 л раствора содержится 5,843 г серной кислоты; тогда титр раствора будет равен;

Моляльными называют растворы, приготовляемые растворением одного (или части) моля вещества в 1 кг растворителя. Например, для приготовления одномоляль-ного раствора NaCl растворяют 58,457 г этой соли в 1 кг воды, приведя массу воды в данных условиях к объему. Следует помнить, что при приготовлении моляльных растворов расчет ведут именно на 1 кг растворителя, а не раствора, как в случае молярных или нормальных растворов.
Объемные проценты для выражения концентрации применяют только при смешивании взаимно растворяющихся жидкостей. Здесь указаны только основные, важнейшие приемы выражения концентраций. При специальных исследованиях могут применяться и другие единицы для выражения содержания вещества.
Источник
СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРА: ПРОЦЕНТНАЯ КОНЦЕНТРАЦИЯ (ИЛИ МАССОВАЯ ДОЛЯ РАСТВОРЕННОГО ВЕЩЕСТВА)
Формула концентрации раствора. Их множество. И каждая соответствует тому или иному способу выражения концентрации. А в химии их применяются достаточно: массовая доля растворенного вещества, молярная, нормальная, моляльная, титр и др.
А зачем так много? Ответ на этот вопрос очень прост. Каждый вид концентрации удобен в том или ином конкретном случае, тогда как применение другого вида концентрации неуместно.
Например, при исследовании содержания массы вещества в очень небольшом объеме раствора удобно пользоваться титром. А в каких-то технологиях вообще концентрация заменяется другими количественными характеристиками раствора. Так, в технологии посола рыбы для расчета необходимой концентрации тузлука (раствора поваренной соли) используют не его процентную концентрацию, а плотность.
Концентрация – что это такое
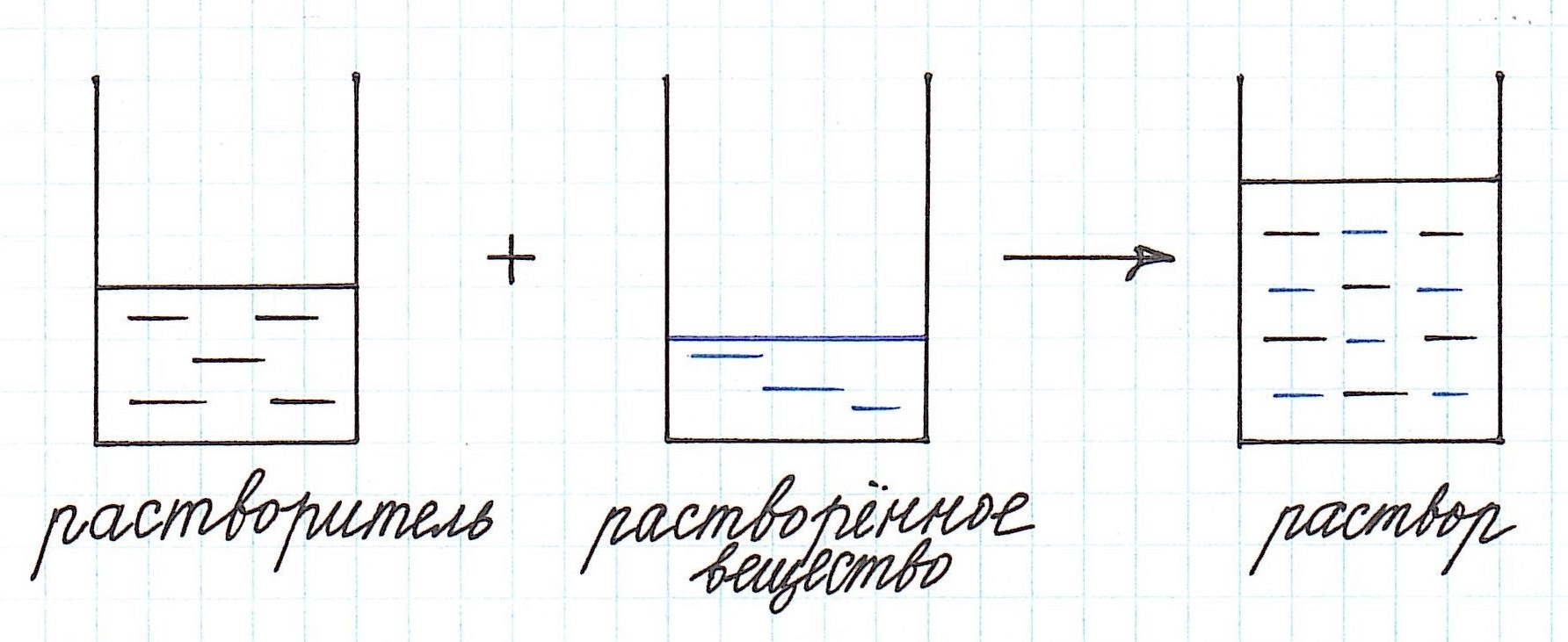
Любой раствор имеет различные характеристики: качественные и количественные. Одной из важнейших количественных характеристик является концентрация раствора.
Концентрация раствора – это количество растворенного вещества, содержащееся в определенном количестве раствора.
Как видно из приведенного определения, основными компонентами раствора являются:
Растворенного вещества в растворе всегда меньше, а растворителя больше.
И вот именно с вычислением количественного содержания растворенного вещества чаще всего и связаны все расчеты, основанные на применении формулы концентрации раствора.
Существует несколько видов концентрации раствора:
— массовая доля растворенного вещества;
— объемная доля растворенного вещества;
— молярная доля растворенного вещества;
— молярная (или молярность);
— моляльная (или моляльность);
— нормальная (или эквивалентная);
Формула концентрации раствора: основные виды
Применение того или иного вида концентрации уместно в каждом конкретном случае. Не существует какой-то универсальной концентрации или универсальной формулы концентрации раствора.
Кстати, с помощью математических преобразований можно перейти от одной концентрации к другой или найти взаимосвязь между разными их видами.
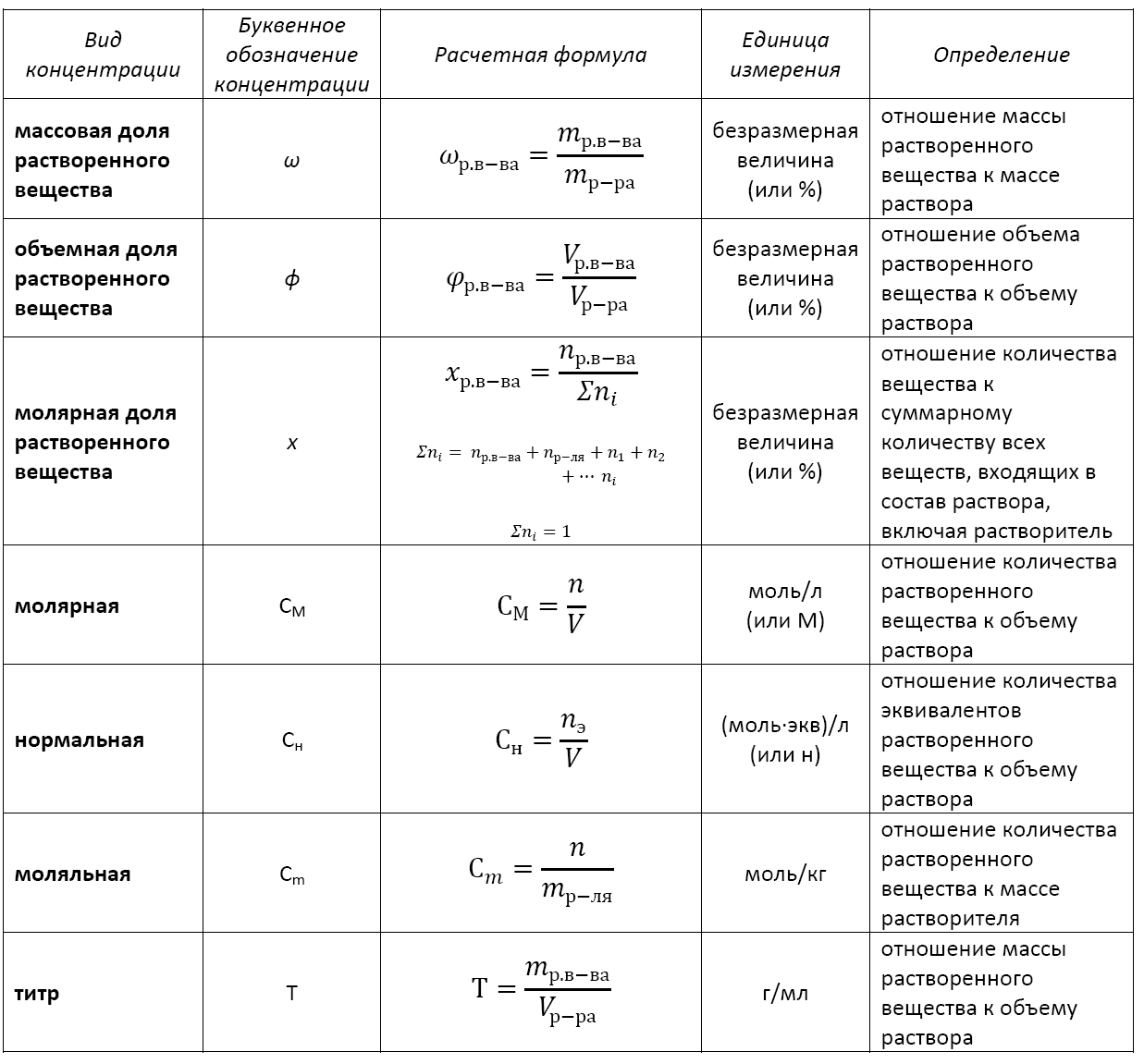
Основные расчетные формулы концентрации раствора приведены в таблице:
Массовая доля растворенного вещества и примеры ее вычисления
Массовая доля растворенного вещества – это отношение массы растворенного вещества к массе раствора.
Ее расчетная формула выглядит так:
где ωр.в-ва – массовая доля растворенного вещества, mр.в-ва – масса растворенного вещества, mр-ра – масса раствора.
ωр.в-ва представляет собой долю или от единицы или от 100%. Так, например, имеется двухпроцентный раствор NaCl. Его концентрация будет записана в первом случае ω(NaCl) = 0,02, а во втором – ω(NaCl) = 2%. Форма записи основной сути не меняет. Можно записывать и так, и так.
Что же означает выражение ω(NaCl) = 0,02 или ω(NaCl) = 2%? Буквально следующее: в 100 г водного раствора поваренной соли содержится 2 г этой соли и 98 г воды.
Необходимо помнить, что раствор состоит из растворителя и растворенного вещества . Поэтому масса раствора будет состоять из массы растворителя и массы растворенного вещества:
Тогда основную расчетную формулу для массовой доли растворенного вещества можно преобразовать:
Очень часто в расчетах с процентной концентрацией используются плотность и объем раствора:
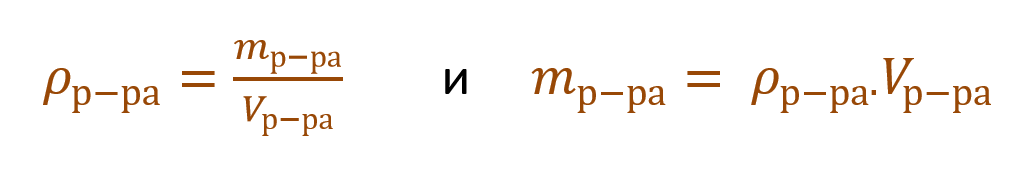
В других ситуациях могут использоваться объем и плотность не раствора, а растворителя. Тогда основная формула для расчета концентрации будет выглядеть так:
На практике бывает необходимо не только приготовить раствор с какой-либо определенной концентрацией, но и увеличить, либо уменьшить ее значение. Это достигается различными приемами:
— добавлением растворенного вещества;
— добавлением к раствору растворителя (например, воды).
Кроме того, приходится часто смешивать друг с другом растворы разных концентраций.
Разберем все возможные случаи.
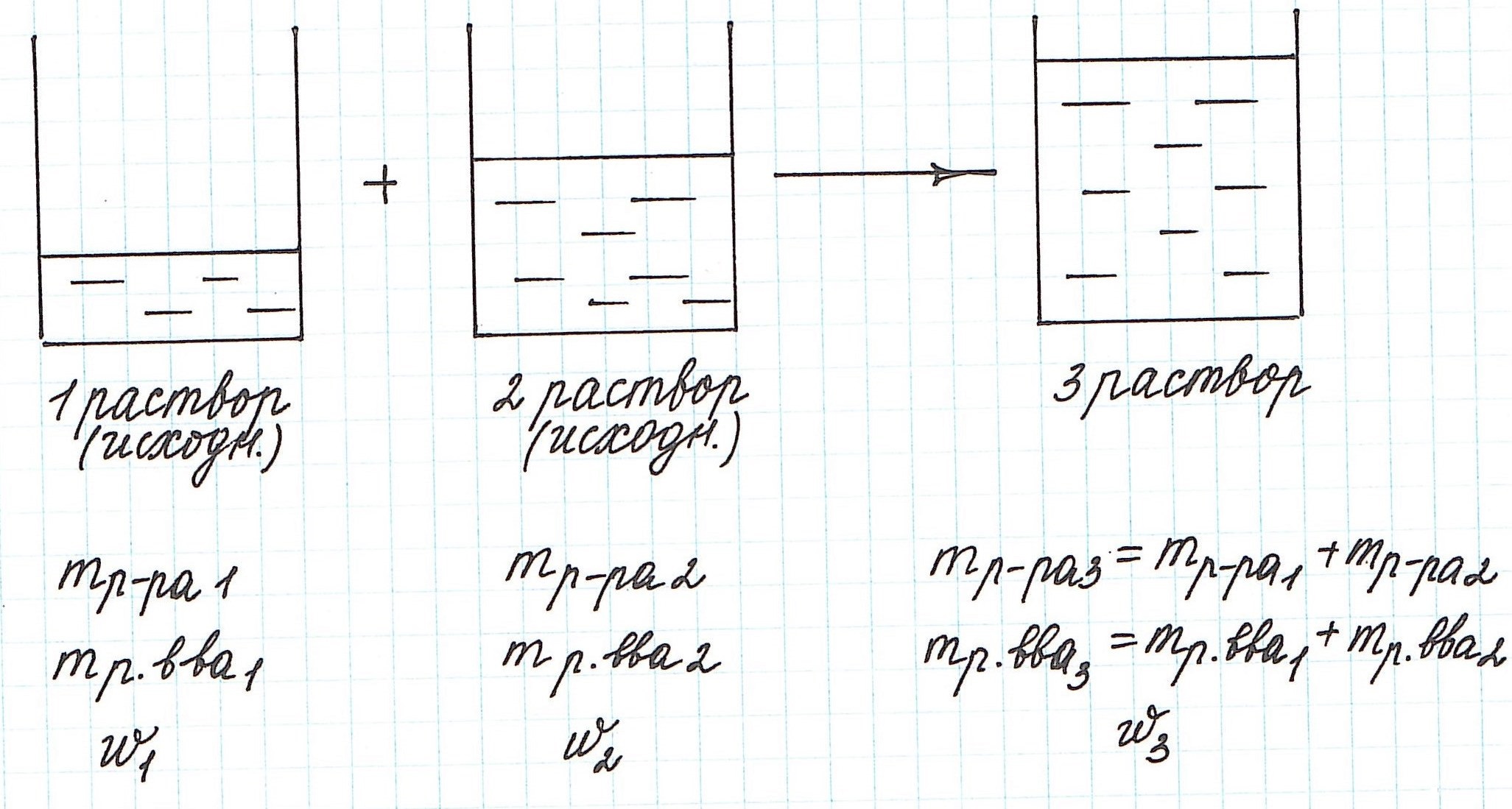
Мы рекомендуем задачи, в которых речь идет о растворах, решать с использованием схематических рисунков. Это очень наглядно, особенно, когда речь идет о смешивании растворов.
Начнем с самого простого: вычислим концентрацию раствора.
Пример 1. В 200 г воды растворили 40 г глюкозы. Вычислите массовую долю глюкозы в полученном растворе.
Обратите внимание, что речи о каком-либо химическом взаимодействии не идет! Поэтому записывать уравнения реакций не требуется!
Запишем общую формулу для расчета массовой доли растворенного вещества:
В данной задаче глюкоза (C6H12O6) – растворенное вещество, а вода (H2O) – растворитель. Масса раствора будет складываться из массы глюкозы и массы воды:
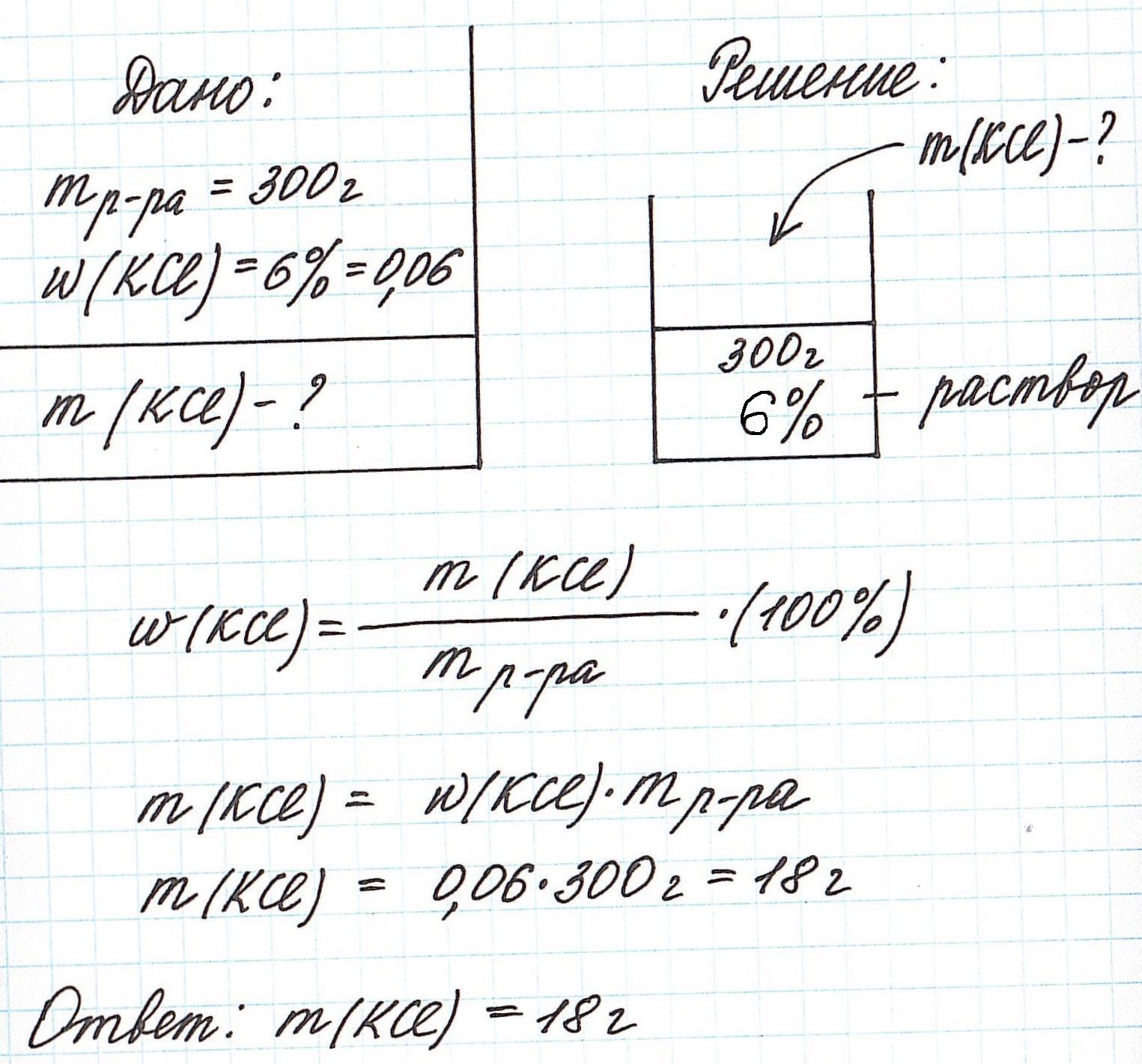
Пример 2. Рассчитайте, сколько потребуется хлорида калия, чтобы приготовить 300 г раствора с массовой долей соли 6%.
Обратите внимание, для того, чтобы расчеты были менее громоздкими, будем использовать выражение концентрации не в %, а в долях от единицы.
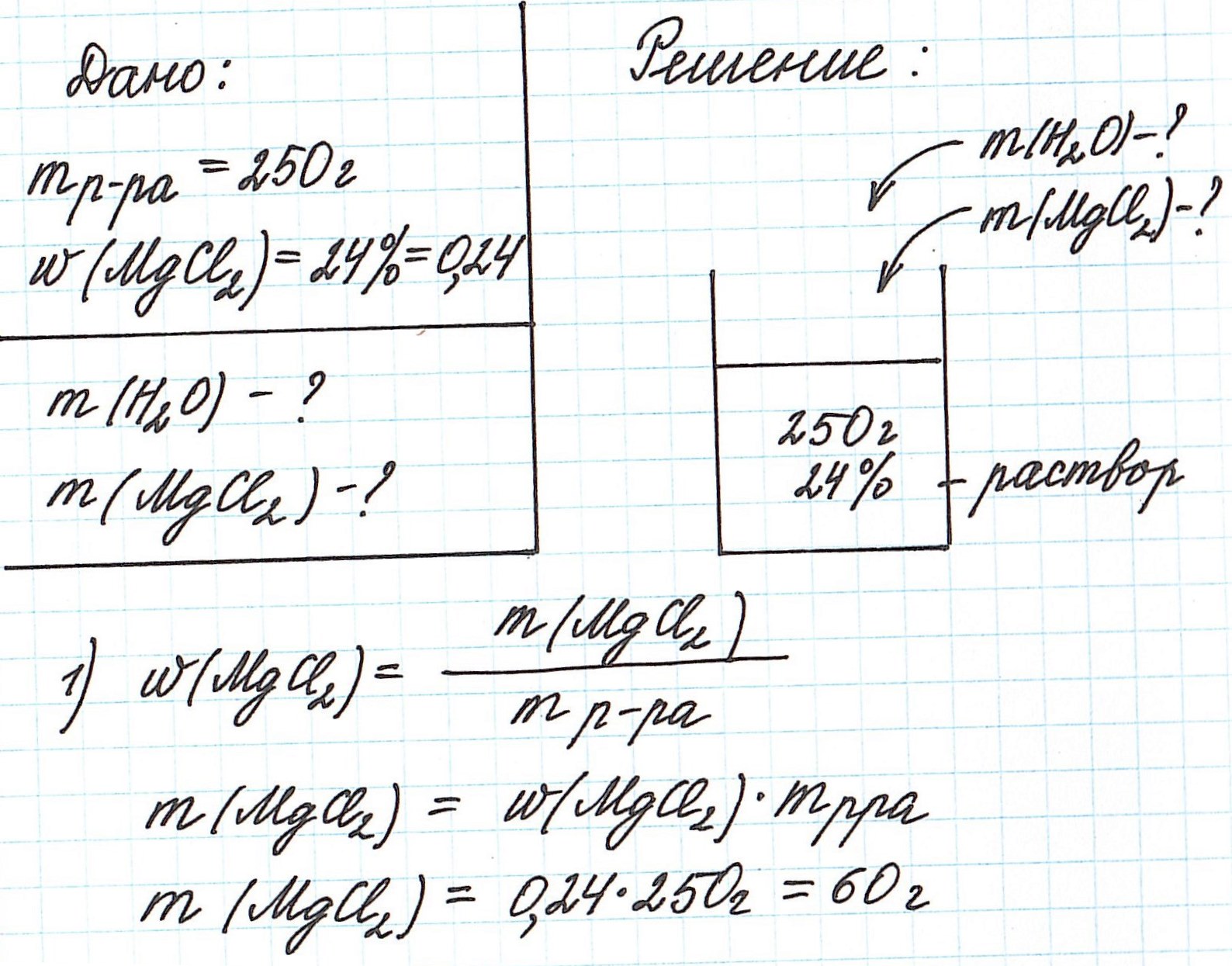
Пример 3. Необходимо приготовить 250 г раствора с массовой долей хлорида магния 24%. Рассчитайте массу требуемых воды и соли.
Так как раствор готовится из хлорида магния и воды, то и масса раствора равна сумме масс хлорида магния и воды:
Рассмотрим задачу, в которой в качестве растворителя выступает не вода, а другое вещество.
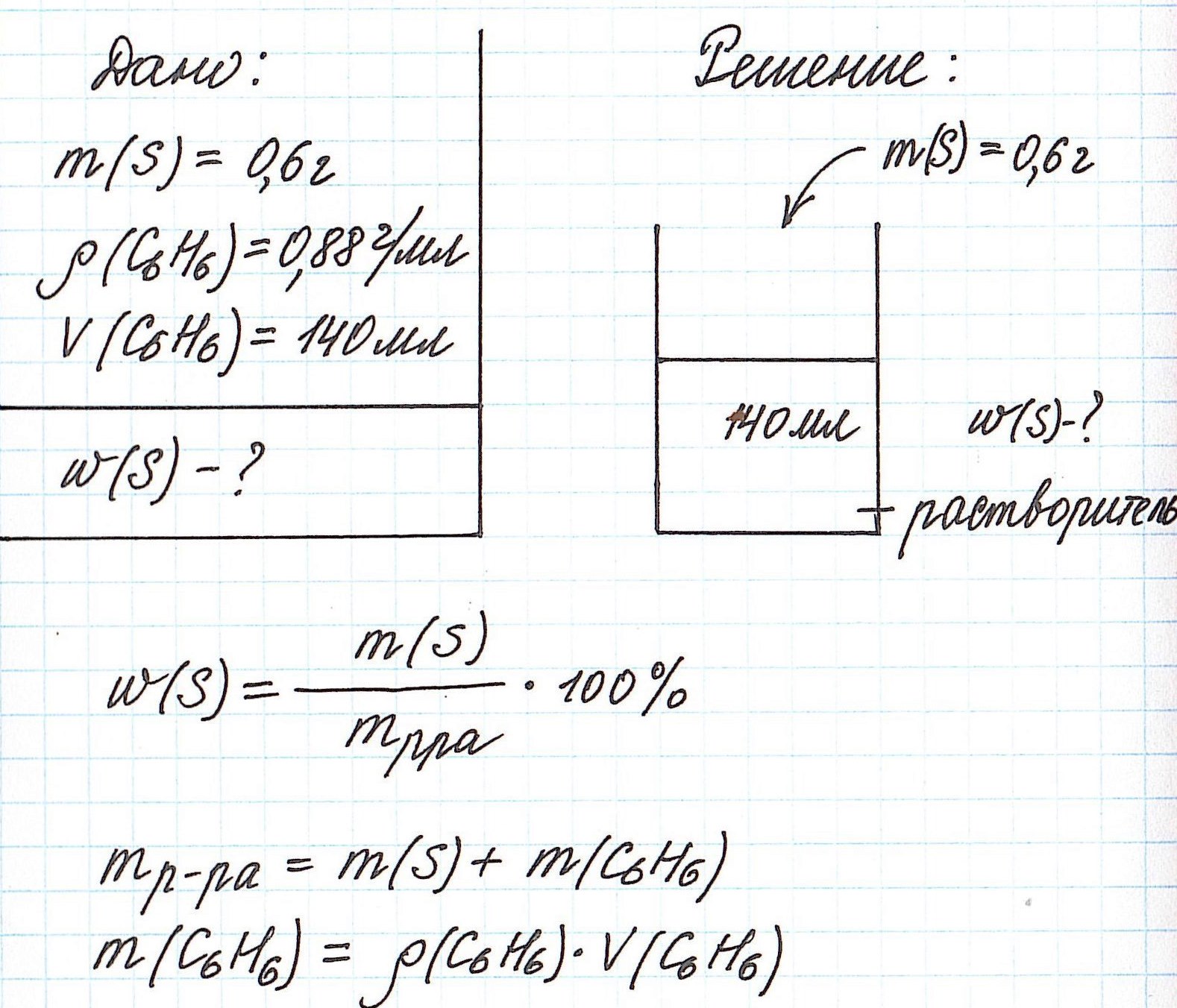
Пример 4. В органическом растворителе бензоле объемом 140 мл растворили серу массой 0,6 г. Вычислите массовую долю серы в полученном растворе, если плотность бензола составляет 0,88 г/мл.
Обратите внимание, что здесь:
— масса раствора не известна;
— масса растворителя (бензола) не известна;
— известны объем и плотность растворителя (бензола), что позволяет нам найти его массу;
— масса раствора состоит из массы растворителя (бензол) и массы растворенного вещества (сера).
Объединим все расчетные формулы в одну и подставим в нее имеющиеся численные значения:
Вычисление массовой доли растворенного вещества при разбавлении раствора водой
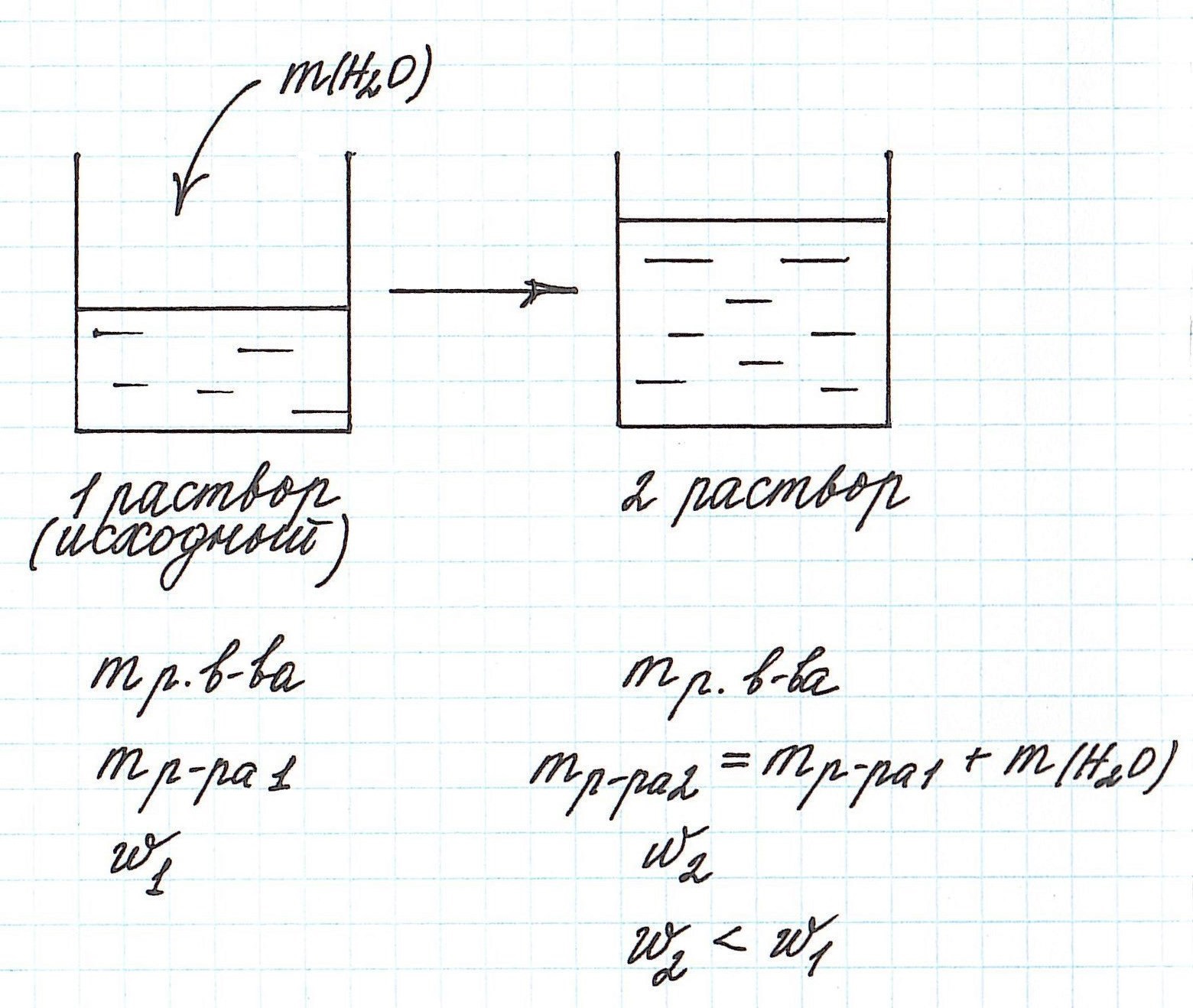
Разбавление раствора водой приводит к уменьшению его концентрации.
Запомним, что в таких случаях:
— увеличивается масса раствора;
— увеличивается масса растворителя;
— масса растворенного вещества остается постоянной.
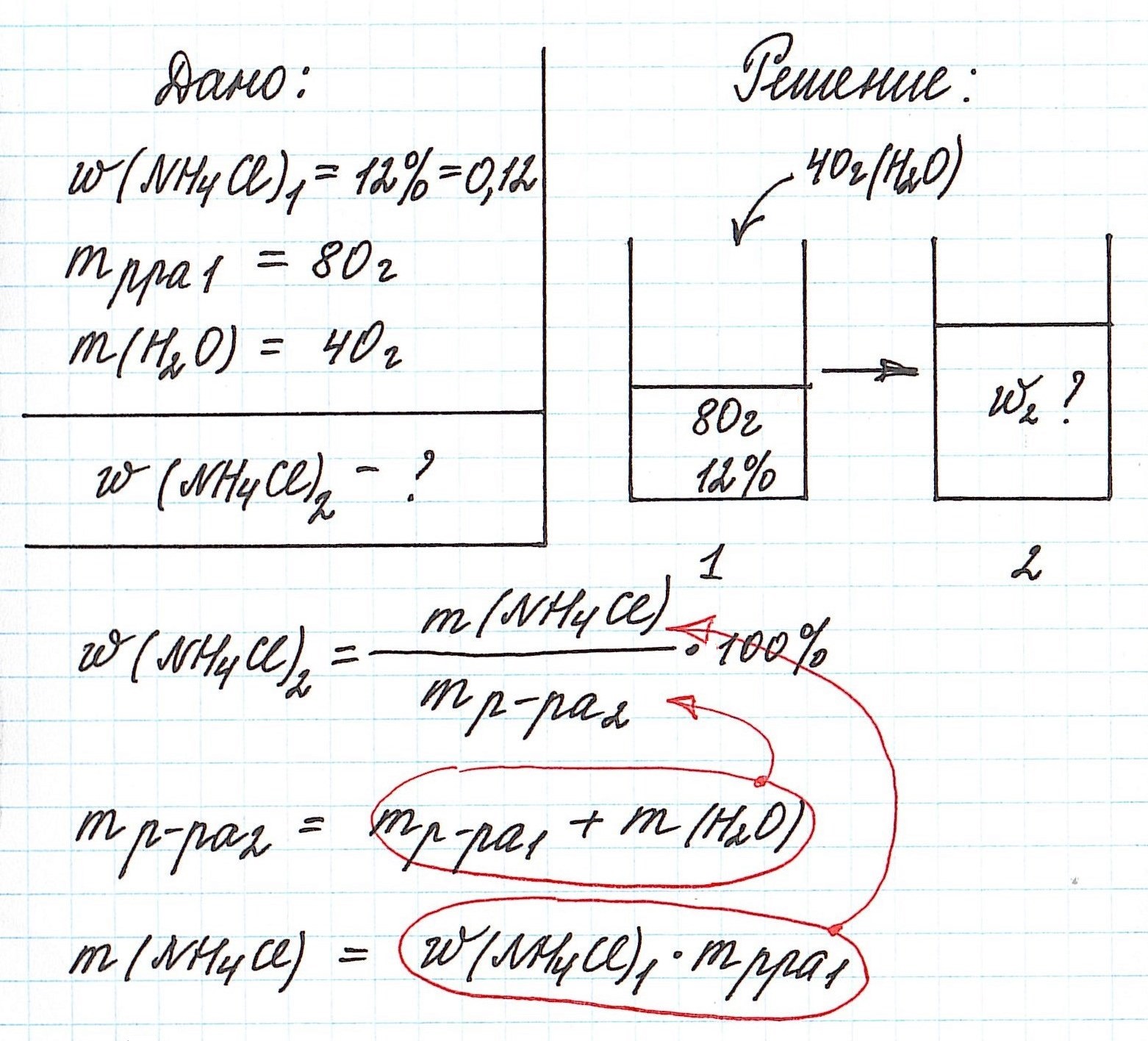
Пример 5. К 80 г раствора с массовой долей NH4Cl 12% добавили 40 г воды. Вычислите массовую долю хлорида аммония в полученном растворе.
Объединим все полученные формулы в одну и подставим имеющиеся данные:
Пример 6. Рассчитайте объем раствора фосфорной кислоты (массовая доля кислоты 12%, плотность 1,065 г/мл), который потребуется для приготовления раствора с массовой долей H3РO4 4% объемом 250 мл (плотность 1,02 г/мл).
В данной задаче речь напрямую о разбавлении раствора не идет. Но судя по тому, что исходный раствор имел концентрацию 12%, а конечный – 4%, становится ясно: последний раствор можно получить путем разбавления первого водой.
Вычисление массовой доли растворенного вещества при концентрировании раствора путем упаривания
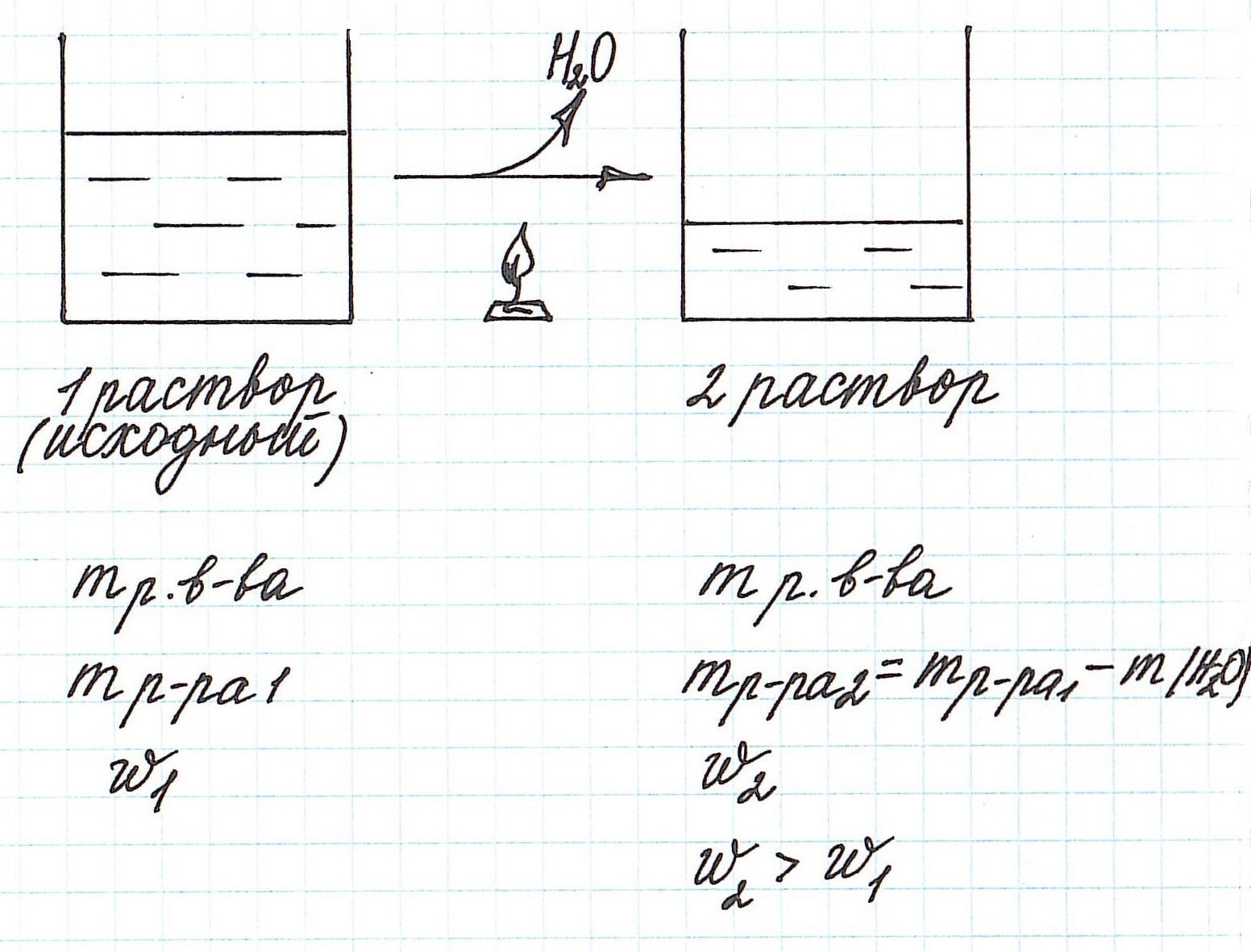
Упаривание раствора, т.е. его нагревание, при котором происходит испарение воды, приводит к увеличению концентрации.
Учтите, что при этом:
— уменьшается масса раствора;
— уменьшается масса растворителя;
— масса растворенного вещества остается постоянной (при условии, что растворенное вещество не разлагается при данной температуре).
Пример 7. Из 200 г 27%-ного раствора глюкозы выпарили 20 г воды. Определите массовую долю глюкозы в полученном растворе.
Вычисление массовой доли растворенного вещества при концентрировании раствора путем добавления растворенного вещества
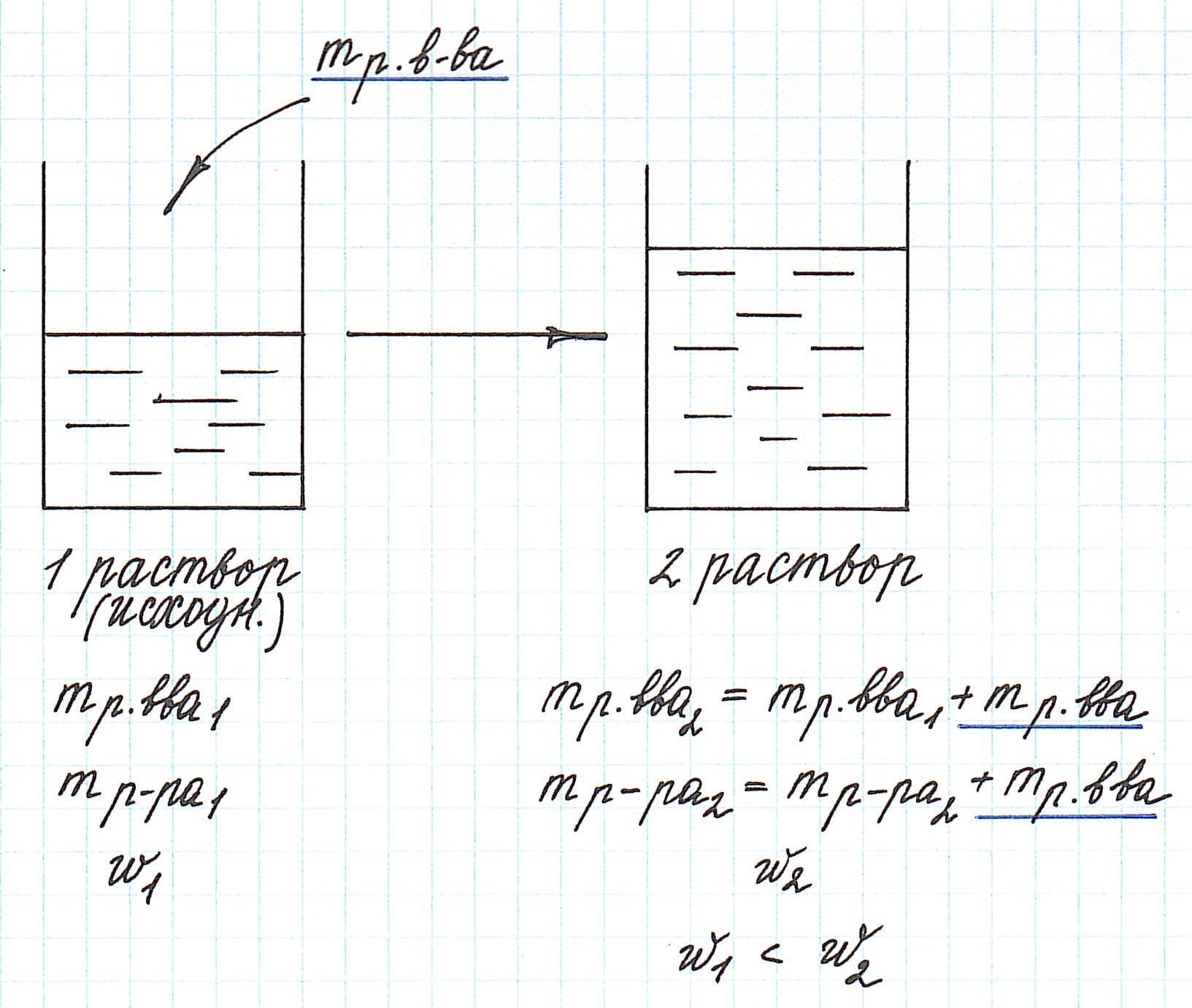
Добавление к уже существующему раствору новой порции растворенного вещества приводит к увеличению концентрации раствора.
Помните, что в таких случаях:
— увеличивается масса раствора;
— увеличивается масса растворенного вещества.
Пример 8. Определите массу хлорида калия, который надо добавить к 180 г 15%-ного раствора этой соли, чтобы получить 20%-ный раствор.
Вычисление массовой доли растворенного вещества при смешивании двух растворов
При смешивании двух растворов (речь о растворах одного и того же вещества конечно же) изменяются все количественные характеристики:
— увеличивается масса раствора;
— увеличивается масса растворенного вещества;
— изменяется массовая доля растворенного вещества.
Пример 9. Смешали 80 г 32%-ного раствора и 30 г 10%-ного раствора нитрата меди (II). Какова концентрация соли в полученном растворе?
Вычисление массовой доли растворенного вещества с применением кристаллогидратов для приготовления раствора
Кристаллогидраты используются для приготовления растворов довольно часто. Кристаллогидраты представляют собой вещества, в состав которых помимо основного вещества входят молекулы воды. Например:
CuSO4·5H2O – кристаллогидрат сульфата меди (II) (или медный купорос);
Na2SO4·10H2O – кристаллогидрат сульфата натрия (или глауберова соль).
Вода, входящая в состав кристаллогидрата, называется кристаллизационной .
Кристаллогидраты различаются прочностью связи между основным веществом и кристаллизационной водой. Одни из них теряют воду при комнатной температуре с течением времени и перестают быть кристаллогидратами (например, Na2СO3·10H2O). Другие – обезвоживаются только при сильном нагревании (например, CuSO4·5H2O).
При расчете концентрации с использованием кристаллогидратов для получения растворов часто приходится учитывать и кристаллизационную воду.
Но сначала поясним некоторые нюансы на конкретном примере:
1) Формула CuSO4·5H2O означает, что 1 моль CuSO4·5H2O содержит 1 моль CuSO4 и 5 моль H2O. Это можно было бы записать так:
2) Относительная молекулярная (и численно молярная) масса будет складываться из относительной молекулярной массы вещества и относительной молекулярной массы воды. Например:
Mr(CuSO4·5H2O) = Mr(CuSO4) + 5·Mr(H2O) = 160 + 5·18 = 250 и, соответственно,
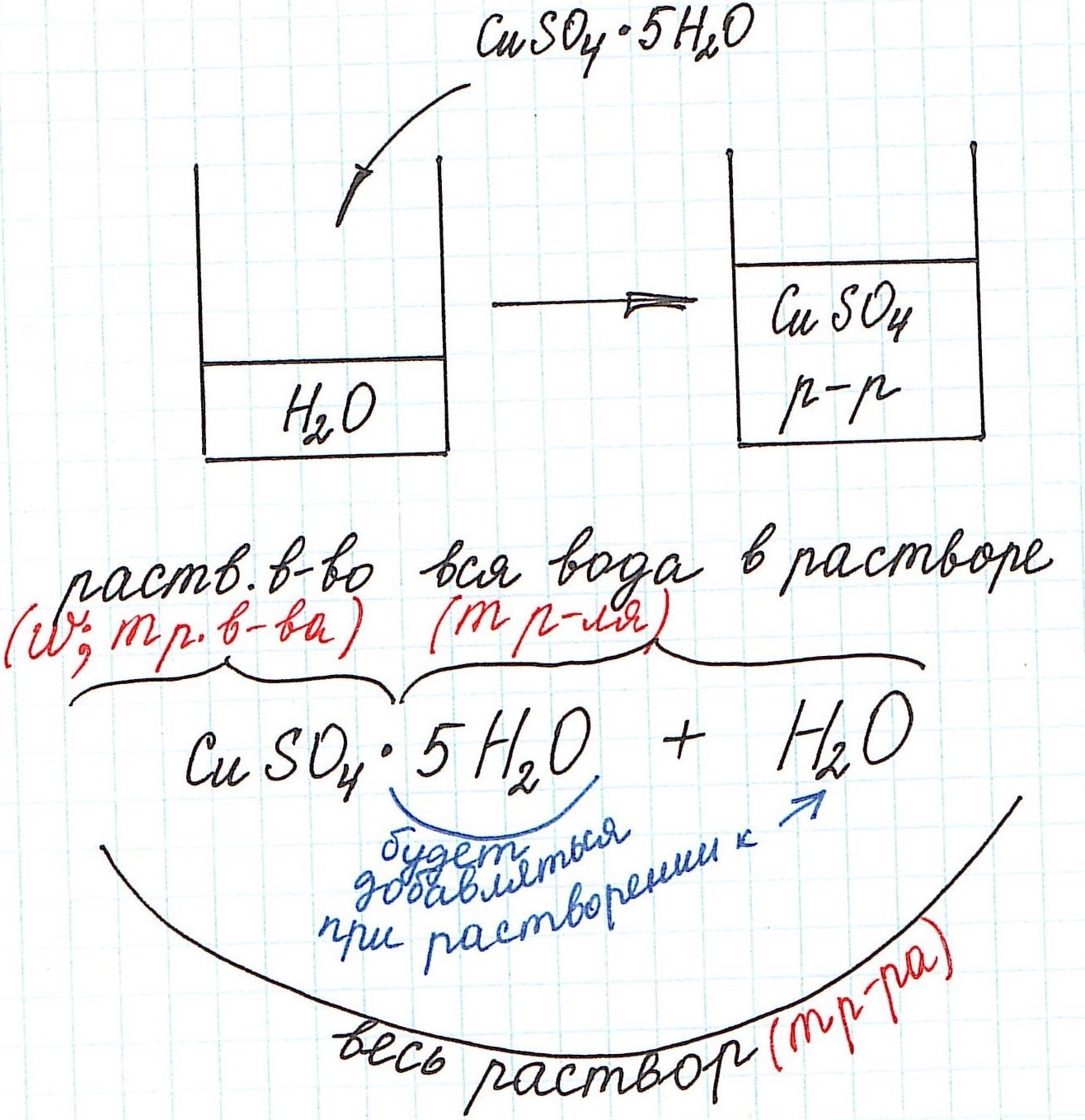
3) Еще одну особенность поясним с помощью рисунка:
Итак, разберем несколько типичных задач.
Пример 10. В 60 г воды растворили глауберову соль Na2SO4·10H2O массой 5,6 г. Какова массовая доля сульфата натрия в полученном растворе?
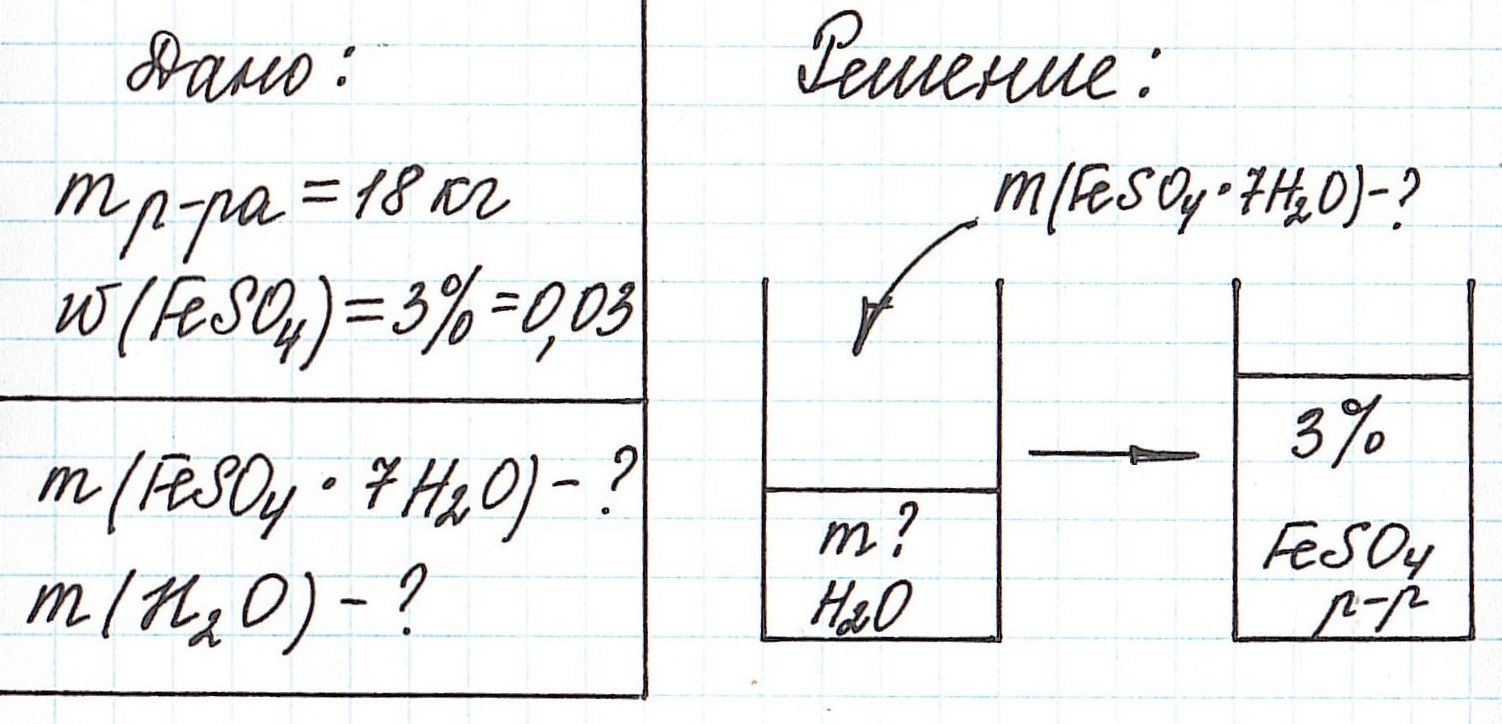
Пример 11. Какая масса железного купороса FeSO4·7H2O и воды потребуется для приготовления 18 кг раствора сульфата железа (II) с массовой долей FeSO4 3%?
Обратите внимание, что масса раствора дана не в граммах (г), а в килограммах (кг). Для того, чтобы привести в ходе расчетов все единицы измерения к единой системе, можно перевести килограммы в граммы и вычислять как обычно.
Но есть более простой способ. Можно считать количество вещества не в моль, а в киломоль (кмоль). Молярную массу вычислять не в г/моль, а в кг/кмоль. В этом случае ответ в задаче мы сразу получим в килограммах.
Пример 12. Вычислите массу кристаллогидрата сульфата никеля NiSO4·7H2O, который надо добавить к 180 г раствора с массовой долей сульфата никеля 1,5%, чтобы получить раствор с массовой долей соли 6%?
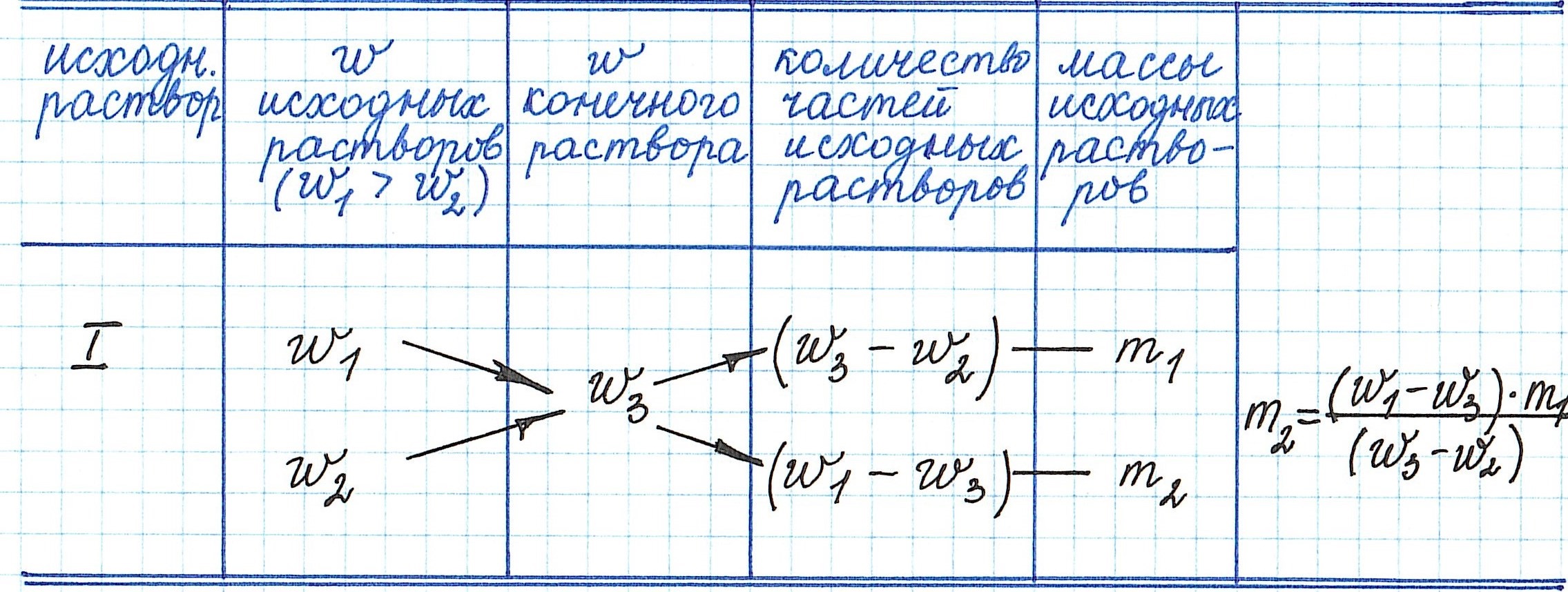
Правило «креста» в химии растворов как метод решения задач на процентную концентрацию растворов
Правилом «креста» (или «квадратом Пирсона») очень удобно пользоваться в расчетах, связанных с разбавлением или смешиванием растворов.
Общая схема вычислений выглядит так:
Пример 13. Какую массу 5%-ного раствора глюкозы надо добавить к 70 г 21%-ного раствора этого же вещества, чтобы получить 12%-ный раствор?
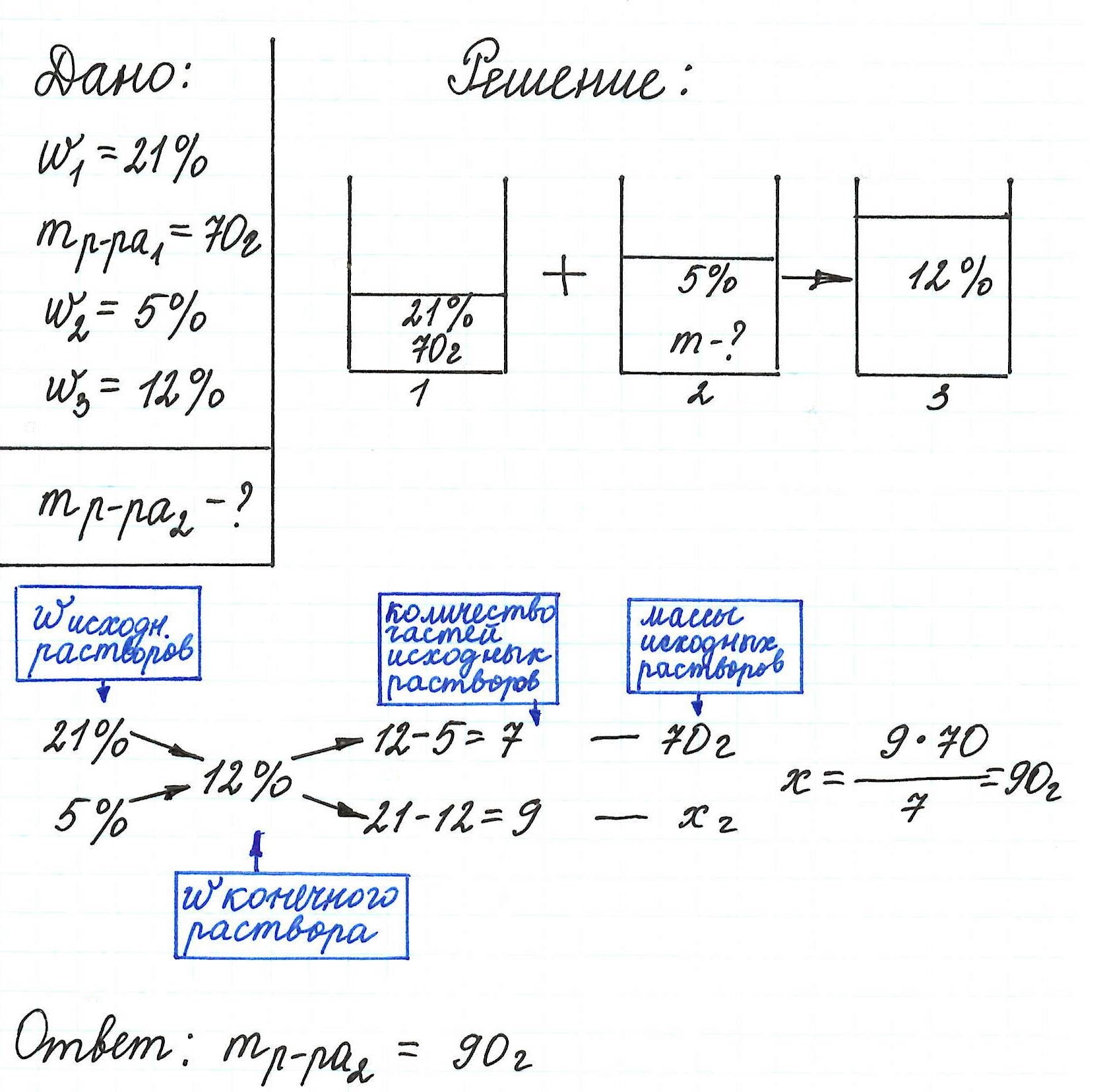
Еще примеры с применением правила «креста» можно посмотреть здесь.
Мы рассмотрели достаточно примеров расчетов, где используется формула такой концентрации раствора как массовая доля растворенного вещества. Как видим, ситуаций, в которых требуется ее применение, множество. Однако, есть достаточно случаев, когда более приемлемыми являются формулы других концентраций (молярной, нормальной, титра и т.д.). Об этом читайте в других статьях.
Источник