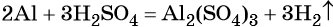- Почему протекают химические реакции?
- Основные понятия химической термодинамики
- Основы термохимии
- Энтропия. Направление химических процессов. Энергия Гиббса
- Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Сохранение массы веществ при химических реакциях
- Тренировочные задания
Почему протекают химические реакции?
Основные понятия химической термодинамики
Химические процессы могут протекать с изменением химического состава вещества (химические реакции) и без его изменения (фазовые переходы). Совокупность веществ, находящихся во взаимодействии и выделенных из окружающего пространства (мысленно) называется системой. Например: атом водорода (система из ядра и электрона), водный раствор различных солей и т.д.
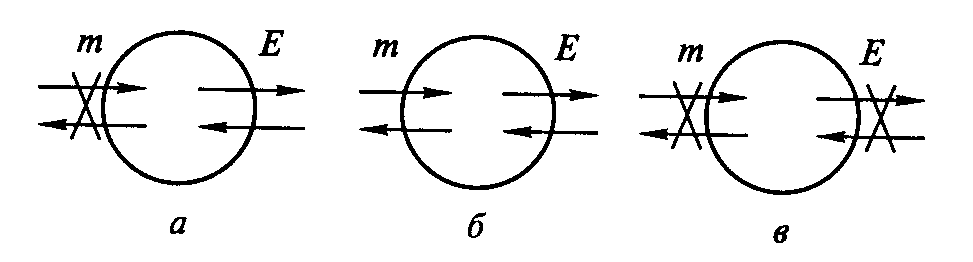
В зависимости от характера взаимодействия системы с окружающей средой различают: открытые или незамкнутые (происходит обмен теплом, энергией и веществом с окружающей средой), закрытые или замкнутые (происходит обмен теплом и энергией с окружающей средой, но нет обмена веществом) и изолированные (отсутствие массо- и теплопереноса между системой и окружающей средой) (рис. 1).
Рис. 1. Примеры закрытой (а), открытой (б) и изолированной систем (в).
Состояние системы определяется совокупностью ее свойств и характеризуется термодинамическими параметрами температурой, давлением и объемом (T, p, V). Любое изменение одного или нескольких параметров системы называется термодинамическим процессом. Так, повышение температуры приводит к изменению внутренней энергии системы (U).
Нельзя рассчитать или измерить абсолютное значение U. Возможно определить изменение внутренней энергии (ΔU) в результате какого-либо процесса. ΔU любой системы при переходе из одного состояния в другое не зависит от пути перехода, а определяется начальным и конечным положениями системы. Это означает, что внутренняя энергия системы — функция состояния.
Где 1 и 2 – символы начального и конечного состояния системы.
Первое начало термодинамики: сообщенное системе тепло Q расходуется на приращение внутренней энергии и на совершение работы (А) против внешних сил:
Следует отметить, что А и Q не являются функциями состояния, т.е. не зависят от пути протекания процесса.
В термодинамике нередко вводят величины, которые тождественны сумме нескольких термодинамических параметров. Такая замена существенно облегчает расчеты. Так, функцию состояния, равную U + pV, называют энтальпией (Н):
При постоянном давлении (изобарный процесс) и в отсутствии других работ, кроме работы расширения, теплота равна изменению энтальпии:
Qp = ΔU + pΔV = ΔH
Если процесс идет при постоянном объеме (изохорный) и в отсутствие других работ, выделившаяся или поглотившаяся теплота соответствует изменению внутренней энергии:
Основы термохимии
Раздел химической термодинамики, изучающий теплоты химических реакций и их зависимость от различных физико-химических параметров, называют термохимией. В термохимии пользуются термохимическими уравнениями реакций, в которых указывают агрегатное состояние вещества, а тепловой эффект реакции рассматривается как один из продуктов. Например:
Что означает, что при образовании 1 моль воды в газообразном состоянии выделяется 242 кДж тепла. При этом изменение энтальпии ΔH = − 242 кДж.
Противоположные знаки Q и ΔH свидетельствуют о том, что в первом случае – это характеристика процессов в окружающей среде, а во втором – в системе. При экзотермическом процессе Q > 0, ΔH 0 f. Так, например, ΔH 0 f (CO2) из С(s) и O2(g ) будет равен −393,51 кДж.
2) Стандартные теплоты образования простых веществ равны нулю.
3) Стандартный тепловой эффект химической реакции (ΔH 0 ) равен разности между суммой теплот образования продуктов реакции (с учетом стехиометрических коэффициентов) и суммой теплот образования исходных веществ (с учетом стехиометрических коэффициентов):
ΔH 0 = Σ ΔH 0 f (продукты) − Σ ΔH 0 f (реагенты)
Например, для реакции:
4) Тепловой эффект химической реакции равен разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов реакции с учетом стехиометрических коэффициентов
5) С термохимическими уравнениями можно производить все алгебраические действия, например:
A= B + C + 400 кДж
B + D = A − 200 кДж
Сложив эти уравнения получим
A + B + D = B + C + A + 200 кДж
Энтропия. Направление химических процессов. Энергия Гиббса
Например, при испарении воды в условиях кипения (Т =373 К, р=1 атм) изменение энтропии равно ΔS = ΔHисп/373 = 44000/373 = 118 кДж/(моль × К).
На основании о стандартной энтропии веществ (S 0 ) можно рассчитать изменение энтропии различный процессов:
где i – продукты реакции, j – исходные вещества.
Энтропия простых веществ не равна нулю.
Рассчитав ΔrS 0 и ΔrH 0 можно сделать вывод об обратимости реакции. Так, если ΔrS 0 и Δ rH 0 больше нуля или ΔrS 0 и ΔrH 0 меньше нуля, то реакция носит обратимый характер.
Существует функция, которая связывает изменение энтальпии и энтропии и отвечает на вопрос о самопроизвольности протекания реакции – энергия Гиббса (G).
О направлении протекания химической реакции судят по величине ΔrG 0 . Если ΔrG 0 0 > 0 – в обратном. С наибольшей вероятностью из 2х реакций будет протекать та, у которой меньше значение Δ rG 0 .
Таблица 1. Условия самопроизвольности протекания химических реакций
Возможность самопроизвольного протекания реакции
Источник
Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Сохранение массы веществ при химических реакциях
Химической реакцией называют взаимодействия, приводящие к изменению химической природы участвующих в них частиц. При этом происходит изменение их состава и (или) строения. В химических реакциях могут участвовать атомы, молекулы, ионы и радикалы.
В ходе химических реакций атомные ядра не затрагиваются и число атомов каждого химического элемента сохраняется.
Химические реакции протекают при определённых условиях (температура, давление, наличие или отсутствие растворителя, катализа, ультрафиолетовое излучение).
Признаками протекания химических реакций являются выделение или поглощение газа, образование или растворение осадка, изменение цвета, выделение или поглощение теплоты.
Описание качественных реакций, используемых для определения некоторых катионов и анионов, приводится в приложении в конце урока.
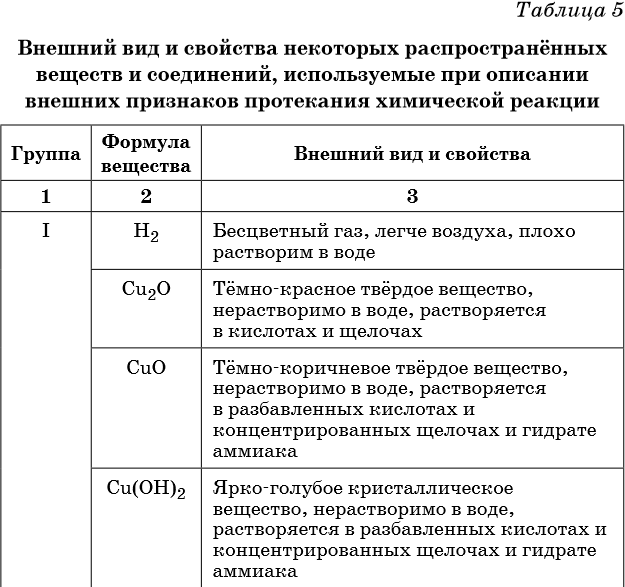
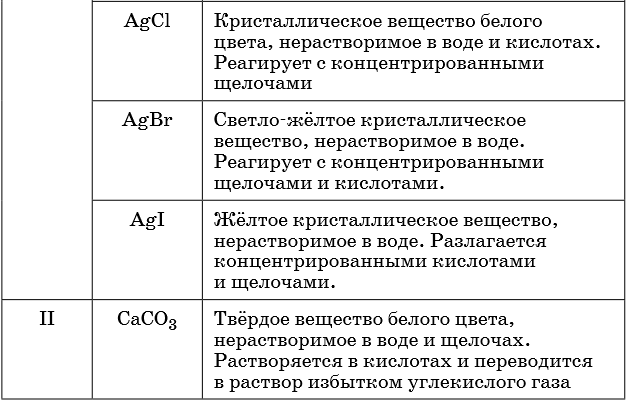
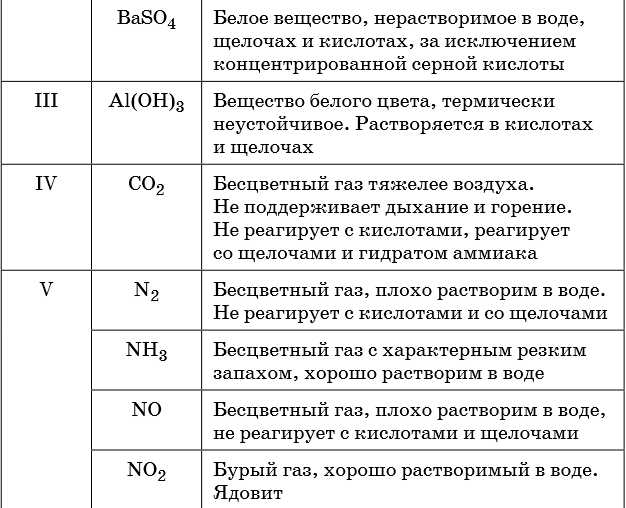
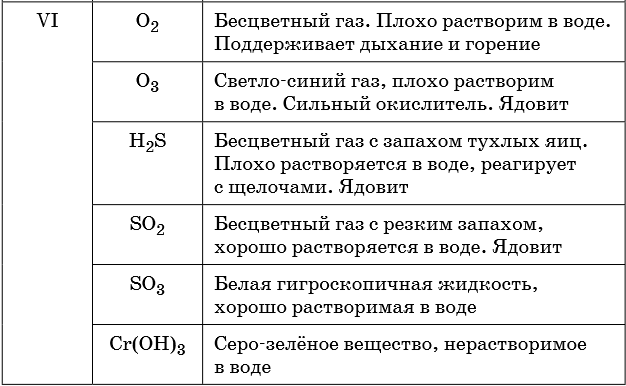
В таблице 5 представлены сведения о внешнем виде и свойствах некоторых распространённых веществ и соединений, используемых при описании внешних признаков протекания химической реакции.
Для описания химических реакций используют химические уравнения, в левой части которых указывают исходные вещества, а в правой — продукты реакции. Обе части химического уравнения соединяют стрелкой (в случае необратимых химических превращений), а если химическая реакция является обратимой, то это показывают с помощью прямой и обратной стрелок.
В неорганической химии, если количество атомов химических элементов в левой и правой частях уравнено с помощью стехиометрических коэффициентов, части уравнения часто соединяют знаком равенства.
Стехиометрией называют учение о количественных соотношениях между реагентами и продуктами реакции.
Коэффициенты стехиометрические — действительные натуральные (то есть положительные, как правило, целые) числа, стоящие перед формулой химического вещества в уравнении реакции. Коэффициенты показывают минимальное количество структурных единиц вещества (атомов, молекул, ионов, радикалов), участвующих в данной реакции.
В вышеприведённой реакции два атома алюминия реагируют с тремя молекулами серной кислоты, в результате чего образуется одна молекула сульфата алюминия (коэффициент, равный одному, перед формулой не ставят) и три молекулы водорода.
В соответствии с законом сохранения массы (закон Ломоносова — Лавуазье) масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции.
Этот закон подтверждает, что атомы являются неделимыми и в ходе химических реакций не изменяются. Молекулы при реакциях претерпевают изменения, но общее число атомов каждого вида не изменяется, и поэтому общая масса веществ в процессе реакции сохраняется.
Тренировочные задания
1. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) растворение осадка
2) выделение чёрного осадка
3) отсутствие внешних признаков
4) выделение синего осадка
2. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение жёлтого осадка
2) растворение осадка
3) выделение белого осадка
4) выделение синего осадка
3. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) отсутствие внешних признаков
2) выделение жёлто-зелёного газа
3) выделение жёлтого осадка
4) растворение осадка
4. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) появление оранжевой окраски
2) выделение газа с характерным запахом
3) растворение осадка
4) отсутствие внешних признаков
5. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение жёлтого осадка
2) отсутствие внешних признаков
3) выделение белого осадка
4) выделение чёрного осадка
6. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ВЕЩЕСТВА:
А) AgNO3 и NaI
Б) Zn и KOH
В) HCl и FeS
ПРИЗНАКИ РЕАКЦИИ:
1) выделение жёлтого осадка
2) выделение газа с характерным запахом
3) выделение бесцветного газа
4) выделение чёрного осадка
7. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) отсутствие внешних признаков
2) выделение газа с характерным запахом
3) выделение белого осадка
4) растворение осадка
8. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение синего осадка
9. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение синего осадка
2) растворение осадка
3) выделение белого осадка
4) выделение бурого осадка
10. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ВЕЩЕСТВА:
А) AgNO3 и NaI
Б) Al и NaOH
В) HCl и K2SO3
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение жёлтого осадка
11. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) отсутствие внешних признаков
12. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ВЕЩЕСТВА:
А) Cu и HNO3 (конц.)
Б) Cu и H2SO4 (конц.)
В) BaCO3 и HCl
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бурого газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение бесцветного газа
13. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение синего осадка
14. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бурого осадка
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение синего осадка
15. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение бесцветного газа
3) выделение белого осадка
4) выделение чёрного осадка
16. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение синего осадка
17. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) отсутствие внешних признаков
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение чёрного осадка
18. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение бесцветного газа с характерным запахом
3) выделение белого осадка
4) растворение осадка
19. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бесцветного газа
2) выделение бесцветного газа с характерным запахом
3) выделение белого осадка
4) выделение студенистого бесцветного осадка
20. Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ПРИЗНАКИ РЕАКЦИИ:
1) выделение бурого газа
2) выделение газа с характерным запахом
3) выделение белого осадка
4) выделение жёлтого осадка
Источник