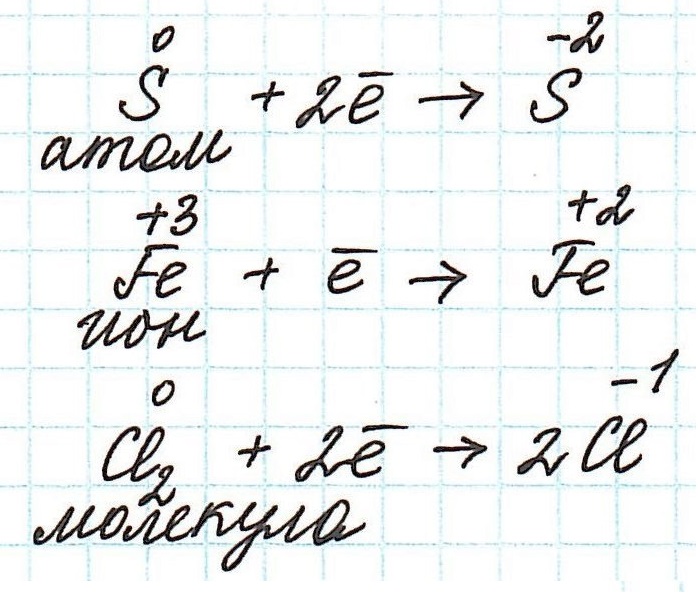- ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ В ХИМИЧЕСКИХ РЕАКЦИЯХ
- Понятие окислительно-восстановительной реакции
- Окислители, восстановители. Окисление, восстановление
- Способность к окислению и восстановлению: как определить
- Сильные или слабые окислители и восстановители: как определить
- Основные окислители и восстановители в химии
- Окисление металлов
- Смотреть что такое «Окисление металлов» в других словарях:
- Окисление металлов
- Полезное
- Смотреть что такое «Окисление металлов» в других словарях:
ОКИСЛИТЕЛИ И ВОССТАНОВИТЕЛИ В ХИМИЧЕСКИХ РЕАКЦИЯХ
Окислители и восстановители в химии — интересный, но очень часто вызывающий затруднения, вопрос.
Окислители и восстановители являются главными участниками особого типа химических процессов, к которым можно отнести большинство реакций, встречаемых нами и в природе, и в технике. Это окислительно-восстановительные реакции (ОВР) .
К примеру, превращение с помощью нитрифицирующих бактерий атмосферного азота в легко усваиваемую растениями форму, фотосинтез, дыхание живых организмов (от бактерий до высших растений и животных) — это ОВР в природе.
А вот выплавка стали, промышленное получение аммиака из азота и водорода, гальванические процессы, электролиз – эти и огромное количество других процессов являются примерами ОВР в технике.
Так что же такое окислительно-восстановительные реакции (процессы)?
Понятие окислительно-восстановительной реакции
Окислительно-восстановительные реакции (ОВР) – это процессы, в ходе которых изменяются степени окисления атомов химических элементов.
Окисление и восстановление сопровождают друг друга. Один процесс без другого просто не существует. Почему?
Изменение степени окисления всегда означает переход электронов от одних частиц к другим. То есть одни частицы отдают электроны в ходе химического или электрохимического взаимодействия, а другие частицы принимают. Здесь срабатывает закон сохранения материи.
Окислители, восстановители. Окисление, восстановление
Итак, окисление – это процесс, в ходе которого частица передает свои электроны другой частице. В качестве таких частиц могут выступать отдельные атомы или ионы, а также молекулы.
Частица, передающая свои электроны, является восстановителем .
Переход электронов принято показывать с помощью полуреакций:
Как не сложно заметить из представленных полуреакций, окислительный процесс приводит к увеличению степени окисления.
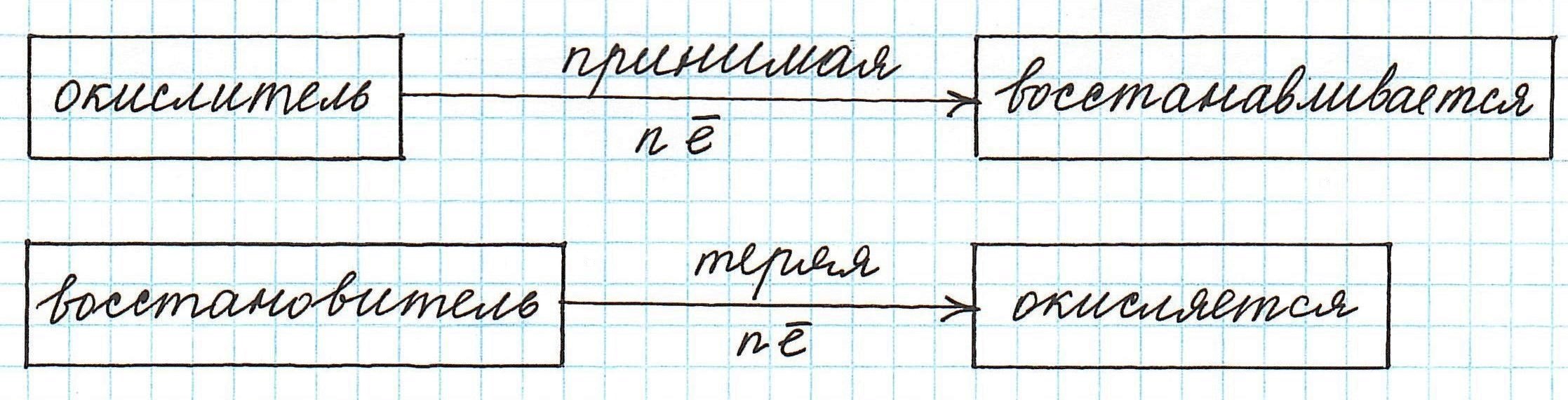
А вот восстановление , по сути, противоположно окислению. В его основе – принятие электронов одной частицей от другой.
Частица, принимающая электроны, является окислителем.
Восстановление всегда сопровождается уменьшением степени окисления!
Способность к окислению и восстановлению: как определить
Существует несколько закономерностей, которые помогают определить наличие у частицы (атома, иона, молекулы) способности окисляться или восстанавливаться. Обратимся к периодической таблице химических элементов.
1) В периодах слева направо (т.е. с повышением порядкового номера элемента) восстановительные свойства простых веществ уменьшаются, а окислительные увеличиваются:
То есть в начале периода находятся явные восстановители, а в конце – окислители. Например, в III периоде активным восстановителем является натрий, а активным окислителем – хлор.
А причина данной закономерности кроется в строении атомов элементов.
У атомов элементов одного периода:
- количество энергетических уровней остается постоянным (так, у элементов III периода их три);
- число электронов внешнего уровня растет (например, от 1 электрона у натрия и до 7 электронов у хлора).
В связи с этим растет и сила притяжения электронов к ядру. В результате радиус атома уменьшается.
У элементов конца периода эта сила велика. Поэтому атомы очень трудно отдают свои электроны в химических взаимодействиях и легче принимают их от других атомов, стремясь завершить внешний энергетический уровень. Так проявляются их окислительные свойства.
Атомам элементов начала периода для завершения внешнего уровня до устойчивого 8-электронного состояния легче отдать свои немногочисленные электроны, проявив тем самым восстановительные свойства.
2) Элементы побочных подгрупп (это металлы четных рядов больших периодов) на внешнем уровне имеют 2 или 3 (реже 1 в случае «провала») электрона, поэтому легко могут их отдавать, являясь, таким образом, восстановителями:
3) Элементы одной главной подгруппы имеют одинаковое число электронов на внешнем энергетическом уровне (например, элементы VI группы – шесть электронов). Число же энергетических уровней увеличивается и, соответственно, радиусы атомов тоже увеличиваются. Это приводит к тому, что электроны внешних уровней удаляются от ядра и притяжение их к нему ослабевает.
Вот именно поэтому, восстановительная способность (способность отдавать электроны) у элементов главных подгрупп сверху вниз растет, а окислительная способность (способность принимать электроны) снижается:
Так, среди элементов главной подгруппы VI группы окислительная способность сильнее всего проявляется у кислорода, а теллур в некоторых взаимодействиях способен проявлять восстановительные свойства.
4) Определить, чем будет являться частица (или вещество, в состав которого она входит) в окислительно-восстановительном процессе, можно по значению степени окисления (с.о.).
Если атомы имеют самую наименьшую с.о., то проявят они восстановительные свойства. Если самую высокую – то окислительные. А если с.о. является промежуточной по значению, то проявят как те, так и другие свойства (в зависимости от конкретных условий химической реакции). Например:
Сильные или слабые окислители и восстановители: как определить
Часто говорят: сильный окислитель, слабый окислитель, сильный восстановитель, слабый восстановитель. А что это значит? И как определить эту самую силу?
Мерой окислительно-восстановительной способности вещества служит значение стандартного электродного потенциала: чем оно больше, тем и окислительные свойства проявляются сильнее.
Обратимся к таблице стандартных электродных потенциалов. В ней значения потенциалов расположены в порядке уменьшения:
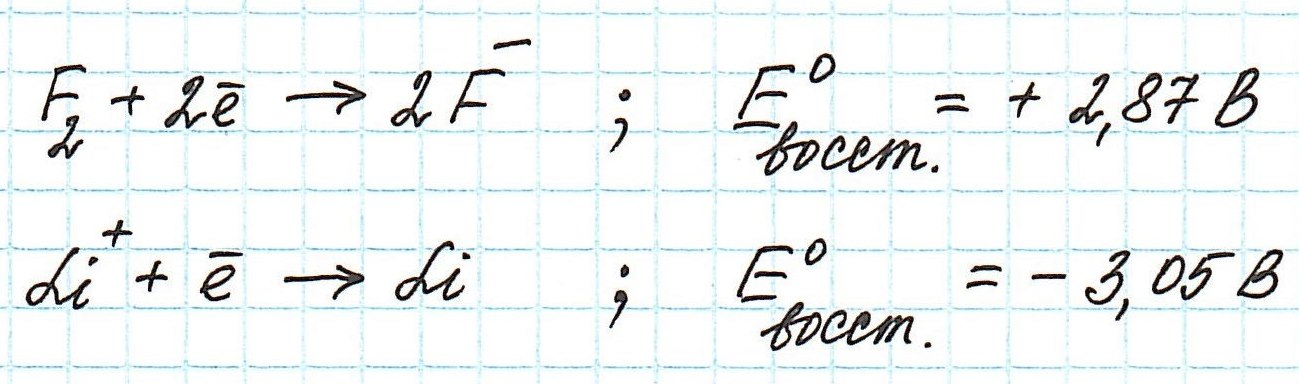
Окислительные потенциалы фтора и лития будут иметь противоположные значения.
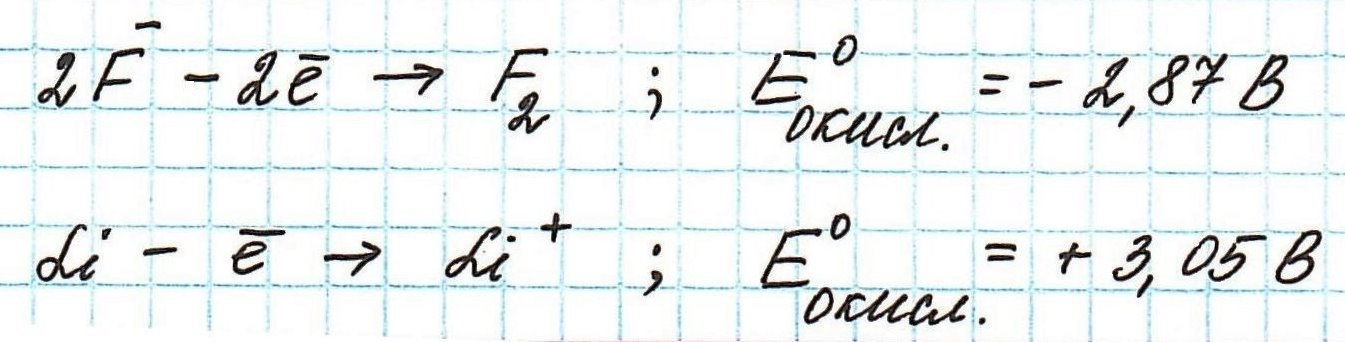
Пример . Используя таблицу стандартных электродных потенциалов, определите, какая из частиц проявляет более сильные окислительные свойства:
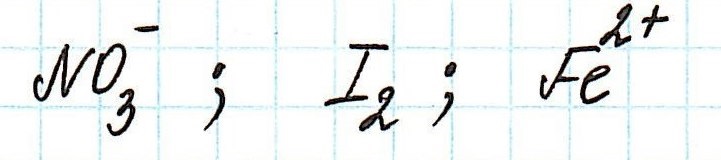
Наиболее сильным окислителем будет та частица, которая лучше всего восстанавливается, а, значит, имеет более высокий восстановительный электродный потенциал.
Сравним значения восстановительных потенциалов:
Таким образом, наиболее сильным окислителем из представленных является нитрат-ион.
Основные окислители и восстановители в химии
В технике применяется огромное количество окислителей и восстановителей с разной окислительной и восстановительной способностью.
Важнейшие из них представлены в таблице:
Итак, окисление и восстановление – два взаимосвязанных процесса. Они широко представлены в природе и играют огромную роль в промышленных производствах. Окислители и восстановители очень разнообразны. Чем будет являться частица (или вещество, в состав которого она входит): окислителем или восстановителем, – можно определить, используя некоторые закономерности.
Источник
Окисление металлов
Большая советская энциклопедия. — М.: Советская энциклопедия . 1969—1978 .
Смотреть что такое «Окисление металлов» в других словарях:
окисление металлов — Процесс взаимодействия твердого или жидкого металла (сплава) с кислородом, сопровождаемый образованием оксидов. В более широком смысле окисление металлов — реакции, в которых атомы теряют электроны и образуют соединения, например, хлориды,… … Справочник технического переводчика
Окисление металлов — [oxydation of metals] процесс взаимодействия твердого или жидкого металла (сплава) с кислородом, сопровождающий образование оксидов. В более широком смысле окисление металлов реакции, в которых атомы теряют электроны и образуются соединения,… … Энциклопедический словарь по металлургии
ОКИСЛЕНИЕ МЕТАЛЛОВ — [oxydation of metals] процесс взаимодействия твердого или жидкого металла (сплава) с кислородом, сопровождаемый образованием оксидов. В более широком смысле окисление металлов реакции, в которых атомы теряют электроны и образуют соединения,… … Металлургический словарь
окисление металлов — ▲ окисление ↑ металл ↓ патина. патинировать. позеленеть. окалина. | оксидирование … Идеографический словарь русского языка
Окисление — восстановление — Окисление восстановление, окислительно восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел атомов. Первоначально (со времени введения в химию кислородной теории горения А. Лавуазье, конец 18 в.)… … Большая советская энциклопедия
Окисление-восстановление — окислительно восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел (См. Окислительное число) атомов. Первоначально (со времени введения в химию кислородной теории горения А. Лавуазье, конец 18 в.)… … Большая советская энциклопедия
МЕТАЛЛОВ ОКИСЛЕНИЕ — подразделяется на химическое и электрохимическое. Для хим. окисления используют обычно газообразные реагенты, для электрохим. водные р ры. М. о. газообразными реагентами протекает при газовой коррозии, получении оксидов или галогенидов металлов… … Химическая энциклопедия
окисление-восстановление — [redox] химические реакции, сопровождаемые изменением окислительных чисел атомов. Согласно кислородной теории горения А. Лавуазье (кон. XVIII в.) окисление называл только реакции соединения с кислородом, восстановлением отнятие кислорода. С… … Энциклопедический словарь по металлургии
окисление-восстановление — Химические реакции, сопровождающиеся изменением окислительных чисел атомов. Согласно кислородной теории горения А. Лавуазье (кон. XVIII в.) окислением называются только реакции соединения с кислородом, восстановлением — отнятие кислорода. С … Справочник технического переводчика
Окисление — – процесс образования окислов металлов. [Блюм Э. Э. Словарь основных металловедческих терминов. Екатеринбург, 2002 г.] Рубрика термина: Общие термины Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги … Энциклопедия терминов, определений и пояснений строительных материалов
Источник
Окисление металлов
Окисление металлов [oxydation of metals] — процесс взаимодействия твердого или жидкого металла (сплава) с кислородом, сопровождающий образование оксидов. В более широком смысле окисление металлов — реакции, в которых атомы теряют электроны и образуются соединения, например, хлориды, Изделия из металлов и сплавов под воздействием окружающей среды подвергаются постепенному окислению — коррозии. При производстве металлургической продукции окисление металлов приводит к образованию на ней окалины, потери ценных легирующих элементов и железа. Окисление жидкого металла происходит в процессе плавки в открытых печах самопроизвольно вследствие контакта металла с воздухом и окислительнным шлаком. Направление процессов окисления металлов определяется как термодинамическое — изменением свободной энергии при реакции, так и кинетическим фактором — скоростью протекания реакции, которая в значительной степени зависит от природы продуктов окисления и характера их взаимодействия с металлом. Плавка металла в вакуумных печах — радикальный метод защиты его от окисления.
В ряде случаев проводят преднамеренное окисление металлоизделий в защитных или декоративных целях (Смотри Оксидирование).
Энциклопедический словарь по металлургии. — М.: Интермет Инжиниринг . Главный редактор Н.П. Лякишев . 2000 .
Полезное
Смотреть что такое «Окисление металлов» в других словарях:
окисление металлов — Процесс взаимодействия твердого или жидкого металла (сплава) с кислородом, сопровождаемый образованием оксидов. В более широком смысле окисление металлов — реакции, в которых атомы теряют электроны и образуют соединения, например, хлориды,… … Справочник технического переводчика
ОКИСЛЕНИЕ МЕТАЛЛОВ — [oxydation of metals] процесс взаимодействия твердого или жидкого металла (сплава) с кислородом, сопровождаемый образованием оксидов. В более широком смысле окисление металлов реакции, в которых атомы теряют электроны и образуют соединения,… … Металлургический словарь
окисление металлов — ▲ окисление ↑ металл ↓ патина. патинировать. позеленеть. окалина. | оксидирование … Идеографический словарь русского языка
Окисление металлов — реакция соединения металла с кислородом, сопровождающаяся образованием окислов (оксидов). В более широком смысле О. м. реакции, в которых атомы теряют электроны и образуются различные соединения, например хлориды, сульфиды и т.п. В… … Большая советская энциклопедия
Окисление — восстановление — Окисление восстановление, окислительно восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел атомов. Первоначально (со времени введения в химию кислородной теории горения А. Лавуазье, конец 18 в.)… … Большая советская энциклопедия
Окисление-восстановление — окислительно восстановительные реакции, химические реакции, сопровождающиеся изменением окислительных чисел (См. Окислительное число) атомов. Первоначально (со времени введения в химию кислородной теории горения А. Лавуазье, конец 18 в.)… … Большая советская энциклопедия
МЕТАЛЛОВ ОКИСЛЕНИЕ — подразделяется на химическое и электрохимическое. Для хим. окисления используют обычно газообразные реагенты, для электрохим. водные р ры. М. о. газообразными реагентами протекает при газовой коррозии, получении оксидов или галогенидов металлов… … Химическая энциклопедия
окисление-восстановление — [redox] химические реакции, сопровождаемые изменением окислительных чисел атомов. Согласно кислородной теории горения А. Лавуазье (кон. XVIII в.) окисление называл только реакции соединения с кислородом, восстановлением отнятие кислорода. С… … Энциклопедический словарь по металлургии
окисление-восстановление — Химические реакции, сопровождающиеся изменением окислительных чисел атомов. Согласно кислородной теории горения А. Лавуазье (кон. XVIII в.) окислением называются только реакции соединения с кислородом, восстановлением — отнятие кислорода. С … Справочник технического переводчика
Окисление — – процесс образования окислов металлов. [Блюм Э. Э. Словарь основных металловедческих терминов. Екатеринбург, 2002 г.] Рубрика термина: Общие термины Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги … Энциклопедия терминов, определений и пояснений строительных материалов
Источник