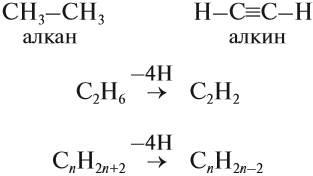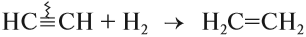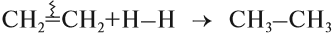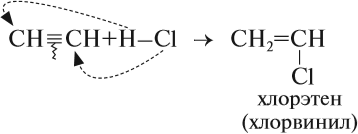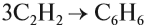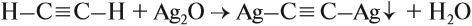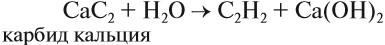Что значит нециклические углеводороды
Алкены (олефины) – это нециклические углеводороды, в молекулах которых два атома углерода находятся в состоянии sp 2 -гибридизации и связаны друг с другом двойной связью.
Алкены – непредельные алифатические углеводороды, молекулы которых содержат одну двойную связь и имеют общую формулу СnН2n.
Алкены (олефины, этиленовые углеводороды) – ациклические непредельные углеводороды, содержащие одну двойную связь между атомами углерода, образующие гомологический ряд с общей формулой СnН2n.
Свое второе название – «олефины» — алкены получили по аналогии с эфирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров – масел.
Алкены содержат в своей молекуле меньшее число водородных атомов, чем соответствующие им алканы (с тем же числом углеродных атомов), поэтому такие углеводороды называют непредельными или ненасыщенными.
Первый представитель этого класса – этилен СН2=СН2, в связи с чем алкены также называются этиленовыми углеводородами.
Общая формула гомологического ряда этиленовых углеводородов СnН2n совпадает с общей формулой циклоалканов, поэтому алкены и циклоалканы являются межклассовыми изомерами.
Простейшие представители алкенов:
Источник
Урок 20. Алкины
Определение. Гомологический ряд, номенклатура, изомерия
Алкины — это нециклические углеводороды, в молекулах которых есть одна тройная связь, а остальные связи простые.
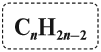
Алкины относят к группе непредельных ненасыщенных углеводородов. Для того чтобы вывести общую формулу гомологического ряда алкинов, сравним состав алканов и алкинов:
Таким образом, алкины образуют гомологический ряд, общая формула которого
Вопрос. Какие ещё углеводороды имеют такую же общую формулу гомологического ряда?
Значит, алкины и алкадиены с одинаковым числом атомов углерода являются изомерами.
Первый член гомологического ряда С2Н2 называется ацетилен. Поэтому алкины относятся к ацетиленовым углеводородам.
Вопрос. Почему в названиях ацетиленовых углеводородов появился суффикс ИН? (См. урок 17.7.)
Задание 20.1. Составьте молекулярную и графическую формулы алкина с n = 4.
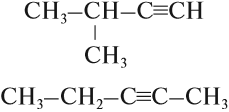
Выполнив последнее задание, вы убедитесь, что для этого алкина можно составить две графические формулы:
Значит, изомерия алкинов связана с положением тройной связи в молекуле. Кроме того, изомерия связана со строением углеводородного радикала:
Задание 20.2. Составьте молекулярные формулы этих соединений и убедитесь, что это изомеры. Назовите эти вещества.
- названия алкинов составляют, используя суффикс ИН;
- нумерацию основной цепи ведут с того конца, к которому ближе тройная связь.
Строение молекул
В состав молекулы любого алкина входит одна тройная связь, поэтому особенности свойств этих соединений будут связаны с особенностями тройной связи. Это сложная, неоднородная связь. Её составляют одна простая σ-связь и две π-связи.
Вопрос. Какая из этих связей легче разрушается в химических реакциях? Почему?
Значит, как и у алкенов, в химических реакциях будет прежде всего разрушаться менее прочная π-связь. Алкины тоже легко вступают в химические реакции, но, в отличие от алкенов, большинство реакций за счёт π-связи идут в две стадии: сначала разрывается одна π-связь, потом вторая π-связь. Характерной реакцией является реакций присоединения, хотя возможны и другие типы реакций.
Свойства алкинов
Физические свойства
По физическим свойствам алкины мало отличаются от алкенов и алканов. Так, простейший алкин ацетилен — газ без вкуса и запаха, плохо растворимый в воде. Среди гомологов ацетилена есть и жидкие, и твёрдые вещества: чем больше молекулярная масса, тем выше температуры кипения и плавления алкинов.
Химические свойства
Для алкинов, как и для алкенов, характерны реакции присоединения. Они идут в две стадии:
Вопрос. Возможна ли для полученного соединения реакция присоединения?
Поскольку полученный этилен содержит двойную связь, возможна вторая стадия этого процесса:
Вопрос. Возможна ли реакция присоединения для полученного вещества? Почему?
Таким образом, в результате реакции гидрирования из ацетилена можно получить и этилен, и этан. Всё зависит от условия процесса и от соотношения исходных веществ. Например, реакцию присоединения хлороводорода к ацетилену часто прерывают на первой стадии:
Дело в том, что хлорвинил применяется для получения полимера полихлорвинила.
Задание 20.3. Составьте уравнения реакции полимеризации хлорвинила.
Изделия из полихлорвинила (–СНСl–СН2–)n имеют разнообразное применение.
Так, полихлорвинил (ПХВ, или ПВХ) является основой для получения искусственной кожи, различной посуды одноразового пользования, полимерной тары, клеёнок, отделочных материалов и т. д. Многие пластмассовые изделия, которые мы используем каждый день, обивка салонов автомобилей, вагонов, самолётов, — сделаны из ПВХ. Он также используется для электроизоляции проводов.
Аналогично идут и другие реакции присоединения. Например, ацетилен, как и этилен, обесцвечивает бромную воду. Кроме того, он обесцвечивает и раствор перманганата калия, т. е. вступает в реакции окисления.
Задание 20.4. Составьте уравнения реакции ацетилена с бромом.
Таким образом, ацетилен тоже даёт качественные реакции на π-связь. Поэтому правильнее говорить, что реакции обесцвечивания бромной воды и перманганата калия — это качественные реакции на кратную связь. Другими словами, при помощи этих реакций можно обнаружить непредельные соединения, содержащие кратную связь, которая содержит π-связь.
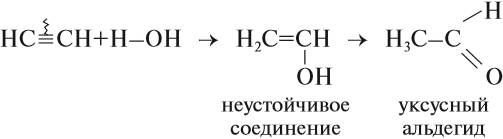
Большое практическое значение имеет реакция присоединения воды к ацетилену — гидратация ацетилена. Поскольку эту реакцию открыл и изучил российский ученый М. Г. Кучеров*, она носит название «реакция Кучерова»:
* Кучеров Михаил Григорьевич (3.06.1850–26.06.1911) — русский химик-органик. Открыл (1881) реакцию каталитической гидратации ацетиленовых углеводородов с образованием карбонилсодержащих соединений.
Уксусный альдегид нужен для получения уксусной кислоты. Ацетилен горит.
Задание 20.5. Составьте уравнение реакции горения ацетилена.
Газообразные углеводороды можно различить по характеру пламени. Так, метан горит бесцветным пламенем, этилен — светящимся, а ацетилен — коптящим, т. е. углерод окисляется не полностью и частично выделяется в виде простого вещества (сажи). В токе кислорода ацетилен горит ослепительно-голубым пламенем с выделением большого количества теплоты (температура пламени превышает 3000 °C!). Поэтому эта реакция используется для газовой сварки и резки металлов.
При неполном окислении ацетилена (раствором перманганата калия) образуется смесь кислот.
Для ацетилена возможна реакция полимеризации, причём в эту реакцию может вступать небольшое число молекул. Так, при тримеризации ацетилена (соединяются три молекулы) образуется циклическое соединение — бензол:
Для алкинов характерна подвижность атомов водорода у тройной связи. За счёт этих атомов происходят реакции замещения таких атомов водорода:
Аналогичная реакция замещения происходит и с оксидом меди (I), и со щелочными металлами. В результате обеих реакций выделяется осадок, поэтому их считают качественными реакциями на алкины, в молекулах которых имеется атом водорода у тройной связи. Такая же реакция замещения происходит и со щелочными металлами.
Получение и применение ацетилена
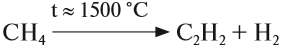
Ацетилен в небольших количествах входит в состав природных газов. Его получают крекингом метана:
В небольших количествах, например для сварки металлов и в лаборатории, его получают из карбида кальция:
Ацетилен, полученный карбидным способом, используется для сварки и резки металлов, поскольку температура пламени автогена (горение ацетилена в кислороде) достигает 3000 °C.
Ацетилен и его производные используются для получения пластмасс, каучуков, уксусной кислоты, растворителей.
Выводы
Алкины — это непредельные углеводороды, содержащие тройную связь. Для таких веществ характерны реакции:
- присоединения;
- окисления;
- полимеризации. Все они происходят за счёт разрыва π-связи, которая входит в состав тройной связи;
- замещения атома водорода у тройной связи.
Источник
Большая Энциклопедия Нефти и Газа
Нециклические углеводород
Нециклические углеводороды , рассмотренные в предыдущем разделе, называются алифатическими углеводородами. [1]
В случае нециклических углеводородов с разветвленной цепью образование карбониевых ионов может происходить путем расщепления углерод-углеродной связи в реакциях деполимеризации или диспропорционирования, о которых уже говорилось ранее. Так, в определенных условиях из диизобутилена получают два моля триметилуксусной кислоты. [2]
В случае нециклических углеводородов с разветвленной цепью образование карбониевых ионов может происходить путем расщепления углерод-углеродной связи в реакциях деполимеризации или дйспропордионирования, о которых уже говорилось ранее. Так, в определенных условиях из диизобутилена получают два моля триметилуксусной кислоты. [3]
При разрушении предельных и непредельных нециклических углеводородов конечными продуктами являются углекислота и вода; предельные углеводороды, окисляясь, превращаются в непредельные, а последние разрушаются биологическим путем [102] значительно быстрее и легче, чем первые. Видимо, наличие двойной связи в соединении способствует их биологическому разложению. [4]
Эта теория довольно хорошо оправдывалась для реакций нециклических углеводородов . Ниже приведены результаты расчета взаимных поляризуемостей ( л) в бутадиене ( см. [ 10, стр. [5]
Вычисления содержания различных типов молекул аналогичны тем, которые были приведены для нециклических углеводородов в неароматическом масле. Ниже описан анализ дестиллатной фракции III нефти о. [6]
Необходимый для деалкилированкя водород получался в результате одновременно протекающих реакций конденсации ароматических углеводородов и дегидрирования нециклических углеводородов С3 — С5, специально вводимых для этой цели в реакционную зону. [7]
В реакции присоединения спиртов к диеновым углеводородам фтористый бор как катализатор применяется с 1946 г. Из нециклических углеводородов исследована только реакция гексадиена-1 2 с метанолом в присутствии катализатора BF3 — 0 ( G. Лучше изучено присоединение спиртов к циклическим диеновым углеводородам. [8]
Простейшие органические соединения, состоящие только из атомов углерода и водорода, называют углеводородами. Нециклические углеводороды классифицируют в соответствии с природой углерод-углеродных связей: содержащие только ординарные именуют алканами, одну двойную-алкенами, две двойных-алкадиенами, одну тройную-алкинами. [9]
Простейшие органические соединения, состоящие только из атомов углерода и водорода, называют углеводородами. Нециклические углеводороды классифицируют в соответствии с природой углерод-углеродных связей: содержащие только ординарные именуют алканами, одну двойную-алкенами, две двойных-алкадиенами, одну тройную-алкинами. [10]
Диенильными лигандами называются такие углеводородные лиганды, которые формально предоставляют пять я-электронов при образовании связи с металлом. В качестве диенильных ли-гандов могут выступать непредельные пяти -, шести — и семи-членные циклические и некоторые нециклические углеводороды . Циклопентадиенильная группа является наиболее простым и в то же время наиболее типичным пятиэлектронным лигандом, и поэтому глава начинается с рассмотрения химии циклопента-диенильных комплексов металлов. Циклопентадиениды переходных металлов для удобства также рассмотрены в этом разделе. [11]
Для смесей метана с ароматическими углеводородами зависи — мость выхода частиц от концентрации имеет совершенно другой вид. Для малых концентраций бензола и нафталина кривые выход частиц — концентрация имеют резко выраженный максимум. Это показывает, что зародыши сажевых частиц из молекул ароматических углеводородов образуются по совершенно другому механизму и со значительно большей скоростью, чем для нециклических углеводородов . Если принять, что для начальной возрастающей ветви кривой выхода частиц для смесей метан — бензол и метан — нафталин наблюдается аддитивность, то выход частиц из бензола должен быть на два, а для нафталина примерно на три порядка выше, чем для метана. [12]
Хотя летучие масла древесины состоят в основном из углерода, водорода и кислорода, они характеризуются большим разнообразием составных частей. Различные масла могут содержать от 3 до 35 и более индивидуальных соединений. Только в редких случаях состав прост и свыше 90 % масла представлено одним соединением. Летучие масла обычно включают в себя несколько, а иногда и много химических веществ, принадлежащих к следующим классам соединений: 1) углеводороды: терпены ( C10Hi6), сесквитер-пены ( Ci5H24), дитерпены ( & 0Нз2) и другие циклические и нециклические углеводороды ; 2) кислоты и фенолы; 3) спирты: терпеновые, сесквитерпе-новые и другие; 4) сложные эфиры; 5) простые эфиры; 6) альдегиды и ке-томы; 7) окиси и лактоны. [13]
Источник