Атомные радиусы
Определение атомных радиусов также связано с некоторыми проблемами. Во-первых, атом не является сферой со строго определенными поверхностью и радиусом. Напомним, что атом представляет собой ядро, окруженное облаком электронов. Вероятность обнаружения электрона по мере удаления от ядра постепенно возрастает до некоторого максимума, а затем постепенно уменьшается, но становится равной нулю только на бесконечно большом расстоянии. Во-вторых, если мы все же выберем некоторое условие для определения радиуса, такой радиус все равно нельзя будет измерить экспериментально.
Эксперимент позволяет определять только межъядерные расстояния, другими словами-длины связей (и то с определенными оговорками, приведенными в подписи к рис. 2.21). Для их определения используется рентгеноструктурный анализ или метод электронографии (основанный на дифракции электронов). Радиус атома полагают равным половине наименьшего межъядерного расстояния между одинаковыми атомами.
Вандерваальсовы радиусы. Для несвязанных между собой атомов половина наименьшего межъядерного расстояния называется вандерваальсовым радиусом. Это определение поясняет рис. 2.22.
Рис. 2.21. Длина связи. Вследствие того что молекулы непрерывно колеблются, межъядерное расстояние, или длина связи, не имеет фиксированного значения. Этот рисунок схематически изображает линейное колебание простой двухатомной молекулы. Колебания не позволяют определить длину связи просто как расстояние между центрами двух связанных атомов. Более точное определение выглядит так: длина связи это расстояние между связанными атомами, измеренное между центрами масс двух атомов и соответствующее минимуму энергии связи. Минимум энергии показан на кривой Морзе (см. рис. 2.1).

Таблица 2.6. Плотности аллотропов углерода и серы Таблица 2.7. Длина связей углерод — углерод
Ковалентные радиусы. Ковалентный радиус определяется как половина межъядерного расстояния (длины связи) между двумя одинаковыми атомами, связанными друг с другом ковалентной связью (рис. 2.22, б). В качестве примера возьмем молекулу хлора Cl2, длина связи в которой составляет 0,1988 нм. Ковалентный радиус хлора полагается равным 0,0944 нм.
Зная ковалентный радиус атома одного элемента, можно вычислить ковалентный радиус атома другого элемента. Например, экспериментально установленное значение длины связи С—Cl в CH3Cl равно 0,1767 нм. Вычитая из этого значения ковалентный радиус хлора (0,0994 нм), находим, что ковалентный радиус углерода равен 0,0773 нм. Такой метод вычисления основан на принципе аддитивности, согласно которому атомные радиусы подчиняются простому закону сложения. Таким образом, длина связи С—Cl представляет собой сумму ковалентных радиусов углерода и хлора. Принцип аддитивности применим только к простым ковалентным связям. Двойные и тройные ковалентные связи имеют меньшую длину (табл. 2.7).
Длина простой ковалентной связи зависит еще от ее окружения в молекуле. Например, длина связи С—H изменяется от 0,1070 нм у тризамещенного атома углерода до 0,115 нм в соединении CH3CN.
Металлические радиусы. Металлический радиус полагается равным половине межъядерного расстояния между соседними ионами в кристаллической решетке металла (рис. 2.22, в). Термин атомный радиус обычно относится к ковалентному радиусу атомов неметаллических элементов, а термин металлический радиус
к атомам металлических элементов.
Ионные радиусы. Ионный радиус-это одна из двух частей межъядерного расстояния между соседними одноатомными (простыми) ионами в кристаллическом ионном соединении (соли). Определение ионного радиуса тоже сопряжено с немалыми проблемами, поскольку экспериментально измеряют межионные расстояния, а не сами ионные радиусы. Межионные расстояния зависят от упаковки ионов в кристаллической решетке. На рис. 2.23 показаны три возможных способа упаковки ионов в кристаллической решетке. К сожалению, экспериментально измеренные межионные расстояния
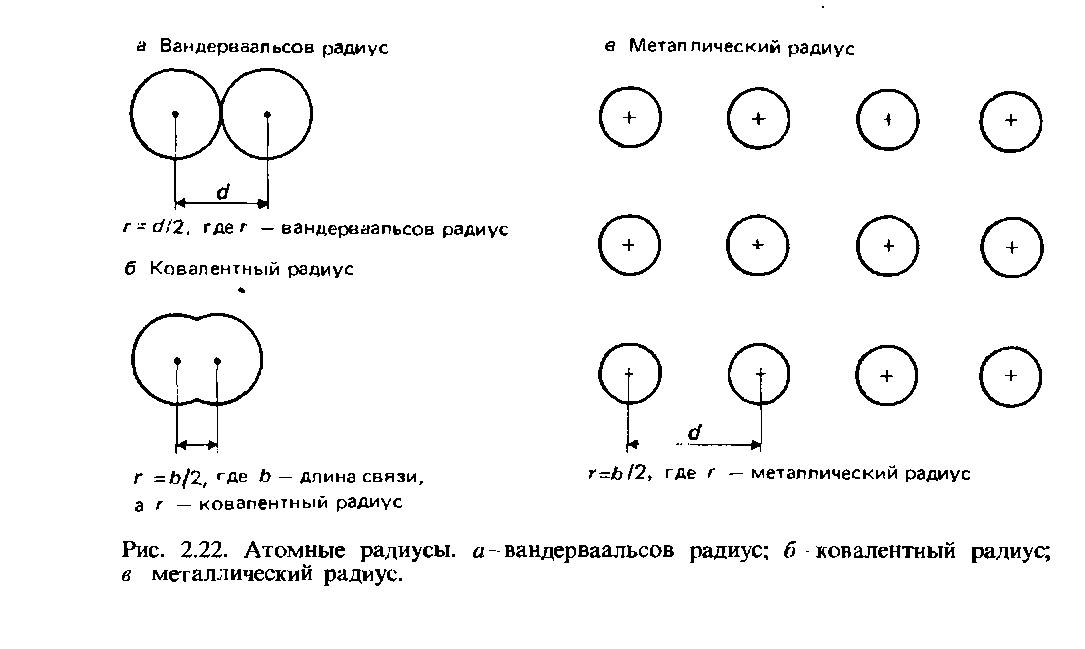
Рис. 2.23. Ионные радиусы, с-анионы соприкасаются друг с другом, но катионы не соприкасаются с анионами; б-катионы соприкасаются с анионами, но анионы не соприкасаются друг с другом; в условно принятое расположение ионов, при котором катионы соприкасаются с анионами и анионы соприкасаются друг с другом. Расстояние а определяется экспериментально. Оно принимается за удвоенный радиус аниона. Это позволяет вычислить межионное расстояние b, представляющее собой сумму радиусов аниона и катиона. Зная межионное расстояние Ь, можно вычислить радиус катиона.
не позволяют судить о том, какой из этих трех способов упаковки действительно осуществляется в каждом конкретном случае. Проблема заключается в том, чтобы найти пропорцию, в которой следует разделить межионное расстояние на две части, соответствующие радиусам двух ионов, другими словами, решить, где же на самом деле кончается один ион и где начинается другой. Как показывает, например, рис. 2.12, этот вопрос не позволяют решить и карты электронной плотности солей. Для преодоления указанной трудности обычно предполагают, что: 1) межионное расстояние представляет собой сумму двух ионных радиусов, 2) ионы имеют сферическую форму и 3) соседние сферы соприкасаются друг с другом. Последнее предположение соответствует способу упаковки ионов, изображенному на рис. 2.23, е. Если известен один ионный радиус, другие ионные радиусы можно вычислить на основании принципа аддитивности.
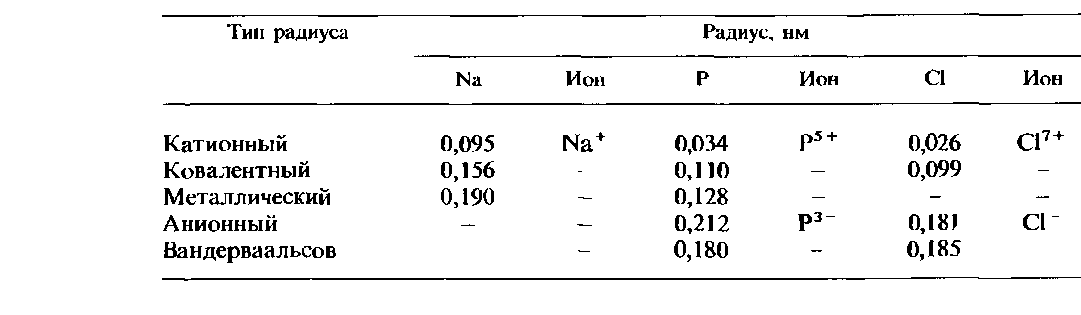
Сопоставление радиусов различных типов. В табл. 2.8 указаны значения радиусов различных типов для трех элементов 3-го периода. Нетрудно видеть, что самые большие значения принадлежат анионным и вандерваальсовым радиусам. На рис. 11.9 сопоставлены размеры ионов и атомов для всех элементов 3-го периода, за исключением аргона. Размеры атомов определяются их ковалентными радиусами. Следует обратить внимание на то, что катионы имеют меньшие размеры, чем атомы, а анионы — большие размеры, чем атомы этих же элементов. Для каждого элемента из всех типов радиусов наименьшее значение всегда принадлежит катионному радиусу.
Таблица 2.8. Сопоставление атомных радиусов различных типов

Экспериментальное определение. Для определения формы простых молекул и многоатомных ионов, а точнее — длин связей и валентных углов (углов между связями), используются разнообразные экспериментальные методы. К ним относятся микроволновая спектроскопия, а также методы изучения дифракции рентгеновских лучей (рентгеноструктурный анализ), нейтронов (нейтронография) или электронов (электронография). В следующей главе подробно рассказывается о том, каким образом с помощью дифракции рентгеновских лучей можно определять кристаллическую структуру. Однако для определения формы простых молекул в газовой фазе обычно используется электронография (метод изучения дифракции электронов). Этот метод основан на использовании волновых свойств электронов. Пучок электронов пропускают сквозь образец исследуемого газа. Молекулы газа рассеивают электроны, и в результате возникает дифракционная картина. Анализируя ее, можно определить длины связей и валентные углы в молекулах. Этот метод аналогичен используемому при анализе дифракционной картины, образуемой при рассеянии рентгеновских лучей.
Источник
Атомный радиус, как он измеряется, как он изменяется в периодической таблице, примеры
атомный радиус это важный параметр для периодических свойств элементов таблицы Менделеева. Это напрямую связано с размером атомов, поскольку на большем радиусе они больше или громоздче. Кроме того, это связано с электронными характеристиками того же.
Пока атом имеет больше электронов, тем больше его размер и атомный радиус. Оба определяются электронами валентной оболочки, потому что на расстояниях за пределами их орбит вероятность обнаружения электрона приближается к нулю. В окрестности ядра происходит обратное: увеличивается вероятность нахождения электрона.
Верхнее изображение представляет собой упаковку ватных шариков. Обратите внимание, что каждый из них окружен шестью соседями, не считая другого возможного верхнего или нижнего ряда. Способ уплотнения ватных шариков будет определять их размеры и, следовательно, их радиусы; как это происходит с атомами.
Элементы в соответствии с их химической природой так или иначе взаимодействуют со своими собственными атомами. Следовательно, величина атомного радиуса варьируется в зависимости от типа присутствующей связи и твердой упаковки ее атомов..
- 1 Как измеряется атомный радиус?
- 1.1 Определение межъядерного расстояния
- 1.2 Единицы
- 2 Как это меняется в периодической таблице?
- 2.1 За период
- 2.2 По убыванию по группе
- 2.3 Сокращение лантаноидов
- 3 примера
- 4 Ссылки
Как измеряется атомный радиус?
На основном изображении можно легко измерить диаметр ватных шариков, а затем разделить его на два. Однако сфера атома не полностью определена. Почему? Потому что электроны циркулируют и диффундируют в определенных областях пространства: орбитали.
Поэтому атом можно рассматривать как сферу с неощутимыми краями, о которых невозможно точно сказать, в какой степени они заканчиваются. Например, на верхнем изображении центральная область около ядра выглядит более интенсивной, а ее края размыты.
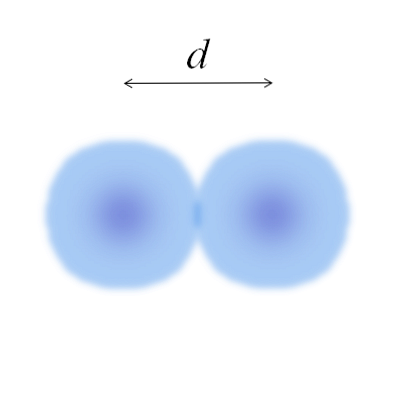
Изображение представляет двухатомную молекулу E2 (как Cl2, H2, О2, и т.д.). Предполагая, что атомы являются сферическими телами, если расстояние было определено d что разделяет оба ядра в ковалентной связи, то было бы достаточно разделить его на две половины (d/ 2) получить атомный радиус; точнее, ковалентный радиус E для E2.
А если Е не образует с собой ковалентных связей, но это металлический элемент? то d это будет указано числом соседей, которые окружают Е в его металлической структуре; то есть по координационному числу (N.C) атома в упаковке (помните ватные шарики основного изображения).
Определение межъядерного расстояния
Определить d, это межъядерное расстояние для двух атомов в молекуле или упаковке, это требует методов физического анализа.
Одной из наиболее часто используемых является дифракция рентгеновских лучей, в которой пучок света облучается через кристалл, и изучается дифракционная картина, возникающая в результате взаимодействия электронов с электромагнитным излучением. В зависимости от упаковки могут быть получены различные дифракционные картины и, следовательно, другие значения d.
Если атомы «плотно» в кристаллической решетке, они будут представлять разные значения d по сравнению с тем, что они имели бы, если бы они были «удобными». Кроме того, эти межъядерные расстояния могут колебаться в значениях, поэтому атомный радиус фактически состоит из среднего значения таких измерений.
Как связаны атомный радиус и координационное число? В. Гольдшмидт установил взаимосвязь между ними, в которой для N.C. из 12 относительное значение равно 1; от 0,97 для упаковки, где атом имеет N.C, равный 8; 0,96 для N.C, равного 6; и 0,88 для N.C. из 4.
единицы
Из значений для N.C, равных 12, было построено много таблиц, сравнивающих атомные радиусы всех элементов периодической таблицы..
Поскольку не все элементы образуют такие компактные структуры (N.C меньше 12), соотношение В. Гольдшмидта используется для расчета их атомных радиусов и выражения для одной и той же упаковки. Таким образом, измерения атомных радиусов стандартизированы.
Но в каких единицах они выражают себя? при условии d имеет очень малую величину, следует прибегнуть к единицам ангстрем Å (10 ∙ 10 -10 м) или также широко используемый, пикометр (10 ∙ 10 -12 м).
Как это меняется в периодической таблице?
На протяжении периода
Атомные радиусы, определенные для металлических элементов, имеют название металлических радиусов, а для неметаллических элементов — ковалентные радиусы (такие как фосфор, P4, или сера, S8). Однако между обоими типами радиостанций существует более заметное различие, чем название.
Слева направо в тот же период, ядро добавляет протоны и электроны, но последние ограничены тем же уровнем энергии (главное квантовое число). Как следствие, ядро оказывает увеличивающийся эффективный заряд ядра на валентные электроны, который сжимает атомный радиус..
Таким образом, неметаллические элементы в тот же период имеют тенденцию иметь атомные (ковалентные) радиусы меньше, чем металлы (металлические радиусы).
По убыванию группой
При спуске по группе включаются новые уровни энергии, которые позволяют электронам иметь больше места. Таким образом, электронное облако преодолевает большие расстояния, его размытая периферия все больше отдаляется от ядра, и, следовательно, радиус атома расширяется.
Сокращение лантаноидов
Электроны внутреннего слоя помогают экранировать эффективный заряд ядра на валентных электронах. Когда орбитали, составляющие внутренние слои, имеют много «дырок» (узлов), как и в случае f-орбиталей, ядро сильно сжимает атомный радиус из-за плохого экранирующего эффекта орбиталей..
Этот факт подтверждается сокращением лантаноидов в период 6 периодической таблицы. От La до Hf происходит значительное сжатие атомного радиуса, создаваемого орбиталями f, которые «заполняются» при прохождении через блок f: у лантаноидов и актиноидов.
Аналогичный эффект можно наблюдать и с элементами блока p периода 4. На этот раз произведение слабого экранирующего эффекта орбиталей d, которые заполняются при пересечении периодов переходных металлов..
примеров
Для периода 2 периодической таблицы атомные радиусы ее элементов:
-Быть: 112 вечера
Обратите внимание, что металлический литий имеет наибольший атомный радиус (257 мкм), в то время как фтор, расположенный в крайней правой части периода, является наименьшим из них (64 мкм). Атомный радиус уменьшается слева направо за тот же период, и перечисленные значения показывают его.
Литий, образуя металлические связи, его радиус металлический; и фтор, поскольку он образует ковалентные связи (F-F), его радиус является ковалентным.
А если вы хотите выразить атомные радиостанции в единицах ангстрема? Просто разделите их на 100: (257/100) = 2,57Å. И так далее с остальными ценностями.
Источник