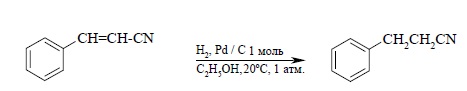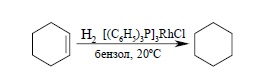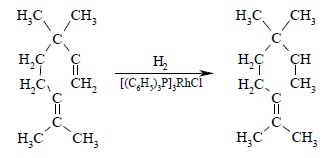- Что значит каталитическое гидрирование
- 8.1. Каталитическое гидрирование
- Каталитическое гидрирование алкенов
- Каталитическое гидрирование алкенов
- Готовые работы на аналогичную тему
- Гетерогенное каталитическое гидрирование
- Гомогенное каталитическое гидрирование
- Механизм гидрирования алкенов
- Катализаторы гидрирования
- Готовые работы на аналогичную тему
- Механизм каталитического гидрирования
- Восстановление алкенов
- Восстановление диенов
Что значит каталитическое гидрирование
В данной главе будет рассмотрено восстановление ряда функциональных групп с кратными связями и некоторые примеры восстановительного разрыва простых связей углерод — гетероатом. Помимо совершенно специфических реакций восстановления определенных функциональных групп существуют три метода, которые могут быть использованы для восстановления многих функциональных групп, а именно: каталитическое гидрирование, восстановление гидридами металлов и восстановление растворяющимися металлами. Эти три общих метода и рассмотрим первыми.
8.1. Каталитическое гидрирование
Каталитическое гидрирование — широко применяемый способ восстановления органических соединений. Как правило, редакцию проводят при перемешивании или встряхивании раствора соединения в присутствии гетерогенного катализатора в атмосфере водорода. Эти реакции удобно рассмотреть, разделив их на два типа: гидрирование при низком давлении и гидрирование при высоком давлении. Первый включает использование давления водорода от 1 до 4 атм при температуре от 0 до 100 °С, а для второго характерны давление водорода 100—300 атм и температура до 300 °С.
Гидрирование при низком давлении проводят в присутствии скелетного никеля, платины (обычно получаемой в реакционной смеси гидрированием катализатора Адамса, 
В зависимости от физических свойств восстанавливаемого соединения гидрирование при высоком давлении можно
Таблица 8.1. (см. скан) Продукты каталитического гидрирования
проводить с использованием растворителя или без него в присутствии таких катализаторов, как скелетный никель, хромит меди или палладий на угле. В табл. 8.1 приведены продукты гидрирования различных функциональных групп, причем порядок расположения примерно соответствует легкости гидрирования: хлорангидрид кислоты наиболее реакционноспособен, арен — наименее реакционноспособен.
Гидрирование с использованием гетерогенного катализатора иногда может приводить к изомеризации субстрата (разд. 8.4.1). Изомеризация может быть сведена к минимуму при использовании гомогенного катализатора, например хлорида 
гетерогенной реакции. Это может играть большую роль при дейтерировании. При использовании гомогенного катализатора возникает проблема его отделения от реакционной смеси после завершения реакции. Полимерные аналоги могут сочетать легкость отделения от раствора с образованием продуктов высокой чистоты.
Источник
Каталитическое гидрирование алкенов
Несмотря на то, что гидрирование этилена и всех других алкенов до алканов сопровождается выделением тепла, эта реакция с достаточной скоростью идет только в присутствии определенных катализаторов. Катализатор, по определению, не влияет на тепловой эффект реакции и его роль сводится к понижению энергии активации. Следует различать гетерогенное и гомогенное каталитическое гидрирование алкенов. В гетерогенном гидрировании используются тонкоизмельченные металлические катализаторы — платина, палладий, рутений, родий, осмий и никель либо в чистом виде, либо нанесенные на инертные носители – BaSO4, CaCO3, активированный уголь и т.д. Все они нерастворимы в органических средах и действуют как гетерогенные катализаторы. Наибольшую активность среди них проявляют рутений и родий, но наибольшее распространение получили платина и никель. Платину обычно применяют в виде черного диоксида PtO2, широко известного под названием «катализатор Адамса». Диоксид платины получают при сплавлении платинохлористоводородной кислоты H2PtCl6•6H2O или гексахлорплатината аммония (NH4)2PtCl6 с нитратом натрия. Гидрирование алкенов с катализатором Адамса проводят обычно при нормальном давлении и температуре 20– 50ºС в спирте, уксусной кислоте, этилацетате. При пропускании водорода двуокись платины восстанавливается непосредственно в реакционном сосуде до платиновой черни, которая и катализирует гидрирование. Другие более активные металлы платиновой группы используют на инертных носителях, например, Pd/C или Pb/BaSO4, Ru/Al2O3, Rh/C и др. Палладий, нанесенный на уголь, катализирует гидрирование алкенов до алканов в спиртовом растворе при 0 – 20ºС и нормальном давлении. Никель обычно используется в виде так называемого «никеля Ренея». Для получения этого катализатора сплав никеля с алюминием обрабатывают горячей водной щелочью для удаления почти всего алюминия и далее водой до нейтральной реакции. Катализатор имеет пористую структуру и поэтому называется также скелетным никелевым катализатором. Типичные условия гидрирования алкенов над никелем Ренея требуют применения давления порядка 5 – 10 атм. и температуры 50 – 100ºС, т.е. этот катализатор значительно менее активен, чем металлы платиновой группы, но более дешев. Ниже приведены некоторые типичные примеры гетерогенного каталитического гидрирования ациклических и циклических алкенов:
Так как оба атома водорода присоединяются к атомам углерода с двойной связью с поверхности металла-катализатора, обычно присоединение происходит с одной стороны двойной связи. Этот тип присоединения называется син-присоединением. В тех случаях, когда два фрагмента реагента присоединяются с различных сторон кратной связи (двойной или тройной), имеет место анти-присоединение. Термины син- и анти- по смыслу эквивалентны терминам цис- и транс-. Чтобы избежать путаницы и недоразумений, термины син- и анти- относятся к типу присоединения, а термины цис- и транс- — к строению субстрата (алкена).
Хотя многие важные детали еще неясны, достигнуто общее понимание механизма и стереохимии сложного процесса каталитического гидрирования. Водород адсорбируется на поверхности металлического катализатора. Кратная углерод-углеродная связь также взаимодействует с поверхностью металла, образуя сложные интермедиаты, в которых органическая молекула сильно адсорбирована. Первоначально образовавшийся интермедиат адсорбирован обоими углеродными атомами двойной связи, и π-орбитали алкена использованы для связывания с поверхностью металла. Водород, адсорбированный на поверхности, далее присоединяется к адсорбированной молекуле субстрата, и образующаяся при этом частица связана с поверхностью металла σ-связью. Этот интермедиат далее подвергается гидрогенолизу – расщеплению новой молекулой водорода по связи C – металл с образованием конечного насыщенного продукта. Схематически и упрощенно это может быть представлено следующим образом:
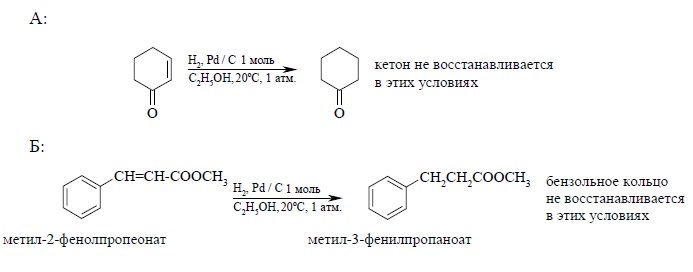
Двойная связь в алкенах гидрируется с большей скоростью по сравнению со многими другими функциональными группами (C=O, COOR, CN и др.) и поэтому гидрирование двойной C=C-связи часто представляет собой селективный процесс, если гидрирование ведется в мягких условиях (0 – 20ºС и при атмосферном давлении. Ниже приведены некоторые типичные примеры:
Большим и принципиально важным достижением в каталитическом гидрировании является открытие растворимых комплексов металлов, которые катализируют гидрирование в гомогенном растворе. Гетерогенное гидрирование на поверхности металлических катализаторов имеет ряд существенных недостатков, таких как изомеризация алкена и расщепление одинарных углерод-углеродных связей (гидрогенолиз). Гомогенное гидрирование лишено этих недостатков. За последние годы получена большая группа катализаторов гомогенного гидрирования – комплексов переходных металлов, содержащих различные лиганды. Лучшими катализаторами гомогенного гидрирования являются комплексы хлоридов родия (I) и рутения (III) с трифенилфосфином – трис-(трифенилфосфин)родийхлорид [(C6H5)3P]3RhCl и гидрохлорид трис-(трифенилфосфин)-рутения [(C6H5)3P]3RuHCl. Наиболее доступен родиевый комплекс, который получается при взаимодействии хлорида родия (III) с трифенилфосфином (катализатор Дж. Уилкинсона). Родиевый комплекс Уилкинсона используется для гидрирования двойной связи в обычных условиях:
Важное преимущество гомогенных катализаторов заключается в возможности селективного восстановления моно- и дизамещенной двойной связи по сравнению с три и тетразамещенной из-за больших различий в скорости гидрирования. Благодаря этому стало возможно селективное восстановление одной двойной связи в присутствии другой двойной связи в одной и той же молекуле:
Присоединение водорода происходит в цис-положение, восстановление цис-2-бутена дейтерием приводит к мезо-2,3-дидейтеробутану:
Источник
Каталитическое гидрирование алкенов
Вы будете перенаправлены на Автор24
Известно, что водород «в момент выделения», образующийся при взаимодействии цинка или олова с кислотами или натрия со спиртом, не удается присоединить к изолированной кратной связи в алкене.
Однако молекулярный водород в присутствии металлов VIII группы способен присоединяться по кратной связи алкена даже в сравнительно мягких условиях с образованием предельных углеводородов:
$CH_2=CH_2 + H_2 → CH_3–CH_3$
Гидрирование можно проводить как в паровой фазе проточным методом, пропуская пары алкена в токе водорода над нагретым катализатором, так и при комнатной температуре в статических условиях, встряхивая суспензию порошка катализатора в гидрируемом алкене в атмосфере водорода,
Механизм реакции полностью не выяснен. В настоящее время экспериментально установлено, что как этилен, так и водород взаимодействуют с поверхностью никеля с выделением энергии (250 и 125 кДж/моль соответственно). Это дает право утверждать, что собственно реакции предшествует активированная адсорбция алкена и водорода на находящихся на поверхности катализатора атомах металла, в результате чего происходит ослабление пи-связи в алкене и связи $H—H$ в молекуле водорода, вплоть до полного разрыва. Последнее можно подтвердить тем, что в присутствии никеля в смеси газообразных водорода и дейтерия быстро наступает равновесие:
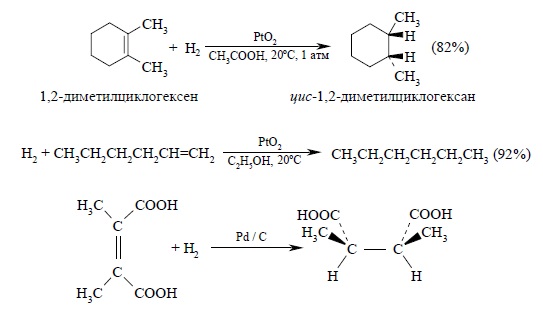
Есть основания утверждать, что присоединение обоих атомов водорода к активированному комплексу алкена на поверхности катализатора происходит синхронно. Об этом свидетельствует тот факт, что при гидрировании 1.2-диметилциклогексена-1 в присутствии платины образуется цис-изомер 1,2-диметилциклогексана.
При частичном гидрировании ацетиленовых углеводородов в присутствии металлов VIІІ группы (например, $Pt/BaSO_4$) с почти количественным выходом образуется цис-изомер алкена.
Согласно мультиплетной теории Баландина, реакция каталитического гидрирования алкенов протекает на активном центре, состоящем из двух атомов катализатора (дублет). Между активным центром катализатора и претерпевающим изменения фрагментом молекулы алкена существует структурное соответствие.
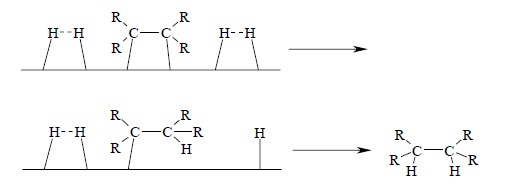
Согласно постулату мультиплетной теории, гемолитический разрыв связей в реагирующих веществах происходит между теми атомами реагентов, которые адсорбированы на разных атомах катализатора, и, наоборот, связь образуется между теми атомами участников реакции, которые адсорбированы на одном атоме катализатора. Применительно к рассматриваемой реакции это можно проиллюстрировать схемой:
Готовые работы на аналогичную тему
Так как образовавшийся в результате реакции предельный углеводород значительно менее прочно адсорбируется на поверхности катализатора, чем участники реакции, он сразу же десорбируется, не отравляя его активных центров.
Гетерогенное каталитическое гидрирование
Ниже приведены некоторые типичные примеры гетерогенного каталитического гидрирования ациклических и циклических алкенов:
Двойная связь в алкенах гидрируется с большей скоростью по сравнению со многими другими функциональными группами ($C=O$, $COOR$, $CN$ и др.) и поэтому гидрирование двойной $C=C$ связи часто представляет собой селективный процесс, если гидрирование ведется в мягких условиях (0 – 20ºС и при атмосферном давлении. Ниже приведены некоторые типичные примеры:
Гомогенное каталитическое гидрирование
Достижением в каталитическом гидрировании является открытие растворимых комплексов металлов, которые ускоряют гидрирование в гомогенном растворе. Большинство из этих катализаторов является ком-плексами ионов металлов платиновой группы, содержащими различные лиганды. Лиганды служат для увеличения растворимости комплексов в органической среде.
Многие из этих катализаторов обладают высокой селективностью.
Гомогенные катализаторы удобны также для направленного вве-дения дейтерия, поскольку обменные процессы, протекающие иногда при гетерогенном катализе, здесь минимальны.
Примерами таких катализаторов гомогенного гидрирования являются комплексы хлоридов родия (I) и рутения (III) с трифенилфосфином – трис-(трифенилфосфин)родийхлорид $[(C_6H_5)_3P]_3RhCl$ и гидрохлорид трис-(трифенилфосфин)-рутения $[(C_6H_5)_3P]_3RuHCl$. Наиболее доступен родиевый комплекс, который получается при взаимодействии хлорида родия (III) с трифенилфосфином (катализатор Дж. Уилкинсона). Родиевый комплекс Уилкинсона используется для гидрирования двойной связи в обычных условиях:
Интересным применением этих катализаторов является асимметрическое присоединение водорода. Для этого синтезированы хиральные катализаторы с оптически активными фосфиновыми лигандами. Их ис-пользование служит очень эффективным способом создания оптически активных центров, поскольку катализаторы не разрушаются.
Важное преимущество гомогенных катализаторов заключается в возможности селективного восстановления моно- и дизамещенной двойной связи по сравнению с три и тетразамещенной из-за больших различий в скорости гидрирования. Благодаря этому стало возможно селективное восстановление одной двойной связи в присутствии другой двойной связи в одной и той же молекуле:
Присоединение водорода происходит в цис-положение, восстановление цис-2-бутена дейтерием приводит к мезо-2,3-дидейтеробутану:
Получи деньги за свои студенческие работы
Курсовые, рефераты или другие работы
Автор этой статьи Дата последнего обновления статьи: 02 06 2021
Источник
Механизм гидрирования алкенов
Вы будете перенаправлены на Автор24
Гидрированне — это самая важная, и поэтому наиболее глубоко изученная каталитическая реакция. Она может осуществляться с использованием большого количества растворимых соединений $d$-металлов, однако наиболее активными катализаторами являются соединения металлов $VIII$ группы.
При гидрировании ненасыщенное соединение обычно активируется путем координации, а водород путем присоединения: окислительного, гомолитического или гетеролитического. Многие катализаторы активны в мягких условиях, т.е. при комнатной температуре и низком давлении водорода.
Катализаторы гидрирования
В лаборатории для гидрирования кратных углерод-углеродных связей чаще всего используют платину, палладий и никель Ренея. Самой активной из них является платина. С ее помощью можно гидрировать при комнатной температуре без давления даже стойкие ароматические связи. Никель Ренея и палладий менее активны. Они позволяют гидрировать при комнатной температуре неароматических кратные связи. Благодаря этому возможно селективное гидрирование, например, стирола в этилбензол. Гидрирование ароматических структур на менее активных катализаторах требуют повышения температуры до 150$^\circ$С и высокого давления 150-200 атм.
Активность катализатора зависит от условий его получения. Выбор катализатора зависит от устойчивости гидрированных веществ при данных условиях (температуре, кислотности среды и т.д.), от конструкции прибора, цены эксперимента. Металлические катализаторы очень чувствительны к катализаторным ядам (серо- и галогенсодержащим соединениям). Поэтому должны использоваться чистые вещества и растворители.
В последнее время найдено много активных и селективных катализаторов, применяющихся в различных реакциях:
Каталитическое восстановление в углеводороды жирноароматических, ароматических и алициклических кетонов:
Рисунок 1. Каталитическое восстановление в углеводороды жирноароматических, ароматических и алициклических кетонов. Автор24 — интернет-биржа студенческих работ
Восстановление нитрилов. ($Ni$ \ $ra$):
Рисунок 2. Восстановление нитрилов. ($Ni$ \ $ra$). Автор24 — интернет-биржа студенческих работ
Гидрирование ароматических систем:
Рисунок 3. Гидрирование ароматических систем. Автор24 — интернет-биржа студенческих работ
Рисунок 4. Гидрирование диенов. Автор24 — интернет-биржа студенческих работ
Готовые работы на аналогичную тему
Механизм каталитического гидрирования
В процессе каталитического гидрирования на поверхности катализатора образуется адсорбированный (хемосорбованый) атомарный водород, за счет которого происходит реакция гидрирования.
Считается, что реакция каталитического гидрирования имеет радикальный механизм.
Например, рассмотрим гидрирования этилена молекулой водорода в присутствии никелевого катализатора. Процесс проходит в несколько стадий.
На первой стадии молекула водорода и этилен в большом количестве адсорбируются на поверхности никеля, поскольку поверхность твердого тела имеет избыток свободной энергии. Адсорбированный водород образует комплексы с поверхностным атомом никеля, что приводит к резкой активации водорода. Одновременно $\pi$-электроны алкена образуют с $d$-орбиталями катализатора комплекс, способствует активации алкена. Затем активированный водород со стороны катализатора приближается к молекуле этилена и в результате взаимодействия образуется сложный комплекс.
На конечной стадии активный комплекс, образованный водородом, катализатором и этиленом, превращается в продукт реакции — этан, то есть происходит разрыв на поверхности катализатора в молекулы водорода и этилена и присоединение двух атомов водорода, где два атома углерода в этилене образуют две новых связи. Образуется этан, который легко десорбируется с поверхности катализатора, потому что в результате гидрирования $\pi$-связь переходит в $\sigma$-связь с образованием алкана.
После десорбции алкана освободившиеся места на поверхности катализатора увлекаются новыми молекулами этилена и водорода.
Схематично это можно изобразить так ($K$ — катализатор):
Рисунок 5. Схема. Автор24 — интернет-биржа студенческих работ
Восстановление алкенов
Водород присоединяется к кратным связям или действием химических средств восстановления, или каталитическим путем (действием водорода в присутствии катализатора).
Установлено, что изолированная двойная связь в алкенах может быть восстановлена (хотя и не полностью) натрием в жидком аммиаке (в присутствии метилового или этилового спирта) или амониакатом кальция ($Ca(NH_3)_6$).
Восстановление протекает лишь частично (на 11-20%). Легче всего восстанавливаются монозамещенные этилены (алкены-1). Нетерминальная двойная связь в этих условиях не восстанавливается.
Рисунок 6. Восстановление алкенов. Автор24 — интернет-биржа студенческих работ
Ранее считалось, что нетерминальные углеводороды с изолированным двойной связью (алкены) или системой изолированных двойных связей (алкадиены, алкаполиены) вообще нельзя восстановить химическими видновникаммы, например, водородом «в момент выделения». Такое название реакции «восстановления водородом в момент выделения» используют для реакций восстановления металлами (натрием, кальцием и другими металлами первой и второй группы таблицы Менделеева), их амальгамами или растворами в жидком аммиаке и в других протонных растворителях (в воде и спиртах). Позже были найдены случаи восстановления нетерминальных двойных связей таким путем.
Двойные связи восстанавливаются легче, если они находятся в сочетании с электроноакцепторными группами — карбоксильными или карбонильными.
Рисунок 7. Восстановление алкенов. Автор24 — интернет-биржа студенческих работ
Восстановление диенов
Легко восстанавливаются раствором натрия в жидком аммиака алкадиены сопряженных типов. Восстановление идет в 1,4 или в 1,2-положении, в зависимости от степени замещения крайних углеродных атомов в сопряженных системах, например:
Рисунок 8. Восстановление диенов. Автор24 — интернет-биржа студенческих работ
Реакции восстановления несопряжённых диенов похожи на таковые для изолированных двойных связей.
Источник