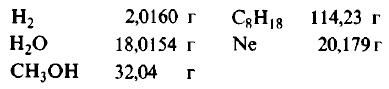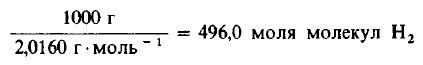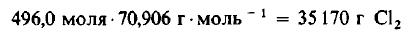- Урок 5. Моль и молярная масса
- Единица измерения количества вещества
- Молярная масса вещества
- Задачи на количество вещества
- Перевод из грамм в число моль и из числа моль в граммы
- Перевод из грамм в число молей и из числа молей в граммы
- Внезапно русский язык
- Моль, молярная масса и граммы: как они связаны
- Пример 1.
- Пример 2.
Урок 5. Моль и молярная масса
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·10 23 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·10 23 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12 C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·10 23 ).
Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·10 23 атомов . Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·10 23 молекул . Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
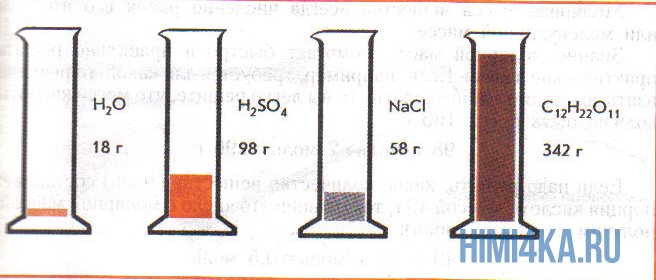
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·10 23 ; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·10 23 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·10 23 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·10 23 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·10 23 × 0,25 = 1,505·10 23 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·10 23 молекул/моль, что равно 2,99·10 26 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
Источник
Перевод из грамм в число моль и из числа моль в граммы
Калькулятор выполняет перевод из массы вещества, заданной в граммах, в количество вещества в молях и обратно.
Для задач по химии бывает нужно перевести массу вещества в граммах в количество вещества в молях и обратно.
Решается это через простое соотношение:
,
где — масса вещества в граммах, — количество вещества в молях, — молярная масса вещества в грамм/моль
Калькулятор ниже автоматически вычисляет молярную массу по формуле вещества и рассчитывает массу вещества в граммах или количество вещества в молях, в зависимости от выбора пользователя. Для справки также выводится молярная масса соединения и детали ее расчета
Химические элементы следует писать так, как они написаны в таблице Менделеева, т. е. учитывать большие и маленькие буквы. Например Co — кобальт, CO — моноксид углерода, угарный газ. Таким образом, Na3PO4 — правильно, na3po4, NA3PO4 — неправильно.
Перевод из грамм в число молей и из числа молей в граммы
Молярная масса — характеристика вещества, отношение массы вещества к количеству молей этого вещества, то есть масса одного моля вещества. Для отдельных химических элементов молярной массой является масса одного моля отдельных атомов этого элемента, то есть масса атомов вещества взятых в количестве равном числу Авогадро (собственно, число Авогадро — это число атомов углерода-12 в 12 граммах углерода-12). Таким образом молярная масса элемента, выраженная в г/моль, численно совпадает с молекулярной массой — массой атома элемента, выраженной в а. е. м. (атомная единица массы). А молярные массы сложных молекул (химических соединений) можно определить, суммируя молярные массы входящих в них элементов.
И, собственно, самым сложным моментом в расчете является определение молярной массы химического соединения.
К счастью, на нашем сайте уже есть калькулятор Молярная масса соединений, который подсчитывает молярную массу химических соединений, основываясь на данных по атомной массе из справочника Таблица Менделеева. Он и используется, чтобы получить молярную массу по введенной формуле химического соединения в калькуляторе.
Внезапно русский язык
Теперь небольшое отступление. При написании этого текста у меня возник вопрос — как правильно писать с точки зрения русского языка: перевод молей в литры или перевод моль в литры.
Согласно викисловарю, слово моль склоняется, т.е. моль, моля, молю, моль, молем, моле в единственном числе, и моли, молей, молям, моли, молями, молях во множественном числе.
При этом согласно Методическому указанию от 1979 года Государственного комитета СССР по стандартам, «Обозначение единиц, совпадающих с наименованиями этих единиц, по падежам и числам изменять не следует, если они помещены после числовых значений, а также в заголовках граф, боковиков таблиц и выводов, в пояснениях обозначений величин к формулам. К таким обозначениям относятся: бар, бэр, вар, моль, рад. Следует писать 1 моль, 2 моль, 5 моль и т.д. Исключение составляет обозначение «св.год», которое изменяется следующим образом: 1 св.год, 2,3,4 св.года, 5 св.лет.»
Таким образом получается что «перевод молей в литры» — правильно, а «перевод моль в литры» — неправильно, но «5 моль» — правильно, «5 молей» — неправильно.
Источник
Моль, молярная масса и граммы: как они связаны
Моль, молярная масса и граммы – эти понятия как-то связаны? Давайте-ка в этом разберёмся и порешаем задачи на молярную массу . Для начала вспоминаем, что моль – это количество вещества, в котором содержится 6,02*10 в двадцать третьей степени части (это число Авогадро).
Молярная масса показывает, сколько весит 1 моль того или иного вещества в граммах.
Молярная масса совпадает с атомной (если речь о простых вещества) или молекулярной (если речь о веществах сложных и газах, молекулы которых состоят из двух атомов, например, О2).
Это была теория. Но любую теорию нужно применять на практике, иначе зачем она нужна? Вот и займёмся этим.
У нас есть химическая реакция:
Из уравнения мы видим, что для неё нам нужна 1 молекула водорода и одна молекула фтора. Мы может взять, например, 10 молекул водорода, сколько нам в таком случае понадобится молекул фтора? Тоже 10. Мы можем взять и 100 молекул водорода, тогда потребуется и 100 молекул фтора. Кстати, заодно давайте уж узнаем, сколько молекул фторида водорода мы получим.
Из 1 молекулы водорода и 1 молекулы фтора получается две молекулы фторида водорода
(коэффициент в уравнении перед HF – 2). А если мы берём по 10 молекул водорода и фтора, то сколько получим HF? 20. Ну и взяв по 100 молекул водорода и фтора, мы получим 200 молекул фторида водорода.
Проблема в том, что молекулы настолько малы, что взять даже миллион молекул у человека не получится, это слишком маленькое количество вещества, которое на весах не взвесить. Вот тут и пришёл на помощь моль. Ещё раз запомните: в одном моле любого вещества содержится одно и то же число частиц!
Это очень важно для любых расчётов в химии. В 1 моле водорода содержится число Авогадро частиц, в 1 моле железа содержится число Авогадро частиц, в 1 моле воды содержится число Авогадро частиц, в 1 моле серной кислоты содержится число Авогадро частиц. Но! По массе моли веществ различаются, об это мы говорили раньше. И это обязательно нужно понять.
Теперь вернёмся к нашей реакции:
1 молекула Н2 + 1 молекула F2 = 2 молекулы HF
2 молекулы Н2 + 2 молекулы F2 = 4 молекулы HF
100 молекул Н2 + 100 молекул F2 = 200 молекул HF
Всё верно, ведь так?
А теперь вот так:
число Авогадро молекул Н2 + число Авогадро молекул F2 = число Авогадро молекул HF
1 моль Н2 + 1 моль F2 = 2 моль HF
И как же нам наконец перейти к граммам? Для этого вспоминаем, что молярная масса – это масса 1 моля вещества, совпадающая с атомной или молекулярной. Атомную или молекулярную массу мы определяем по таблице Менделеева : 1 моль водорода весит 2 г (атомная масса водорода 1, формула газообразного водорода Н2, поэтому его молекулярная масса 1*2=2), 1 моль фтора весит 38 г (атомная масса фтора 1, формула газообразного фтора F2, поэтому его молекулярная масса 19*2=38). Таким образом, для того, чтобы произошла реакция, нам нужно взять 2 г водорода и 38 граммов фтора. В этом случае оба вещества прореагируют полностью, образовав 40 граммов фторида водорода.
Теперь ещё пара задач на молярную массу с решениями.
Пример 1.
Сколько граммов оксида кальция и углекислого газа нужно взять, чтобы получить 50 граммов оксида кальция в реакции СаО + СО2 = СаСОз?
Первое, что нужно сделать, рассчитать молярные массы всех веществ. Используем периодическую таблицу, чтобы узнать атомные массы:
· молярная масса оксида кальция СаО 40+16=56 г/моль
· молярная масса углекислого газа СО2 12+2*16=44 г/ моль
· молярная масса карбоната кальция СаСО3 40+12+3*16=100 г/моль.
Давайте подумаем, сколько моль карбоната кальция СаСО3 составляют 50 г? 1 моль СаСО3 весит 100 г (см. выше на молярную массу). Следовательно 50г весят 0,5 моль. Это означает, что при проведении реакции в условиях задачи получится 0,5 моль карбоната кальция.
Второе, что нужно сделать, — понять в каком соотношении взяты вещества. Об этом нам говорят коэффициенты в уравнение:
СаО + СО2 = СаСОз
1 моль + 1 моль = 1 моль
Но мы уже выяснили, что в нашем случае мы получим всего 0,5 моль СаСОз. То есть и исходных веществ СаО и СО2 нужно взять по 0,5 моль. Переводя в граммы, получим, что оксида кальция требуется 56 г/моль*0,5 моль=28 г, а углекислого газа – 44 г/моль*0,5 моль=22 г. Это и есть ответ.
Пример 2.
Этот пример не из учебника химии, он сложный, но если вы его поймёте, вас никакой репетитор по химии уже не запугает. Пробуем!
Задача звучит так. Алюминий прореагировал с кислородом с образованием оксида алюминия. Известно, что в реакцию вступило 9 граммов алюминия. Определите, сколько получилось оксида алюминия в граммах.
Для начала запишем уравнение 4Al + 3O2 = 2Al2O3 и сразу увидим, что 4 моля алюминия, сгорев, образуют 2 моля оксида алюминия.
Теперь смотрим в таблицу Менделеева и определяемся с молярными массами:
· молярная масса алюминия 27 г/моль, с этим всё просто
· молярная масса оксида алюминия Al2O3 102 г/моль (помните, как мы считаем? 2*27 (это алюминий)+3*16 (это кислород)=54+48=102).
Из условия задачи мы узнали, что в реакцию вступило 9 г алюминия. 1 моль алюминия весит 27 г (это молярная масса). Следовательно, в реакцию вступило 9/27 моль алюминия, или 0,3 моль алюминия. Вернёмся к реакции:
4Al + 3O2 = 2Al2O3
4 моля алюминия при сгорании образуют 2 моля оксида алюминия
0,3 моля алюминия при сгорании образуют Х моля оксида алюминия
Находим Х=0,3*2/4=0,15 моль. Таким образом, если в реакции участвовало 9 г алюминия (или 0,3 моль), то получилось 0,15 моль оксида алюминия. Теперь самое простое – ищем массу в граммах. Припоминаем, что молярная масса оксида алюминия 102 г/моль. То есть 102 г весит 1 моль. А у нас всего 0,15 моль, и весит это количество вещества 102*0,15=15,3 г. Ответ на задачу: при сгорании 9 граммов алюминия получается 15,3 граммов оксида алюминия.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Источник