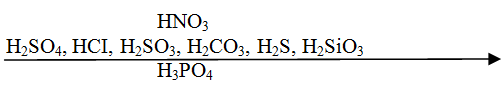- Химические свойства кислот, их классификация и реакции
- Общие свойства кислот. Классификация
- Химические свойства кислот
- 1. Диссоциация
- 2. Разложение
- 3. Реакция с металлами
- 4. Реакции с основаниями
- 5. Реакции кислот с солями
- 6. Реакция кислот с основными и амфотерными оксидами
- 7. Восстановительные свойства бескислородных кислот
- Физические свойства кислот
- Бескислородные килоты
- Химические свойства кислот
- Диссоциация
- Разложение
- Взаимодействие кислот с металлами
- Таблица: химические свойства кислот-окислителей
- Взаимодействие кислот с основаниями
- Взаимодействие кислот с солями
- Взаимодействие кислот с основными и амфотерными оксидами
- Восстановительные свойства бескислородных кислот
- Способность окрашивать индикаторы
- Вопросы для самоконтроля
- Краткий конспект подготовки к ЗНО по химии №10 Кислоты
Химические свойства кислот, их классификация и реакции
Общие свойства кислот. Классификация
Кислоты — класс сложных химических веществ, состоящих из атомов водорода и кислотных остатков.
В первую очередь кислоты делятся на:
- органические или карбоновые и
- неорганические или минеральные.
Свойства карбоновых кислот подробно разбираются в статье Карбоновые кислоты (ссылка на статью)
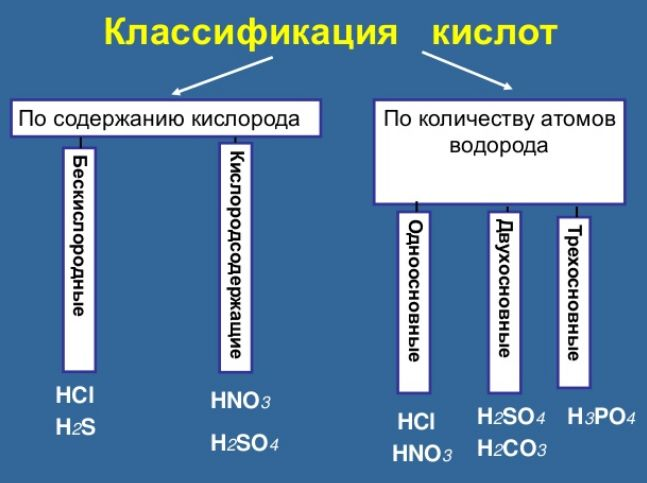
В зависимости от количества атомов водорода, которые могут замещаться в химических реакциях различают:
- одноосновные кислоты
- двухосновные кислоты
- трехосновные кислоты.
Не смотря на то, что в уксусной кислоте четыре атома водорода, три из них принадлежат кислотному остатку и в реакциях замещения не участвуют. Соответственно, уксусная кислота — одновалентная.
Свойства неорганических кислот также зависят от наличия в их составе кислорода и делятся на
Растворы кислот способны диссоциировать и проводить электрический ток т.е. являются электролитами. В зависимости от степени диссоциации делятся на:
Химические свойства кислот
1. Диссоциация
При диссоциации кислот образуются катионы водорода и анионы кислотного остатка.
Многоосновные кислоты диссоциируют ступенчато.
НРО 2- 4 ↔ Н + + PО З- 4 (третья ступень)
2. Разложение
Кислородсодержащие кислоты разлагаются на оксиды и воду.
Бескислородные на простые вещества
| t | ||
| 2HCl | → | Cl2 + H2. |
3. Реакция с металлами
Кислоты реагируют лишь с теми металлами, что стоят в ряду активности до кислорода. В результате взаимодействия образуется соль и выделяется водород.
Найти ряд активности можно на последней странице электронного учебника «Химия 9 класс» под редакцией В. В. Еремина.
Бдительные ученики могут сказать: «Золото стоит в ряду активности металлов после водорода, а с „царской водкой“ реагирует. Как же так?»
Из всех правил есть исключения.
Поскольку в состав азотной кислоты входит азот со степенью окисления +5, а в состав серной — сера со степенью окисления +6, то с металлами реагируют не ионы водорода, а более сильные окислители. Образуется соль, но не происходит выделения водорода.
4. Реакции с основаниями
В результате образуются соль и вода, происходит выделение тепла.
Реакции такого типа называются реакциями нейтрализации. Простейшая реакция, которую можно провести на собственной кухне — гашение соды столовым уксусом или 9%раствором уксусной кислоты.
5. Реакции кислот с солями
Вспомним, когда мы разбирали ионные уравнения ( ссылка на статью), одним из условий протекания реакций было образование в ходе взаимодействия нерастворимой соли, выделение летучего газа или слабо диссоциирующего вещества — например, воды. Те же условия сохраняются и для реакций кислот с солями.
6. Реакция кислот с основными и амфотерными оксидами
В ходе реакции образуется соль и происходит выделение воды.
7. Восстановительные свойства бескислородных кислот
Если в окислительных реакциях первую скрипку играет водород, то в восстановительных реакциях основная роль принадлежит анионному остатку. В результате реакций образуются свободные галогены.
Физические свойства кислот
При нормальных условиях (Атмосферное давление = 760 мм рт. ст. Температура воздуха 273,15 K = 0°C) кислоты чаще жидкости, хотя встречаются и твердые вещества: например ортофосфорная H3PO4 или кремниевая H2SiO3.
Некоторые кислоты представляют собой растворы газов в воде: фтороводородная-HF, соляная-HCl, бромоводородная-HBr.
Кислотные свойства кислот в ряду HF → HCl → HBr → HI усиливаются.
Для некоторых кислот (соляная, серная, уксусная) характерен специфический запах.
Благодаря наличию ионов водорода в составе, кислоты обладают характерным кислым вкусом.
Химическая лаборатория не ресторан, и в целях безопасности существует жесткий запрет на опробование на вкус химических веществ.
Как же можно определить кислота в пробирке или нет?
В 1300 году был открыт лакмус, и с тех пор алхимикам и химикам не пришлось рисковать своим здоровьем, пробуя на вкус содержимое пробирок. Запомните, что лакмус в кислой среде краснеет.
Вторым широко используемым индикатором является фенолфталеин.
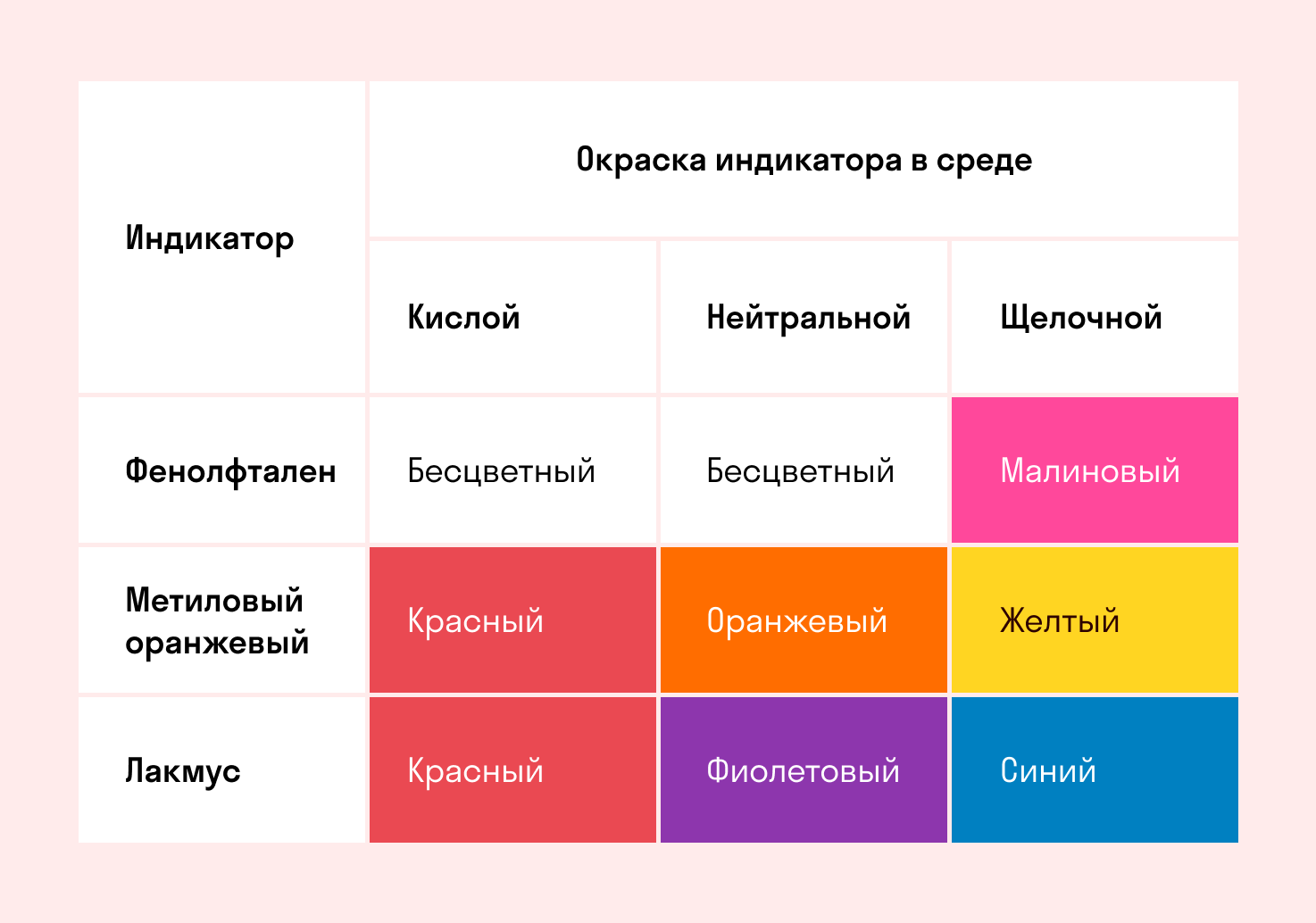
Простой мнемонический стишок поможет запомнить, как ведут себя индикаторы в разных средах.
Индикатор лакмус — красный
Кислоту укажет ясно.
Индикатор лакмус — синий,
Щёлочь здесь — не будь разиней,
Когда ж нейтральная среда,
Он фиолетовый всегда.
Фенолфталеиновый — в щелочах малиновый
Но несмотря на это в кислотах он без цвета.
Источник
Бескислородные килоты



Общая формула таких кислот HхЭу. Эта группа соединений по химическим свойствам и характеру диссоциации в водных средах (образование ионов гидроксония Н3О + ) сходна с кислородсодержащими кислотами, однако может быть выделена в отдельную группу, т.к. они не являются гидроксидами. Аналогично кислородным кислотам, они могут быть различной основности.
Название по систематической номенклатуре формируют следующим образом: на первом месте стоит слово «водород» с соответствующими количественными приставками, затем следует латинское название элемента с суффиксом «ид», например:
HCl- водород хлорид
H2S – диводород сульфид
HCNS — водород роданид
Наиболее распространенные бескислородные кислоты, название по полусистематической (международной) номенклатуре их кислотных остатков и солей приведены ниже:
| Формула | Название кислоты | Кислотный остаток | Название кислотного остатка и соли |
| HF | фтороводородная (плавиковая) | F — | фторид-ион, фториды |
| HCl | хлороводородная (соляная) | Cl — | хлорид-ион, хлориды |
| HBr | бромоводородная | Br — | бромид-ион, бромиды |
| HI | иодоводородная | I — | иодид-ион, иодиды |
| H2S | сероводородная | S 2- | сульфид-ион, сульфиды |
| HCN | циановодородная | CN — | цианид-ион, цианиды |
Название бескислородной кислоты: сочетание корня русского названия элемента и слова «водородная». (По полусистематической номенклатуре на первом месте — название кислотного остатка + слово «водорода», например HCl-хлорид водорода, H2S- сульфид водорода, в современной русской учебной литературе наиболее распространены названия, которые приведены в таблице).
Название кислотного остатка: корень латинского названия элемента с суффиксом «ид».
Как и основания, все кислоты, независимо от их состава являются электролитами разной силы и подразделяют в зависимости от степени диссоциации на сильные, слабые кислоты и кислоты средней силы.
Следует запомнить, что сильными кислотами являются следующие: H2SO4, HCl, HBr, HI, HNO3, HClO4, HMnO4.
Соли
Соли – сложные вещества, состоящие из катионов (положительно заряженных частиц, чаще всего атомы металла) и отрицательно заряженных кислотных остатков. Разделяют по видам на нормальные (средние), гидросоли (кислые соли), гидроксосоли (основные соли), двойные соли, смешанные и комплексные. Двойные соли содержат атомы двух металлов и общий кислотный остаток, например, алюмокалиевые квасцы — KAl (SO4)2·12H2O. Смешанные соли имеют в своем составе разные кислотные остатки, например CaOCl2— смешанная соль кислот HCl и HСlO. В составе комплексных солей присутствует комплексный катион, например, [Ag(NH3)2]Cl, или комплексный анион – Na[Al(OH)4]. Как правило, вне зависимости от растворимости, большинство солей являются сильными электролитами.
Источник
Химические свойства кислот
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Кислоты — это сложные химические вещества, состоящие из одного или нескольких атомов водорода, способных замещаться атомами металла, и кислотных остатков.
Рассмотрим подробнее общие свойства кислот.
Диссоциация
Кислоты — это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Диссоциация кислот происходит ступенчато. По способности к диссоциации кислоты разделяют на две группы:
Хорошо диссоциирующие (сильные): H2SO4, HCl, HBr, HNO3, HClO4, HI.
Разложение
В результате реакций разложения кислородсодержащих кислот образуются кислотный оксид и вода. Бескислородные кислоты образуют простые вещества. Для разложения некоторых кислот необходимо нагревание или излучение (HCl, HNO3, H3PO4) другие же разлагаются самопроизвольно в момент образования (H2CO3, H2SO3, HNO2).
Взаимодействие кислот с металлами
Металл может вытеснять водород из кислоты только в том случае, если металл стоит левее водорода в ряду активности металлов. Продукты реакции — соль и водород.
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Высокая окислительная способность серной и азотной кислот позволяет им вступать в реакции с металлами. Продукты реакции будут зависеть от активности металла и от концентрации кислот.
Таблица: химические свойства кислот-окислителей
На холоду — пассивация
На холоду — пассивация
Реакция не проходит
На холоду — пассивация
На холоду — пассивация
Взаимодействие кислот с основаниями
Кислоты реагируют с основаниями и амфотерными гидроксидами, в результате образуются соль и вода. Взаимодействие кислот с основаниями называют реакцией нейтрализации.
NaOH + HCl = NaCl + H2O
Взаимодействие кислот с солями
Сильные кислоты вытесняют слабые из растворов их солей, при этом образуются новая соль и новая кислота. Условие протекания реакции кислот с солями — одним из продуктов реакции должны быть нерастворимая соль или слабая кислота, вода, газ.
Взаимодействие кислот с основными и амфотерными оксидами
Кислоты вступают в реакцию с основными и амфотерными оксидами (последние ведут себя как основные оксиды). В результате реакции образуется соль и вода.
Восстановительные свойства бескислородных кислот
Бескислородные кислоты (кроме HF) проявляют восстановительные свойства за счет химического элемента, который входит в состав аниона, при действии на них различных окислителей.
Например, в качестве окислителей для всех галогеноводородных кислот выступают диоксид марганца MnO2, перманганат калия KMnO4, дихромат калия K2Cr2O7.
Результат этих реакций — образование свободных галогенов.
Из галогеноводородных кислот наибольшая восстановительная активность — у йодоводородной. Ее могут окислять оксид железа (III) и соль трехвалентного железа.
Высокая восстановительная активность характерна для сероводородной кислоты, она может быть окислена диоксидом серы.
Способность окрашивать индикаторы
Индикаторы кислот — это специальные вещества, при помощи которых определяют наличие кислот в растворе.
Вопросы для самоконтроля
С чем реагируют кислоты?
При каких условиях кислоты взаимодействуют с солями? Приведите пример.
Составьте уравнения реакций и назовите продукты реакций:
Разбавленный раствор серной кислоты реагирует с: медью, хлоридом меди, сульфатом меди, цинком?
Соляная кислота вступает в реакцию с каждым из двух веществ:
Источник
Краткий конспект подготовки к ЗНО по химии №10 Кислоты
Подготовка к ВНО. Химия.
Конспект 10. Кислоты
Общая характеристика кислот
Кислота – это сложное вещество, содержащие один или несколько атомов водорода, способных при химических реакциях замещаться на атомы металла и кислотного остатка.
Кислотным остатком называют часть молекулы кислоты, соединенную с атомом водорода
При замещении водорода в кислотах металлами, кислотные остатки переходят в неизменном виде в состав образующихся веществ – солей. Если кислотный остаток в кислоте соединен с одним атомом водорода, то он одновалентен, если с двумя — двухвалентен, если с тремя – трехвалентен и т.д.
Валентность кислотного остатка определяется количеством атомов водорода в кислоте.
Формулы и названия важнейших кислот указаны в таблице.
Важнейшие неорганические кислоты.
| Название кислоты | Формула кислоты | Кислотный остаток | Название солей |
| Фтороводородная (плавиковая) |  |  | Фторид |
| Хлороводородная (соляная) |  |  | Хлорид |
| Бромоводородная |  |  | Бромид |
| Угольная |  | =  | Карбонат |
| Кремниевая |  | =  | Силикат |
| Азотная |  |  | Нитрат |
| Ортофосфорная |  |  | Ортофосфат |
| Серная | =  | Сульфат | |
| Сернистая |  | =  | Сульфит |
| Сероводородная |  | =  | Сульфид |
Одним из представителей органических кислот является уксусная кислота 
Кислоты в природе
Слово «кислота» по значению связано со словом «кислый», так как имеют общий корень. Отсюда следует, что растворы всех кислот имеют кислый вкус.
Несмотря на это, не следует пробовать на вкус никакие растворы кислот, так как некоторые из них относятся к едким и ядовитым растворам.
Природные источники кислот.
В природе встречается много кислот: лимонная кислота в лимонах, яблочная кислота – в яблоках, щавелевая кислота – в листьях щавеля.
Муравьи защищаются от врагов, выбрасывая едкие капельки муравьиной кислоты. (Она же содержится в пчелином яде и жгучих волосках крапивы.)
При прокисании виноградного сока получается всем известная уксусная кислота (уксус), а при прокисании молока – молочная кислота, та же самая молочная кислота получается при квашении капусты.
Кислоты делят на несколько групп. К каждой группе принадлежат кислоты, сходные по определенным признакам.
1. Существуют бескислородные и кислородсодержащие кислоты. Название этих групп указывает на наличие или отсутствие в молекуле кислоты атомов кислорода.
2. Другой признак классификации кислот – количество атомов водорода в кислоте. Соответствующую характеристику кислоты называют основностью. Существуют одно-, двух-, трехосновные кислоты.
3. Приведем еще один признак классификации кислот, как электролитов по степени электролитической диссоциации. Кислота – это электролит, водный раствор которого содержит катионы водорода и анионы кислотного остатка. Если электролит диссоциирует практически нацело – это сильный электролит. Электролит, степень диссоциации которого мала, это слабый электролит.
Классификация по степени электролитической диссоциации.
| Признак классификации | ||
| Степень электролитической диссоциации | Сильные кислоты |  |
| Слабые кислоты |  |
Физические свойства кислот
Агрегатное состояние.
При обычных условиях кислоты могут быть твердыми веществами(ортофосфорная 


Такие газы как хлороводород 


Цвет.
Водные растворы соляной, азотной, серной, ортофосфорной и ряда других кислот не имеют окраски. Водные растворы хромовой кислоты 

Запах.
Некоторые кислоты имеют запах. Например, кислоты: 
Растворением в воде сероводорода получают сероводородную кислоту 
Растворимость, летучесть и стабильность некоторых кислот.
| Физические свойства | Группы кислот | Пример |
| Растворимость | Растворимые |  |
| Нерастворимые |  | |
| Летучесть | Летучие |  |
| Нелетучие |  | |
| Стабильность | Стабильные |  |
| Нестабильные |  |
Серная, соляная, уксусная кислоты могут вызывать сильные ожоги, разрушать ткани. Поэтому при работе с кислотами необходимо соблюдать меры предосторожности.
Если кислота попала на одежду или на поверхность тела, то её необходимо очень быстро смыть большим количеством проточной воды или нейтрализовать нашатырным спиртом.
Если кислота попала на деревянную, металлическую или на другие поверхности, то ее нейтрализуют известью, мелом или содой. Кислоты необходимо хранить в хорошо укупоренной посуде в недоступном месте для детей, и обязательно на таре должна быть бирка с названием кислоты.
Серная кислота является более сильной кислотой, чем соляная. Концентрированная серная кислота обугливает сахар, дерево, хлопок, шерсть и вызывает очень глубокие ожоги кожи.
При приготовлении раствора серной кислоты необходимо следовать следующему правилу: Кислоту льют в воду тонкой струйкой по стенке стеклянной посуды, но не наоборот.
Химические свойства кислот
1. Действие на индикаторы.
Кислоты в водных растворах изменяют окраску индикаторов.
В кислой среде фиолетовый лакмус приобретает красную окраску. Метиловый оранжевый – красную, а фенолфталеиновый – бесцветный. Если в раствор кислоты добавим по несколько капель универсального индикатора, он также поменяет окраску на красную.
Окраска индикаторов в различных средах.
2. Реакция с металлами.
Кислоты взаимодействуют с металлами, стоящими в ряду активности металлов до водорода. При этом получается соль и выделяется водород.
Металлы, расположенные в ряду активности металлов до водорода, вытесняют водород из кислот. Каждый предыдущий металл активнее, чем каждый последующий. 
Эта реакция относится к реакциям замещения.
Реакцию между простым и сложным веществами, в результате которой образуются новые простое и сложное вещества, называют реакцией замещения.
При реакциях азотной кислоты и концентрированной серной кислоты с металлами образуются соли, но водород не выделяется.
3. Реакция с основными и амфотерными оксидами с образованием соли и воды. 
Произошла реакция обмена: два сложных вещества обменялись своими составными частями.
4. Реагируют с основаниями. 

Реакция нейтрализации – реакция между кислотой и основанием, в результате которой получается соль и вода.
5.Реакция с солями.
Реакции кислот с солями не всегда возможны.
А. Кислоты реагируют с растворами солей, если в результате реакции один из продуктов выпадает в осадок. 


Б. Если кислота – продукт является летучей, происходит от газообразного соединения или разлагается с образованием газа. 


Сокращение (тв.) означает «твердое вещество», а (конц.) – «концентрированный раствор».
В. Если кислота, которая вступает в реакцию, является сильной, а кислота, которая образуется, – слабой.
Пользуясь вытеснительным рядом кислот можно предсказать течение реакции. Каждая предыдущая кислота может вытеснить из соли последующую.
Например,

но не будет происходить реакция между 


Вытеснительный ряд кислот.
Взаимодействие кислот с солями также относится к реакциям обмена.
6. Термическое разложение кислородсодержащих кислот.
Кислородсодержащие кислоты при нагревании, а угольная кислота и сернистая в обычных условиях, разлагаются с образованием соответствующих кислотных оксидов и воды:
Химические свойства кислот можно обобщить таким образом:
А. Изменяют цвет индикаторов
Б. Реагируют с металлами
В. Реагируют с основными и амфотерными оксидами
Г. Реагируют с основаниями
Д. Реагируют с солями (более слабых и летучих кислот)
Е. Некоторые кислоты разлагаются при нагревании.
В промышленности.
Наибольшее применение получили серная, соляная, азотная и ортофосфорная кислоты. Их получают на химических заводах в больших количествах.
| Кислота | Область применения |
 | Производство других кислот, солей, удобрений, красителей, лекарств, очистка нефтепродуктов. Серную кислоту, за счет ее свойств поглощать большие количества воды, используют для осушения. Применяется для приготовления аккумуляторной кислоты. |
 | Производство солей, красок, лекарств. |
 | Производство удобрений, красителей, взрывчатых веществ. |
 | Производство удобрений, моющих средств. |
В медицине.
Борная кислота — находит применение в медицине (борная мазь).
Ортофосфорная кислота широко применяется в стоматологии при пломбировании зубов. Ею протравливают зубную эмаль перед процедурой. Также в незначительных количествах ортофосфорная кислота применяется в составах отбеливателей для зубов.
Раствор соляной (хлороводородной) кислоты применяется для лечения заболеваний желудочно-кишечного тракта (гастрит, панкреатит).
В быту.
Лимонная кислота используется для выведения всевозможных пятен: от вина, различных ягод, красок, ржавчины, чернил.
Щавелевая кислота применяется для удаления пятен от чернил, краски, ржавчины. Кристаллическая кислота может вызвать ожоги слизистых оболочек ротовой полости, пищевода и желудка. Является ядовитым веществом.
Борная кислота – в качестве микроудобрения и средства для борьбы с тараканами и домовыми муравьями.
Уксусная кислота применяется либо в виде столового уксуса, с концентрацией кислоты до 9% или в виде 80 %-ной эссенции. Разбавленная кислота не действует на металлы, ткани растительного и животного происхождения, покровы человека и животных. Уксус применяется в качестве приправы к блюдам, удаления фруктовых пятен с тканей.
Соляная кислота хорошо растворяет металлы, в том числе цинк, олово, железо, но не взаимодействует с золотом, серебром и медью. Применяется для очистки от известкового налета раковины эмалированные и фаянсовые, унитазы, умывальники. Можно применять для очистки тканей от ржавых пятен, чернил (готовится слабый раствор кислоты). Соляная кислота разрушает ткани, изготовленные из льна, хлопка, искусственного шелка. При попадании на кожу вызывает химические ожоги.
Азотная кислота в быту используется только в виде разбавленных растворов для чистки изделий, в первую очередь из благородных металлов.
Общие способы получения кислот
1. Бескислородные кислоты получают при растворении в воде газообразных соединений неметаллов с водородом. Так, например, соляная кислота получается в результате растворения газа хлороводорода 


2. Кислородсодержащие кислоты можно получить взаимодействием соответствующих кислотных оксидов с водой. 
3. Получение кислот вытеснением из солей слабых кислот сильными, летучих нелетучими, растворимых – нерастворимыми. Например, сильная соляная кислота вытесняет слабую уксусную из растворов их солей. 


Тесты подготовки к ЗНО:
Online-тест подготовки к ЗНО по химии №12 «Кислоты»
Источник