Нейромолекулы: адреналин
Названия большинства нейромедиаторов мало что говорят непосвящённому человеку. Ацетилхолин, ГАМК, серотонин – просто набор странных звуков. То ли дело адреналин! Это слово тут же рождает целую бурю ассоциаций. В чьей-то голове возникнет брутальный профиль Джейсона Стэтхема из одноимённого фильма, кто-то представит себе отмороженного фрирайдера-экстремала летящего вниз по горному склону или вспомнит былые разборки с гопниками в соседнем дворе. Адреналин уже давно превратился в настоящую икону популярной культуры, став символом чего-то страшного, рискованного и по-своему притягательного. Но что же такое адреналин с точки зрения нейрофизиолога?
Начнём с истоков. Ещё в середине XIX века известный английский терапевт Генри Солтер включил в свою монографию об астме главу, посвящённую «стимулянтам». В это понятие он включил крепкий кофе, подавляющий сонливость, а также «сильные душевные эмоции». Действительно, приступы астмы обычно случаются во сне и никогда не происходят во время нервного напряжения. Однако природа этого эффекта долгие годы ускользала от физиологов.
В начале 1890-х годов немецкий фармаколог Карл Якобж (Jacobj), работая в лаборатории Освальда Шмидеберга исследовал влияние надпочечников на перистальтику кишечника. Электрическая стимуляция блуждающего нерва немедленно вызывала сокращения кишки, так же как и введение мускарина, алкалоида красного мухомора. Оба этих эффекта быстро исчезали при электрической стимуляции надпочечников. Казалось бы, результат говорил о том, что надпочечники способны выделять какое-то вещество, угнетающие перистальтику кишечника. Однако исследователи склонились к выводу, что действие надпочечников передаётся в кишечник через какие-то тончайшие нервные волокна, всё ещё не найденные анатомами.
В конце 1893-го года практикующий терапевт, англичанин Джордж Оливер, изобрёл инструмент, позволяющий измерять диаметр артерии подопытного, не прибегая к какому-либо повреждению кожи. Желая изучить действие ряда веществ на тонус лучевой артерии, Оливер, недолго думая, взял в качестве испытуемого собственного сына. На дворе был конец XIX века, и практика использования учёными членов своей семей в роли подопытных была самым обычным делом. Подкожное введение глицеринового экстракта надпочечной железы коровы привело к быстрому сокращению диаметра лучевой артерии мальчика. Взволнованный таким результатом, Оливер поделился своим наблюдением с лондонским профессором Эдваром Шафером, проводившим похожие исследования на анастезированных собаках. Профессор скептически отнёсся к рассказам коллеги. Тогда, дабы наверняка разрешить все сомнения, они вместе повторили эксперимент: на этот раз сын Оливера получил дозу экстракта надпочечника уже прямо по вене. Результат превзошёл все ожидания — столбик ртути в манометре моментально взлетел вверх, что говорило о быстром сокращении артерий и росте давления крови Справедливости ради, нужно сказать, что схожий результат почти одновременно был получен польскими учёными Владиславом Жимоновичем и Наполеоном Цыбульски (Władysław Szymonowicz and Napoleon Cybulski). Однако оба польских автора никогда не оспаривали приоритет Оливера и Шафера.
Вдохновлённые этими данными химики сразу из нескольких лабораторий мира начали гонку по выделению и очистке загадочного действующего начала экстракта. Первым успех улыбнулся Джону Абелю из Балтимора, выделившему еще не очищенное вещество и назвавшему его – эпинефрин. Именно под этим названием адреналин более известен сейчас в англоязычном мире. Но только в 1901 году, японскому химику Дзёкити Такаминэ удалось получить чистое соединение, которое вскоре начало производиться под торговой маркой «Адреналин».
Связанные одной цепью
С химической точки зрения адреналин – типичный член семейства нейромедиаторов-катехоламинов. Мы уже знакомы с двумя его близкими родственниками: дофамином и леводопой. Пращур всей этой семейки – аминокислота тирозин, которая благодаря работе целого каскада ферментов превращается сначала в леводопу, потом в дофамин, затем в норадреналин, и, наконец, после метилирования норадреналина на свет появляется адреналин. Рождаясь в реакциях одного метаболического пути, катехоламины имеют так же и общую систему расщепления. Их существование обрывается одним из двух ферментов: моноаминоксидазой, окисляющей катехоламины, либо и катехол-о-метилтрансферазой, присоединяющей метильную группу к одному из их гидроксилов. Многие антидепрессанты, а так же препараты против болезни Паркинсона временно подавляют работу этих ферментов, увеличивая содержание катехоламинов (в первую очередь дофамина) в мозге.
В 1904 году, меньше чем через 10 лет после работы Оливера и Шафера, берлинский невролог Макс Левандовски обнаружил, что экстракт надпочечника расширяет зрачок глаза, точно также как электрическая стимуляция ганглиев симпатической системы. Получив сообщение о результатах коллеги, Томас Элиотт, работавший в Кембридже, проводит кропотливое сравнение действия адреналина на различные органы и ответа тех же органов при стимуляции симпатических узлов электричеством. Реакции полностью совпали! Возможно именно адреналин является передатчиком информации от симпатических нервных окончаний к органам и тканям? Эта гипотеза оказалась пророческой, а адреналин стал первым открытым веществом-нейромедиатором в истории науки.
Двуликий Янус
По факту, адреналин является не только нейромедиатором, но и гормоном. Обе его роли тесно связаны с симпатической нервной системой. Как мы помним, внутренними органами тела управляет вегетативная нервная система. Она заботливо избавляет сознание от уймы лишних тревог, например — за переваривание пищи, работу желёз, регуляцию сокращений сердца. Как в любой приличной организации, в вегетативной системе работает принцип разделения обязанностей. Одна её часть, называемая парасимпатической системой, специализируется на том, что переводит внутренние органы в режим переваривания пищи и восстановления сил: активирует перистальтику кишечника, расширяет кровеносные сосуды пищеварительной системы, вместе с тем она сужает кровеносные сосуды мозга и мышц. Именно из-за неё послеобеденный час – не лучшее время для великих свершений. Смежная, симпатическая система наоборот подготавливает организм к реакциям типа борьбы или бегства. Она учащает сердцебиение, угнетает работу кишечника, расширяет просвет бронхов и диаметр зрачка, сужает сосуды внутренних органов, одновременно расширяя сосуды мышц.
Симпатическая нервная система состоит из центров, находящихся в головном и спинном мозге, нервов, отходящих от спинного мозга и двух тяжей узлов (ганглиев) вдоль позвоночника. Эти самые ганглии и стимулировали током Левандовски и Элиотт. Тела преганглионарных симпатических нейронов (тех, которые находятся перед ганглиями) расположены в спинном мозге, отростки же идут в ганглии. Из окончаний этих отростков выделяется нейромедиатор ацетилхолин. Он активирует постганглионарные нейроны, тела которых и составляют большую часть объёма симпатических ганглиев. Отростки этих нейронов идут к органам и тканям. Именно из их окончаний выделяется нейромедиатор адреналин, локально действуя на гладкие мышцы полых органов и кровеносных сосудов.
Но к каждому кровеносному сосуду невозможно подвести отдельный нерв. Поэтому адреналину пришлось взять на себя ещё и работу гормона. И тут пришло время вспомнить про надпочечники. Мозговое вещество надпочечников – это по сути, пара видоизменённых эволюцией симпатический ганглиев. Разве что их постганглионарные нейроны не имеют длинных отростков, а выделяют адреналин прямо в кровь, превращая нейромедиатор в гормон.
Бабочки в животе
В качестве гормона адреналин действует практически на все ткани. Его первоочердная задача – сделать так, чтобы организм выжил в опасной ситуации. Решая её, он мобилизует скрытые резервы, стимулируя энерговыделение и не стесняется отключать лишние, в данной ситуации, процессы синтеза и запасания. Попадая в печень, адреналин активирует расщепление гликогена до глюкозы, увеличивая её содержание в крови. Одновременно он запускает расщепление жиров и тормозит синтез белка. Под его действием угнетается перистальтика кишечника и теряется аппетит. Он усиливает процессы энергообмена и расширяет кровеносные сосуды в мышцах и лёгких. В большинстве остальных тканей он наоборот сужает сосуды, чтобы сэкономить энергетические ресурсы и поднять давление. Но самый верный признак выброса адреналина – учащение дыхания и частоты сердцебиения. Офисный работник, почувствовав все эти события на себе, воспримет их как надоевший стресс, влюблённый – как приятное порхание «бабочек в животе». А для спортсменов-экстремалов они вообще сливаются в настоящую адреналиновую эйфорию.
Благодаря своему быстрому сосудосуживающему эффекту и стимулирующему действию на все основные жизненные функции организма, адреналин стал незаменимой частью арсенала медиков. При различных видах шока и во время проведения реанимации введение адреналина – одна из первых мер помощи. Он быстро снимает отёки, стимулирует сердце и поднимает давление. А его способность сокращать сосуды используется в местной анестезии: при введении ультракаина в смеси с адреналином, анестезия действует гораздо дольше, ведь ультракаин медленнее вымывается из-за снижения кровотока. Так что, если стоматолог спрашивает: делать вам анестезию с адреналином или без – поймите его правильно! Он переживает из-за вашей возможной гипертонии, а не из-за того, что вы можете недополучить острых ощущений во время его работы.
Почему же на разные типы тканей адреналин действует так по-разному? Всё дело в разнообразии адренергических рецепторов. Все адренорецепторы принадлежат к метаботропным рецепторам, то есть не имеют ионного канала и реагируют на связь с адреналином изменением конфигурации и активацией G-белка (подробнее о них мы писали в статьях (см. «серотонин» и «глутамат»). Адренорецепторы делятся на две группы α-типа: α1, α2 и β-типа: β1, β2, β3. Каждый подтип рецептора специализируется на своей функции, а наличие на поверхности клетки рецепторов того или иного типа определит то, как она будет реагировать на адреналин. При этом адреналин не всегда является единственным естественным агонистом адренорецепторов, так, например, адренорецепторы α2-типа, локализованные в ЦНС активируются под действием его близкого родственника — норадреналина.
Как работают адренорецепторы
Любопытно, что введение адреналина влияет на работу долговременной памяти, увеличивая способность к запоминанию информации. С точки зрения эволюции, это вполне логично – если вам удалось выбраться из опасной ситуации, очень полезно хорошенько запомнить, из-за чего она произошла и как вы из неё выпутались.
Наверное, герой нашего сегодняшнего рассказа не зря получил свою скандальную известность. Его действие делает наше существование не только более длительным, но и ярким. Ведь с какой-то стороны, интересная жизнь – это просто умение правильно выбрать источник адреналина по своему вкусу.
Текст: Дмитрий Лебедев, ИБХ РАН при участии Алексея Паевского
Источник
Научная электронная библиотека
Тапбергенов С. О., Тапбергенов Т. С., Советов Б. С.,
3. Стресс и симпато-адреналовая система
Многочисленными исследованиями установлено, что роль пускового фактора во многих реакциях организма, в ответ на действие разнообразных агентов, играют гормоны мозгового вещества надпочечников, выполняющие одновременно роль медиаторов симпато-адреналовой системы. Экстренное выделение катехоламинов при действии внешних стимулов есть первое проявление стресса.
Согласно представлениям И.П. Павлова, реакция организма на чрезвычайное разражение и возникающие при этом повреждения органов, являются результатом нарушения трофики, вызываемых чрезмерной нервной импульсацией. На основании многочисленных исследований Л.А. Орбели построил теорию об адаптационно-трофической функции симпатической нервной системы. «С одной стороны, она (симпатическая нервная система) изменяет функциональные свойства, адаптация, с другой – вызывает существенные химические, физико-химические и физические сдвиги (трофики)» – Л.А. Орбели (1962).
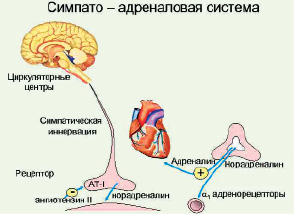
Рис. 8. Симпато-адреналовая система
Целым рядом исследований показано, что возбуждение симпато-адреналовой системы, сопровождаемое мобилизацией катехоламинов, является одной из ранних реакций организма на лучевое воздействие и свидетельствует о пусковой роли гормонов мозгового вещества в реакциях адаптации (В.С. Даниленко и др., 1970, Г.М. Мусагалиева и др., 1988).
Известно (А.М. Бару, 1968,), что увеличение или уменьшение коэффициента А/НА отражает степень активности периферического, либо центрального отдела симпато-адреналовой системы (САС). Установлено, что стресс может привести к нарушениям механизмов адаптационных реакций, к истощению медиаторного звена симпато-адреналовой системы.
Наблюдаемая при стрессе активация симпато-адреналовой системы носит компенсаторный характер и происходит за счет гуморального звена. Повышенная экскреция катехоламинов при стрессе также указывает на значительную активацию симпато-адреналовой системы.
Активация симпато-адреналовой системы при хирургическом стрессе вызывает нарушения гемодинамики, особенно эти нарушения выражены у больных с облитерирующими заболеваниями сосудов, у которых отмечаются снижение сердечного и ударного индексов, повышение общего периферического сопротивления сосудов.
Вместе с тем, активация симпато-адреналовой системы с относительным преобладанием гормонального звена в ближайшем послеоперационном периоде рассматривается как одно из неблагоприятных проявлений постишемического периода.
Длительно существующие высокие концентрации катехоламинов в крови отрицательно влияют на микроструктуру миокарда, вызывают аритмию, резко увеличивают содержание циклических нуклеотидов в клетках сердечной мышцы (Podzweit I. et al., 1981). Ежедневное, в течение 6 недель введение адреналина в дозе 100 мкг/кг веса вызывает изменения обмена веществ и функции органов, характерные для состояния длительной физической тренировки.
Установлено, что токсические дозы катехоламинов могут способствовать развитию аритмий (П.Ф. Литвицкий, 1979), уменьшению эффективности механической работы, повышению потребления кислорода, гипоксемии и развитию феномена «кислородной утечки» (М.Е. Райскина и др., 1963, И.В. Голубева, 1972, Opie L.H. et al., 1979).
Это действие катехоламинов сопровождается сменой прессорных влияний на депрессорные и вызвана стимуляцией бета2-адренорецепторов и может быть предотвращена введением кальция и бета-адреноблокадой (Opie L.H. et al., 1979). Введение токсических доз катехоламинов приводит к некротическим изменениям, воспалению и фибринозному перерождению миокарда (Haft J.I., 1973), нарушению структуры митохондрий (К.С. Митин и др., 1975).
Защитным действием к катехоламиновым некрозам миокарда обладают бета-адренолокаторы (В.В. Малышев и др., 1986 Kulig A. et al., 1973) и антиоксиданты типа витамина Е и этанол. Положительный эффект бета-адреноблокаторов наблюдается и при остром инфаркте миокарда (Edoute Y et al., 1981) и при нейрогенных поражениях миокарда, вызванных трехчасовой электростимуляцией дуги аорты (И.С. Заводская и др., 1977).
Большой цикл исследований по проблеме влияния стресса на кровообращение человека провели P. Obrist (1985) и Е.В. Белова (1987). Согласно этим работам, при стрессе характерно увеличение ЧСС, повышение минутного обьёма кровобращения (МОК) и систолического АД, при отсутствии повышения общего периферического сопротивления сосудов (ОПС), а при корректурной пробе – увеличение ОПС и диастолического АД, без повышения МОК.
В других работах (Б.М. Федоров, 1991) отмечено, что во время стрессового воздействия при напряженной умственной работе показатели кровообращения в различных случаях изменяются не однотипно. В ряде наблюдений вначале отмечается снижение ОПС сосудов и увеличение МОК. По мере нарастания стрессорной реакции характер изменений системной гемодинамики существенно изменялся. При этом снижение тонуса сосудов большого круга кровообращения сменяется его повышением. Соответственно более резко повышается АД и менее значительно повышается или даже снижается МОК.
В стрессорных ситуациях изменяется сердечная деятельность, состояние артериальных и венозных сосудов, микрогемоциркуляция. Учащение сердечных сокращений лишь до определенного предела отражает выраженность стрессорной реакции.
Нарушения кровообращения четко коррелируют с динамикой стрессорных реакций. Влияние стрессов на кровообращение на микроциркуляторном уровне выражается в констрикции артериол, появлением агрегатов эритроцитов, нарушением сосудистой проницаемости, замедлением кровотока в венах, а затем в артериолах, возникновением стазов.
Установлено, что изменения активности симпатической нервной системы, общего периферического сопротивления сосудов и среднего артериального давления в ходе хирургического стресса имеют однонаправленный характер (Т.С. Тапбергенов, 1992).
При психоэмоциональном стрессе отмечено изменение реологических свойств крови, в частности, увеличение ее вязкости и проницаемости стенок венулярных сосудов.
Как показано исследованиями Т.С. Тапбергенова (1992), при хирургическом стрессе степень выраженности изменений показателей вегетативной регуляции и центральной гемодинамики зависят от исходного состояния каждого из них и этапа оперативного вмешательства. При исходно высоком тонусе симпатического отдела вегетативной нервной системы его влияние на среднее артериальное давление и тонус сосудов компенсирует, ожидаемое в начале операции, угнетение сердечно-сосудистой системы, а исходно низкая симпатическая активность вегетативной регуляции усугубляет гемодинамические нарушения в ходе хирургического вмешательства.
В происхождении различных вариантов изменений гемодинамики в стрессорных и экстремальных ситуациях существенное значение имеют изменения венозного возврата крови к сердцу. Так развитие прессорной реакции, вызванной введением катехоламинов, в начальном периоде связано с изменениями тонуса артерий и соответственно повышением общего периферического сопротивления.
При дальнейшем развитии прессорной реакции, вызванной катехоламинами, характерно повышение роли венозного возврата в формировании величины сердечного выброса. Роль этих изменений в поддержании высоких показателей АД становится весьма существенной, составляя до 50 % вклада в реализацию эффекта гипертензии (Б.Я. Зонис, 1986). Давление в венах, состояние окружающих их тканей, в частности скелетных мышц, и особенно симпатическая стимуляция венозного тонуса, чувствительность альфа-адренорецепторов, обеспечивающих констрикторные эффекты – все это отражается на изменении просвета сосудов, емкости венозного русла и возврате крови к сердцу.
Показана возможность в условиях патологии значительного увеличения объёма вен и задержки в них крови при сочетании повышенного давления в растянутых венах с адренергической стимуляцией венозных «сфинктеров», расположенных в области венозных клапанов. При стрессорных воздействиях возникновение коллаптоидных состояний может быть следствием резкого снижения возврата венозной крови к сердцу. Повышение тонуса венозных сосудов и увеличение венозного возврата рассматривается как существенный фактор в патогенезе гипертонии.
Анализ результатов реакции торможения миграции лимфоцитов (РТМЛ) с митогеном конкавалином А (Соn A) в присутствии различных концентраций норадреналина, позволяющей оценить чувствительность адренорецепторов (В.Р. Вебер, 1992), показал, что на разных этапах хирургического стресса имеет место снижение индекса чувствительности адренорецепторов лимфоцитов к норадреналину (табл. 1).
Индекс торможения миграции лимфоцитов при хирургическом стрессе (на 100 клеток, М ± m)
Источник